5.1. Índices predictivos de asma en edad escolar
Preguntas para responder:
- ¿Cuál es el índice predictivo más apropiado para predecir la evolución a asma en niños menores de tres años con clínica de sibilancias?
- ¿La frecuencia de episodios de sibilancias podría servir como índice predictivo de asma persistente en edad escolar?
Las sibilancias recurrentes son un problema muy frecuente en los primeros años de vida. Hasta un 30 o 40% de los niños presentan síntomas «asmáticos» (sibilancias, disnea o tos persistente) en esa franja etaria. Sin embargo, solo el 30% de los niños con sibilancias van a persistir con esa clínica a los 6 años de edad. Desde el punto de vista clínico sería muy útil disponer de un «índice de riesgo», combinando antcedentes con hallazgos clínicos o de laboratorio, que permitiera identificar aquellos niños con mayor probabilidad de desarrollar un asma persistente en el tiempo. Ya que, aunque no se modifica el curso natural de la enfermedad, en los niños con síntomas y alto riesgo de persistencia se recomienda iniciar tratamiento farmacológico para disminuir la morbilidad. Con el objetivo de ayudar al clínico a identificar a los niños que continuarán con sibilancias en edad escolar, se han estudiado varios modelos de predicción o indicadores clínicos de riesgo. Estos modelos han empleado diversos factores de riesgo asociados con el desarrollo de asma en estudios epidemiológicos, tales como la historia familiar de la sensibilización alérgica y asma, la historia de sibilancias, enfermedad atópica en el niño, los niveles de inmunoglobulina E (IgE), y los perfiles de secreción de citosina. Cuando se publicó la guía de asma en el 2005 (21), se disponía de dos índices (71, 72) y un tercero que fue una modificación parcial del primero de ellos (73). Ambos índices mostraban problemas de aplicabilidad ya que no fueron validados en poblaciones diferentes a las originales (74). En el estudio inglés de Kurukulaaratchy et al. (73) la población presentaba una prevalencia de asma muy superior a la observada en nuestra comunidad. En el estudio de Castro-Rodríguez et al. (71) no se utilizó un análisis multivariante para la construcción de la regla de predicción. En la GPC sobre asma (21) se recomendaba «hasta que se desarrollen nuevas escalas de mayor exactitud y que hayan sido validadas en nuestro entorno», la utilización del índice de Castro-Rodríguez modificado (73). En la presente revisión se pretende actualizar la evidencia referente a la utilización del índice predictivo propuesto en la guía, y su posible aplicación en nuestro contexto.
Evidencia científica
Las GPC seleccionadas (45, 46) definen los posibles factores predictivos implicados en la evolución a asma en épocas más tardías en los niños menores de tres años, haciendo referencia a la presencia de más de un episodio de sibilancias, dificultad respiratoria, opresión torácica y/o tos, y obstrucción respiratoria variable. Además, la guía de SIGN (45) reconoce que en el primer episodio de sibilancia infantil no es posible distinguir entre los diferentes patrones clínicos («fenotipos») que determinarán la persistencia de sibilancias y el desarrollo de asma posterior. La guía SIGN (45) recomienda la evaluación cuidadosa inicial del niño prestando especial atención a: sibilancias, tos, dificultad respiratoria y opresión torácica. La guía GEMA (46) recomienda la utilización del IPA (Índice Predictivo de Asma) modificado recomendado en la guía de 2005 (21).
En la bibliografía se han identificado varios estudios que pretendían validar en nuevas poblaciones los índices predictivos existentes (IPA y PIAMA (Prevention and Incidence of Asthma and Mite Allergy)), y proponer nuevos índices en general más sencillos. Teniendo en cuenta que el test de referencia o estándar de estas herramientas predictivas es el diagnóstico clínico al de unos años, se ha considerado como criterio de inclusión la utilización en una misma población de la nueva herramienta a estudio y el índice predictivo de asma (IPA) recomendado en la guía de asma (21). Así, se han seleccionado tres estudios (75-77) de cohorte longitudinal prospectiva y otro estudio de casos y controles anidados (78) de una cohorte poblacional; los estudios comparan los resultados de aplicación de nuevos índices predictivos en una población preescolar con los resultados de la aplicación del índice IPA propuesto por Castro-Rodríguez et al. (71) en la misma población, utilizando como test de referencia o Gold Standard el diagnóstico clínico de asma en edad escolar. Se han excluido cuatro estudios (72, 79-81) que aun proponiendo nuevos índices predictivos no los comparan con la aplicación del índice de nuestro interés (IPA). Ninguno de los estudios seleccionados se ha realizado en nuestro contexto, uno se ha realizado en Inglaterra (76), otro en Noruega (78). y los otros dos en Latinoamérica (Colombia (77). y Cuba (75)). Los estudios europeos se realizan a través de encuestas realizadas a padres de una base poblacional de niños, aunque también aportan datos de la subpoblación de mayor riesgo, de pacientes preescolares con sibilancias recurrentes. Los otros dos estudios validan el índice predictivo en población de riesgo con sibilancias recurrentes y en el cuarto se incluyen a niños hospitalizados por cuadros de sibilancias. Ninguno de los estudios describe herramientas que hayan sido validadas en su diseño. Para evaluar la validez del IPA estricto, recomendado en la guía del asma del 2005 (21) para predecir el diagnóstico de asma en edad escolar de aquellos pacientes preescolares con sibilancias recurrentes que acuden a consulta, se han tenido en cuenta los resultados de su aplicación en los diferentes estudios. La gran heterogeneidad existente entre los estudios, debido a las diferencias de prevalencia de asma que oscila entre un 22% a un 35% y a las diferencias de poblaciones de validación con diferente severidad en los diferentes estudios (en dos de los estudios es de base poblacional, en otro se trata de una población con sibilancias recurrentes y en el cuarto se incluyen a niños hospitalizados por cuadros de sibilancias), habría impedido la combinación de resultados por lo que no se ha realizado el metaanálisis de los mismos. Los datos relacionados con la validez del IPA estricto de cada estudio muestran una sensibilidad del IPA estricto que oscila entre el 43% y el 78% y valores de especificidad entre el 18% y 83% (Ver Figura 1).

Los valores predictivos positivos (VPP) van desde el 34% hasta el 47% y los negativos (VPN) desde el 61% al 87%.
Esto supondría que en una población de 1000 pacientes (en cada uno de los estudios), desde un 22% hasta un 61% de la población será incorrectamente clasificado con el IPA estricto: desde un 13% hasta un 53% de los niños serán tratados de forma innecesaria con glucocorticoides inhalados, falsos positivos (FP) y desde un 7% hasta un 13% de los niños se les retrasará el inicio del tratamiento falsos negativos (FN). Nuestro interés se centra en resultados que minimicen el diagnóstico incorrecto y sobre todo que haya menos pacientes tratados entre los que no deberían haber sido tratados (FP). En los resultados se observa que cuando mayor es la prevalencia de la enfermedad en población escolar peor se comporta el IPA, y éste muestra mejores resultados en muestras poblacionales, es decir, en población similar en la que fue originalmente desarrollada. Se observa heterogeniedad entre los estudios, debido sobre todo al estudio cubano donde se incluyen a pacientes con sintomatología más grave, niños que han estado ingresados en el hospital por cuadros de sibilancias. Posiblemente también explicada por las diferentes características poblacionales y la variabilidad de la prevalencia de asma (desde un 21% hasta un 35%) e incidencia de algunas de las enfermedades (dermatitis atópica) valoradas en el IPA. Además, se trata de un índice no validado en el contexto español. La capacidad predictiva del IPA en las poblaciones de los estudios no es para nada satisfactoria, en el mejor de los casos se ha observado un coeficiente de verosimilitud positivo (LR+) y negativo (LR-) de 3,34 y 0,72, respectivamente, en un estudio de base poblacional (78), resultados similares a los obtenidos en la muestra de base poblacional donde fue desarrollada. Los resultados de validez del índice IPA siguen sin ser favorables y siguen siendo necesarios estudios que validen el índice propuesto en nuestro contexto, así como el desarrollo de nuevos índices con mayor capacidad predictiva. En relación a la validez de los nuevos índices propuestos en los estudios seleccionados, cabe mencionar que dos de ellos (76, 78) son índices sencillos basados en la frecuencia de exacerbaciones. Los otros dos (75-77), además de la frecuencia de sibilancias, también incluyen otros factores de riesgo.
Rodríguez-Martínez et al. (77) pretenden comparar el comportamiento de la también conocida escala de puntuación PIAMA en una población de preescolares con sibilancias recurrentes o con alguna sibilancia con el comportamiento del IPA. Para ello se aplican ambos índices en la misma población de edad preescolar y el diagnóstico clínico de dicha población en edad escolar. Por falta de datos, no toda la muestra estudiada con el PIAMA pudo clasificarse con el IPA y la prevalencia de asma observada en la muestra analizada con PIAMA fue mucho mayor que en la muestra que pudo ser clasificada con IPA (53,7% frente a 22,6%). Los resultados mostraron que en dicha población, un 34% de la población fueron mal clasificados con el PIAMA (9% de FP y 24% de FN) y un 29% con IPA (16% de FP y 12% de FN). Aun así, los valores de LR para ambos test fueron similares que el IPA (LR+ 2,59 para PIAMA frente a 2,06 para IPA y LR- 0,58 frente a 0,72 respectivamente).
Coronel C et al. (75), por su parte, proponen un nuevo índice no desarrollado mediante análisis multivariante y no validado, y comparan su aplicación con la aplicación del IPA en la misma población hospitalaria de 312 pacientes menores de tres años ingresados por presentar tres o más episodios de sibilancias en el último año, asociados o no a resfriados. Con una prevalencia de sibilancias del 34.6% el nuevo índice propuesto se comporta con exactitud mostrando un LR+ de 12,4 y un LR- de 0,09, con tan solo 8% de diagnósticos desacertados (5% de FP y 3% de FN). Por el contrario, el IPA muestra un LR+ de 0,95 y un LR- de 1,19, con un 60% de diagnósticos desacertados (53% de FP y 7% de FN), completamente inadecuado para dicha población. Se cree que estos resultados desfavorables puedan ser debidos a la población más severa incluida en este estudio, aunque se desconoce su razón real. Dos de los estudios incluidos comparan el IPA estricto con índices sencillos basados en la frecuencia de sibilancias. En el primero de ellos (76) realiza una validación del índice IPA en una cohorte de base poblacional en Reino Unido comparándolo con el nuevo índice más sencillo (tabla a). El estudio evaluó el riesgo de asma en edad escolar mediante un índice basado en la frecuencia de sibilancias a los tres años en 1954 pacientes infantiles y comparó el riesgo con las tasas de asma a los siete y 10 años.

Cuando se analiza la cohorte del estudio con ambos índices (el nuevo propuesto y el IPA) se obtienen unos resultados comparables: Nuevo índice- EFW: S: 41(34-48) %, E: 91(89-92) %, VPP: 36%(30-42), VPN: 92 (91-93)%, LR+:4,56 (vs. IPA estricto: S: 37%(30-44), E: 93% (92-95), VPP: 40% (32-48), VPN: 93% (91-94), LR+: 5,29). En el estudio se realiza un análisis de sensibilidad, en la que se muestran los resultados de la validez de los dos índices en una superpoblación de solo pacientes infantiles con sibilancias precoces a los tres años. Esta es una población más cercana a la de nuestro interés, que serían los niños que acuden a consulta por sibilancias, por eso nos hemos basado en la evaluación de los resultados de dicho sub-análisis:
Seleccionando como punto de cohorte la existencia de ≥ 4 crisis en el último año evaluado a los dos o tres años, es decir la categoría EFW del nuevo índice propuesto, se observa una S: 55%, E: 74%, VPP: 36%, VPN: 86%, LR+:2,12 y LR- 0,61 (vs. IPA Estricto: S: 49% , E: 81%, VPP: 40%, VPN: 86%, LR+: 2,58 y LR- 0,63). Ambos índices obtienen un LR+ insuficiente para confirmar el diagnóstico de asma. Esto supone que para la prevalencia del estudio, 32%: un 32,1% de la población será incorrectamente clasificado con el nuevo índice propuesto, 14,5% de los niños serán tratados de forma innecesaria con glucocorticoides inhalados (FP) y al 17,6% se les retrasará el inicio del tratamiento (FN). Para una prevalencia del 28% (estimada en nuestro contexto) habrá un 19% de FP y un 12,6% de FN.
El segundo de los estudios (78) pretende evaluar si la severidad de episodios de obstrucción de vías respiratorias (OVR) en los dos primeros años predice el asma a los diez años. Para ello propone un índice o escala de riesgo basado en la frecuencia y persistencia de OVR y hospitalizaciones durante los dos primeros años (Tabla b). Selecciona una muestra de casos y controles de una cohorte poblacional de nacimiento y realiza análisis mediante regresión logística ajustado por sexo, atopia familiar y dermatitis atópica, así como por sensibilización alérgica a los dos años.

Cuando se analiza la cohorte del estudio con el nuevo índice propuesto se obtienen mejores resultados que los obtenidos con el índice IPA en la misma población. Seleccionando como punto de cohorte una puntuación >5 en la escala de severidad el nuevo índice muestra una: S: 51%, E:88%, VPP: 54%, VPN:87% y LR+ 4,33 y LR- de 0,55 (vs. IPA Estricto: S:57%, E:83%, VPP:48%, VPN:87%, LR+:3,34 y LR- de 0,52). Esto supone que para la prevalencia del estudio, 21,3%: un 20% de la población será incorrectamente clasificado, 9,8% de los niños serán tratados de forma innecesaria con glucocorticoides inhalados (FP) y al 10,5% se les retrasará el inicio del tratamiento (FN). Para una prevalencia del 28% (estimada en nuestro contexto) habrá un 8,6% de FP y un 13,7% de FN. Se trata de un solo estudio de casos y controles anidado a una cohorte prospectiva que evalúa este índice, con un número discreto de pacientes, el índice no está validado en nuestra población lo que supone una incertidumbre sobre si su comportamiento será el mismo que el de la población original (evidencia indirecta) por ello se considera que la calidad de la evidencia es baja. En resumen, se considera que la escala de puntuación PIAMA (77) y el nuevo índice propuesto por Coronel et al. (75) no aportan beneficios significativos frente al IPA y tampoco suponen una ventaja para su aplicación en nuestro medio de interés. En relación con los índices basados en sibilancias muestran resultados comparables al IPA. Los resultados del índice propuesto por Devulapalli et al. (78) proceden de su aplicación en una muestra de casos y controles procedentes de una muestra poblacional; mientras que los resultados del índice propuesto por Leonardi et al. (76) proceden de una población más similar a la de nuestro interés y por ello se confía más en su aplicabilidad en la misma.
Resumen de la evidencia
|
Calidad muy baja
|
Las estimaciones de validez del IPA estricto muestran altas tasas de FP y un muy bajo valor predicitivo. Desde un 16% hasta un 66% de la población será incorrectamente clasificado, en poblaciones con diferentes prevalencias de enfermedad. Además, el índice no está validado en su diseño, ni en nuestro contexto (75-78). |
|
Calidad baja
|
El nuevo índice propuesto por Coronel se comporta con exactitud mostrando solo un 8% de diagnósticos desacertados (5% de FP y 3% de FN) en una población hospitalaria, con una prevalencia de sibilancias del 34,6%. El índice no fue desarrollado mediante análisis multivariante, ni fue validado en su diseño ni en nuestro contexto (75). |
|
Calidad baja
|
Las estimaciones de validez de la nueva escala de riesgo basado en la frecuencia de obstrucción de vías respiratorias y hospitalizaciones durante los dos primeros años, propuesta por Devulapalli y seleccionando como punto de cohorte una puntuación >5 en la escala de severidad, muestra un 20% de clasificaciones incorrecta (10% de FP y 10% de FN) en una muestra infantil de base poblacional. El índice no está validado en su diseño, ni en nuestro contexto (78). |
|
Calidad moderada
|
El índice propuesto por Leonardi y basado en la frecuencia de sibilancias muestra altas tasas de pacientes incorrectamente clasificados (un 32% de pacientes: 17,6% de FP y 14,5% de FN) en la subpoblación de pacientes infantiles con sibilancias precoz a los tres años. El índice no está validado en su diseño, ni en nuestro contexto (76). |
|
Calidad baja
|
El índice nuevo propuesto por Rodríguez-Martínez conocido como escala de puntuación PIAMA, muestra que un 34% de la población de preescolares, de riesgo con sibilancias recurrentes o con alguna sibilancia, fueron mal clasificados (9% de FP y 24% de FN). El índice no está validado en su diseño, ni en nuestro contexto (77). |
De la Evidencia a la recomendación
Los aspectos que han determinado la fuerza y la dirección de esta recomendación han sido los siguientes:
- La calidad global de la evidencia es la siguiente para cada una de las comparaciones: • C1: Herramienta de predicción IPA estricto VS. Diagnóstico clínico (a los seis años), muy baja. • C2: Herramienta Nueva-1 (Coronel) VS. Diagnóstico clínico (a los seis años), baja. • C3: Herramienta Nueva-2 (Devulapalli) VS. Diagnóstico clínico (a los 10 años), baja. • C4: Herramienta Nueva-3 (Leonardi) VS. Diagnóstico clínico (a los seis años), moderada. • C5: Herramienta Nueva-4 (PIAMA-Rodríguez) VS. Diagnóstico clínico (a los seis años), baja.Tres de los estudios aportan resultados procedentes de respuestas de familiares, en un estudio hay pérdidas no explicadas, y en otros dos existen otras posibles causas de riesgo de sesgo. Las poblaciones de validación son muy diferentes: dos de los estudios son de base poblacional, en otro estudio se trata de una población con sibilancias recurrentes y en el cuarto se incluyen niños hospitalizados. Se trata de índices no validados en el contexto español.
- El balance entre beneficios y riesgos: para C1, C3, C4 y C5 los beneficios y riesgos/inconvenientes están equilibrados y para C2 los riesgos/inconvenientes superan ligeramente los beneficios. Herramienta 1: Resultados IPA sin combinar:En una población de 1000 habitantes con una prevalencia de enfermedad desde un 22% hasta un 35%: Desde un 16% hasta un 66% de la población será incorrectamente clasificado con los diferentes índices: desde un 14% hasta un 53% de los niños serán tratados de forma innecesaria con glucocorticoides inhalados (FP) y desde un 2% hasta un 13% de los niños se les retrasará el inicio del tratamiento(FN). Herramienta 2: Para una prevalencia del 34,6%: un 8% de los niños fueron mal clasificados con un 5% de FP y 3% de FN.- para una prevalencia del 28% (estimada en nuestro contexto): 58% de FP y un 6% de FN. Herramienta 3: Para una prevalencia de 21,3% un 20% de niños fueron mal clasificados: 9,8% de FP y 10,5 de FN.- para una prevalencia del 28% (estimada en nuestro contexto): 13,3% de FP y un 9,4% de FN. Herramienta 4: Para una prevalencia del estudio 32%: El 32,1% de la población será incorrectamente clasificado, 14,5% de los niños serán tratados de forma inncesesaria con glucocorticoides inhalados y al 17,6% se les retrasará el inicio del tratamiento.- para una prevalencia del 28% (estimada en nuestro contexto): habrá un 18,7 de FP y un 12,6% de FN. Herramienta 5: Para una prevalencia del 53% un 34% de la población fueron mal clasificados (9% de FP y 24% de FN)- para una prevalencia del 28% (estimada en nuestro contexto): 15% de FP y un 16% de FN. Nos interesa la validación del IP y las herramientas 3 y 4, que son las basadas en la frecuencia de sibilancias.
- Valores y preferencias de pacientes y/o sus ciudadores: incertidumbre o variabilidad importantes en la opinión sobre los desenlaces.Incertidumbre sobre si las implicaciones serán consideradas igual por clínicos o por pacientes, y si habrá variabiliad dentro de la población.Los índices que precisan extracción sanguínea pueden suponer una menor aceptabilidad por parte de los padres de los pacientes.
- Costes y uso de recursos: los costes son bajos en relación a los beneficios.Se trata de índices predictivos que necesitan de recursos y tiempo en consulta para la evaluación de los datos. Los exámenes complementarios y el prick test son más costosos en tiempo y recursos, mientras que la utilización de índices basados en sibilancias implicaría un menor uso de recursos y costes por tratarse de unas reglas predictivas muy sencillas de realizar con datos disponibles en el lugar de aplicación (tanto en cribado como en consulta), aunque con mayores resultados falsos que con el índice IPA en el caso del índice propuesto por Leonardi, lo que podría llevar a un consumo mayor de recursos por consultas médicas por asma mal controlado.Por lo tanto, Herramienta IPA: IPA- La calidad global de las estimaciones de validez del IPA en los estudios evaluados se considera como muy baja. Estos muestran altas tasas de FP y un muy bajo valor predictivo. El índice no está validado en su diseño ni en nuestro contexto y además, se tiene gran incertidumbre sobre el valor que otorgarían los padres de los niños asmáticos a la utilización de estos índices. Los índices que precisan extracción sanguínea pueden suponer una menor aceptabilidad por parte de los padres de los pacientes. Herramientas nuevas 2 y 3: Basadas en frecuencia de sibilancias- Se trata también de herramientas no validadas en su diseño, que aún no mostrando mejorías importantes respecto al IPA son herramientas muy sencillas basados en la frecuencia de sibilancias. Su utilización implicaría un menor uso de recursos y costes por tratarse de reglas predictivas muy sencillas de realizar con datos disponibles en el lugar de la aplicación (tanto en cribado como en consulta), aunque, en el caso del índice propuesto por Leonardi, con mayores resultados falsos que con el índice IPA lo que podría llevar a un consumo mayor de recursos por consultas médicas por asma mal controlada.
Recomendaciones
|
Débil
|
Se sugiere no utilizar los índices de predicción clínica de asma en niños menores de tres años con sibilancias para valorar la posibilidad de que éstos presenten asma en la edad escolar (6-13 años), debido a que aún no se dispone de herramientas validadas. |
5.2. Medición de la Fracción exhalada de Óxido Nítrico
Preguntas para responder:
- ¿La medición de la FeNO en niños menores de cinco años con sibilancias ayuda a predecir la presencia de asma en edad escolar?
Las sibilancias son un signo muy común que afectan al 30% de los preescolares. Estos síntomas pueden deberse a diferentes causas, entre las que se encuentran las infecciones virales y el asma con sus diferentes fenotipos. Estos síntomas sólo persisten en la edad escolar en una pequeña parte de los niños. El principal reto médico está en distinguir qué niños preescolares presentan sibilancias transitorias y cuáles tienen realmente un asma persistente, ya que esto permitiría adecuar el tratamiento anti-inflamatorio de la mejor manera posible. Se han propuesto diferentes índices índices de factores de riesgo epidemiológicos para ayudar a predecir la evolución a asma persistente en niños sibilantes; sin embargo, se trata de índices que presentan una baja sensibilidad y especifidad. Por ello, se piensa que añadir medidas objetivas, como el nivel de la FeNO (Fracción exhalada de óxido nítrico) a los algoritmos de predicción de asma puede mejorar la identificación de estos niños.
Evidencia científica
la guía SIGN (45) no hace ninguna recomendación en relación a la medición de la FeNO, mientras que la guía GEMA (46) y la guía ATS (American Thoracic Society) (82) sugieren la utilización de la medición de la FeNO para apoyar el diagnóstico de asma en situaciones en las que se requiere de evidencia objetiva.
En la búsqueda de estudios originales se preseleccionaron cinco estudios (83-87), aunque finalmente se seleccionó un único estudio (83). Entre los cuatro artículos excluidos se encuentran dos protocolos (84-85), un estudio transversal (86) y otro artículo en el que se estudiaba la asociación de la medición de la FeNO a los ocho años con fenotipos sibilantes específicos (87). El estudio seleccionado (83) es un estudio longitudinal y prospectivo en el que se analiza el valor añadido de la medición de la FeNO en niños pequeños para predecir asma en la edad escolar, junto con otros factores de riesgo, como la historia maternal de alergia, la presencia de IgE específica, el diagnóstico de eccema o la frecuencia de sibilancias a los cuatro años de edad.
Los autores concluyen que añadir la medición de la FeNO en niños que tienen una probabilidad pretest intermedia o alta de tener sibilancias a los ocho años de edad puede cambiar la probabilidad post-test de forma clínicamente relevante e independiente del nivel de IgE y la historia clínica del niño, y que el OR de
tener sibilancias a los ocho años de edad es de 1,57 (IC95% de 1,10 a 2,23( cuando el nivel de la FeNO es 1,95 veces mayor que el valor de referencia (ver Figura 1).
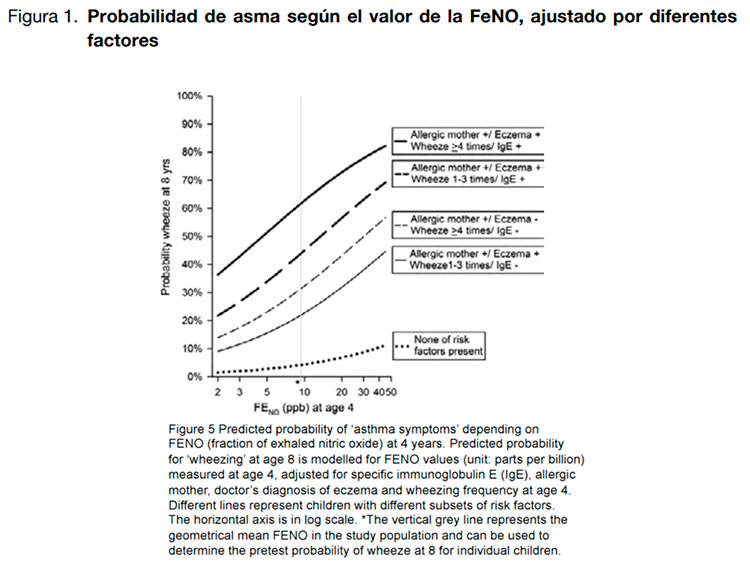
Sin embargo, sólo se consiguieron datos de la FeNO e IgE específica de 185 de los 848 niños incluidos, y los resultados que se presentan derivan de la imputación de datos a través de técnicas estadísticas complejas. En cuanto a la medición de la FeNO, de los 848 niños, 180 no consintieron hacer la prueba, 179 no pudieron realizarla porque no se disponía de un analizador, 140 niños no realizaron la prueba con éxito (miedo, incapacidad para hacerla…), hubo problemas técnicos en 33 casos y en 10 las mediciones fueron de mala calidad, por lo que finalmente sólo se consiguió medir el nivel de la FeNO en 306 de los 848 niños.
Resumen de evidencia
|
Calidad baja
|
La adición de la medición FeNO en niños con probabilidad pretest intermedia-alta de tener sibilancias a los ocho años de edad puede cambiar la probabilidad post-test de forma clínicamente relevante y de forma independiente del nivel de IgE y la historia clínica del niño (83). |
De la Evidencia a la recomendación
Los aspectos que han determinado la fuerza y la dirección de esta recomendación han sido los siguientes:
- La calidad global de la evidencia es baja.Añadir la FeNO en niños con una p pretest intermedia-alta de tener sibilancias a los 8 años de edad puede cambiar la probabilidad post-test de forma clínicamente relevante e independiente a la IgE y a la historia clínica del niño. El OR de tener sibilancias a los 8 años de edad es de 1,57 (IC95% de 1,10 a 2,23) cuando el nivel de la FeNO es 1,95 veces mayor que el valor de referencia.
- El balance entre beneficios y riesgos: Los beneficios y riesgos/inconvenientes están equilibrados.No se ha validado un índice predictivo que incluya la medición de la FeNO. Además, se señala en el estudio que la FeNO sólo se pudo medir en 306 de los 848 niños.
- Valores y preferencias de pacientes y/o sus ciudadores: Probable incertidumbre y variabilidad en la opinión sobre los desenlaces.No se ha podido extraer información del grupo focal realizado. En principio se trata de una prueba fácil de realizar, aunque se necesita que los niños sean colaboradores, algo más difícil de conseguir en este grupo de edad.
- Costes y uso de recursos: los costes son altos en relación a los beneficios.Se trata de una prueba cara de realizar. Las unidades especializadas ya cuentan con equipos para medir el FeNO. No se considera necesario la implantación en Atención Primaria (AP).Por lo tanto, dado que no se ha validado un índice predictivo que incluya esta prueba así como las dificultades técnicas que conlleva, el precio y la falta de suficiente evidencia para apoyar su papel en el diagnóstico de asma en el niño, no consideramos adecuado su generalización, quedando de momento para estudios de investigación y áreas especializadas. Además, determinar FeNO en niños preescolares es muy complicado y solo se puede realizar en centros de referencia, por lo que a día de hoy no se puede utilizar en niños preescolares de forma rutinaria.
Recomendaciones
|
Fuerte
|
Se recomienda no utilizar de forma generalizada la medición de la FeNO en niños menores de cinco años para apoyar el diagnóstico de asma. |
|
√
|
Se sugiere que la medición de la FeNO se puede utilizar en niños menores de cinco años en el contexto de investigación. |
21. Grupo de Trabajo de la Guía de Práctica Clínica sobre Asma. Guía de Práctica Clínica sobre Asma. 2005. Disponible en: http://www9.euskadi.net/sanidad/osteba/datos/gpc_05-1.pdf.
45. Zhang X, Norris SL, Chowdhury FM, et al. The Effects of Interventions on Health-Related Quality of Life Among Persons With Diabetes A Systematic Review. Med Care 2007;45: 820-34.
46. Murphy HR, Wadham C, Rayman G, Skinner TC. Approaches to integrating paediatric diabetes care and structured education: experiences from the Families, Adolescents, and Children’s Teamwork Study (FACTS). Diabet Med 2007;24:1261-8.
71. Castro-Rodriguez JA, Holberg CJ, Wright AL, Martinez FD. A clinical index to define risk of asthma in young children with recurrent wheezing. Am J Respir Crit Care Med. 2000;162(4 Pt 1):1403-6.
72. Caudri D, Wijga A, CM AS, Hoekstra M, Postma DS, Koppelman GH, et al. Predicting the long-term prognosis of children with symptoms suggestive of asthma at preschool age. J Allergy Clin Immunol. 2009;124(5):903-10.e1-7.
73. Kurukulaaratchy RJ, Matthews S, Holgate ST, Arshad SH. Predicting persistent disease among children who wheeze during early life. Eur Respir J. 2003;22(5):767-71.
74. McGinn T WP, Wisnivesky J, Devereaux PJ, Stiell I, Richardson S, Guyatt G. Clinical prediction rules. In: Guyatt G, Rennie D, Meade MO, Cook DJ, eds Users’ Guides to the Medical Literature: A Manual for Evidence-Based Clinical Practice2008
75. Coronel-Carvajal C. Predicción del futuro de un niño con sibilancias. Rev Mex Pediatr. 2010;77(3):2.
76. Leonardi NA, Spycher BD, Strippoli MP, Frey U, Silverman M, Kuehni CE. Validation of the Asthma Predictive Index and comparison with simpler clinical prediction rules. J Allergy Clin Immunol. 2011;127(6):1466-72.e6.
77. Rodriguez-Martinez CE, Sossa-Briceno MP, Castro-Rodriguez JA. Discriminative properties of two predictive indices for asthma diagnosis in a sample of preschoolers with recurrent wheezing. Pediatr Pulmonol. 2011;46(12):1175-81.
78. Devulapalli CS, Carlsen KC, Haland G, Munthe-Kaas MC, Pettersen M, Mowinckel P, et al. Severity of obstructive airways disease by age 2 years predicts asthma at 10 years of age. Thorax. 2008;63(1):8-13.
79. Vial Dupuy A, Amat F, Pereira B, Labbe A, Just J. A simple tool to identify infants at high risk of mild to severe childhood asthma: the persistent asthma predictive score. J Asthma. 2011;48(10):1015-21.
80. Matricardi PM, Illi S, Gruber C, Keil T, Nickel R, Wahn U, et al. Wheezing in childhood: incidence, longitudinal patterns and factors predicting persistence. Eur Respir J. 2008;32(3):585-92.
81. Matricardi PM, Illi S, Keil T, Wagner P, Wahn U, Lau S. Predicting persistence of wheezing: one algorithm does not fit all. Eur Respir J. 352010. p. 701-3.
82. Dweik RA, Boggs PB, Erzurum SC, Irvin CG, Leigh MW, Lundberg JO, et al. An official ATS clinical practice guideline: interpretation of exhaled nitric oxide levels (FENO) for clinical applications. Am J Respir Crit Care Med. 2011;184(5):602-15.
83. Caudri D, Wijga AH, Hoekstra MO, Kerkhof M, Koppelman GH, Brunekreef B, et al. Prediction of asthma in symptomatic preschool children using exhaled nitric oxide, Rint and specific IgE. Thorax. 2010;65(9):801-7.
84. van de Kant KD, Klaassen EM, Jöbsis Q, Nijhuis AJ, van Schayck OC, Dompeling E. Early diagnosis of asthma in young children by using non-invasive biomarkers of airway inflammation and early lung function measurements: study protocol of a case-control study. BMC Public Health. 2009;9:210.
85. van Wonderen KE, van der Mark LB, Mohrs J, Geskus RB, van der Wal WM, van Aalderen WM, et al. Prediction and treatment of asthma in preschool children at risk: study design and baseline data of a prospective cohort study in general practice (ARCADE). BMC Pulm Med. 2009;9:13.
86. Debley JS, Stamey DC, Cochrane ES, Gama KL, Redding GJ. Exhaled nitric oxide, lung function, and exacerbations in wheezy infants and toddlers. J Allergy Clin Immunol. 2010;125(6):1228-34.e13.
87. van der Valk RJ, Caudri D, Savenije O, Koppelman GH, Smit HA, Wijga AH, et al. Childhood wheezing phenotypes and FeNO in atopic children at age 8. Clin Exp Allergy. 2012;42(9):1329-36.











