Preguntas a responder:
- ¿Se debe realizar una radiografía de tórax en todos los pacientes con antecedente de TTCNG que acuden a un centro sanitario?
- ¿Se debe realizar una radiografía de parrilla costal para el diagnóstico de fracturas costales en pacientes con TTCNG?
- ¿Está justificado realizar una radiografía de esternón además de una radiografía de tórax de dos proyecciones en la valoración inicial en pacientes con síntomas y signos de traumatismo esternal?
- ¿Se debe realizar una ecografía torácica en pacientes con antedecente de TTCNG que acuden a un centro sanitario?
- ¿Cuándo es necesario realizar una TC torácica en pacientes con TTCNG?
- ¿Cuándo es deseable realizar un análisis de sangre en pacientes con antecedente de TTCNG?
- En pacientes con TTCNG, ¿se debe pedir un ECG (electrocardiograma) y la medición de enzimas cardíacas?
- ¿Se puede utilizar la pulsioxiometría en vez de la gasometría arterial en pacientes con TTCNG?
5.1. Diagnóstico por imagen
5.1.1. Radiografía de tórax
Preguntas a responder:
- ¿Se debe realizar una radiografía de tórax en todos los pacientes con antecedente de TTCNG que acuden a un centro sanitario?
La radiografía de tórax es un método barato, no invasivo, fácil de obtener y que puede aportar información útil en el traumatismo torácico.
Ocupa un lugar importante en la evaluación inicial del paciente politraumatizado y a menudo es el estudio de imagen inicial en la evaluación del paciente con traumatismo torácico cerrado, complementando la exploración física.
Un porcentaje elevado de las lesiones que amenazan la vida tras un traumatismo torácico cerrado tienen tratamiento específico, pero es necesario un alto grado de sospecha para evitar las complicaciones derivadas del mismo. En más del 80 % de los casos de traumatismo torácico cerrado, éste es leve y sin signos de complicación, por lo cual no se requiere tratamiento hospitalario y podría ser tratado de forma ambulatoria.
La radiografía de tórax posteroanterior (PA) juega un papel fundamental en el diagnóstico de los traumatismos torácicos cerrados. Su indicación no solo es diagnosticar y descartar las lesiones potencialmente graves (hemotórax, neumotórax, contusión pulmonar, fracturas costales y signos indirectos de lesión de grandes vasos), sino que además puede ser útil durante el seguimiento evolutivo de las lesiones.
Evidencia científica
Se ha identificado una guía de la American College of Radiology (ACR) sobre la adecuación de las pruebas de imagen en el diagnóstico de fracturas costales (23), en la que se señalaba que la radiografía de tórax PA era generalmente adecuada para el diagnóstico de fractura costal en pacientes con traumatismo torácico leve cerrado y sospecha de fractura costal (23).
También se identificó una revisión no sistemática general sobre el manejo del paciente con traumatismo torácico cerrado en el servicio de urgencias (24), en la que los autores señalaban que la radiografía de tórax tiene baja S para detectar lesiones torácicas tras un traumatismo torácico cerrado (se pierde un 36 % de los casos cuando se compara con la TC), aunque solo un pequeño porcentaje de estas lesiones era clínicamente significativo. En esta revisión también señalan que la ACR recomienda la radiografía PA como adecuada y complementaria a la TC cuando el mecanismo de lesión es de alta energía (24).
En cuanto a los estudios individuales, se preseleccionaron 12, de los que uno fue excluido por falta de acceso al texto completo (25).
De los 11 estudios preseleccionados, cinco trataban sobre la publicación de dos reglas de predicción para evitar la realización de radiografía en pacientes con traumatismo torácico cerrado (26-30). Los seis estudios trataban sobre la utilidad del juicio clínico o de la presencia de signos y síntomas específicos para saber en qué pacientes se podía descartar la realización de una radiografía de forma segura (31-36).
Además de estos 11 artículos, también se incluyó un estudio individual identificado en la elaboración de otra pregunta de la guía (37), así como el artículo sobre la derivación de una de las reglas de predicción (38) identificado de forma manual.
Las dos reglas de predicción clínica identificadas son la herramienta NEXUS-Chest (26-29) y TIRC (30;38), modelos que incluyen poblaciones más amplias que la definida para esta guía (pacientes con traumatismo debido a mecanismos de alta energía o con traumatismo múltiple).
El NEXUS Chest se elaboró en EE.UU. e incluye los siguientes siete criterios:
- Presencia de dolor torácico.
- Dolor/sensibilidad a la palpación.
- Presencia de lesión distractora.
- Intoxicación.
- Mayor de 60 años.
- Estado mental alterado.
- Mecanismo rápido de deceleración.
Cuando no se cumple ninguno de estos criterios, la regla permite descartar con suficiente seguridad la presencia de lesión intratorácica significativa (SITI en inglés) en pacientes con traumatismo torácico cerrado (S y E del 99,3 % (IC95 % de 97,4 a 99,8) y 14,0 % (IC95 % de 12,6 a 15,4), respectivamente). En el estudio de validación (28), la S y E para descartar SITI leve o grave fueron del 99,0 % (IC95 % de 98,2 a 99,4) y 16,3 % (IC95 % de 15,6 a 17,1), respectivamente.
Teniendo en cuenta los datos del estudio de validación, si se aplicara la regla NEXUS Chest a 1000 pacientes con traumatismo torácico entre los que hubiera 145 casos de lesión intratorácica significativa, se diagnosticarían 144 de estos casos (VP), lo que supone que sólo se habría perdido uno de los casos (un solo FN)).
En cuanto a los FP, en 1000 pacientes habría 741, mientras que los VN serían 114.
Calidad
moderada
para todos
los desenlaces
La S de los criterios individuales de la regla NEXUS Chest para detectar SITI o cualquier tipo de lesión se sitúa entre el 15 % y 56 % y el 14 % y 53 %, respectivamente (29). Por ello, la realización de una radiografía cuando se presenta uno o más criterios dependerá del criterio clínico y de la opinión del paciente.
El otro modelo identificado (TIRC) fue desarrollado en Irán, e incluía los siguientes criterios:
- Mayor de 60 años.
- Crepitación.
- Pérdida de conciencia.
- Disminución de ruidos pulmonares.
- Dolor en la pared torácica.
- Sensibilidad a la palpación.
- Disnea.
- Abrasión.
Para su validación se incluyeron 1.518 pacientes conscientes y hemodinámicamente estables. La presencia de al menos uno de los criterios detecta lesión torácica con una S y E del 100 % (IC95 % de 87 a 100) y del 80,1 % (IC95 % de 78,0 a 82,1), respectivamente.
Además de estos dos modelos, se han identificado seis estudios individuales que valoran la precisión diagnóstica del juicio clínico para detectar una posible lesión intratorácica (31-33;36), así como los signos y síntomas que pueden ayudar a descartar la presencia de fractura costal y de complicaciones (35;37).
Dubinsky y Low (35) evalúan los signos y síntomas clínicos que pueden predecir la presencia de fractura costal, encontrando que tras un traumatismo torácico, los síntomas clínicos no son buenos predictores, aunque solo incluyen 69 pacientes con dolor torácico atendidos en urgencias.
El estudio de Nejati et al (37) encuentra que la combinación de dos criterios clínicos (dolor torácico y taquipnea) identifica el 100 % de los pacientes que presentan una radiografía anormal (todos con fracturas costales).
El estudio de Dunlop et al (36), valora la utilidad del juicio clínico (del médico de urgencias) y la presencia de determinados signos y síntomas clínicos para identificar fractura o fractura y complicaciones, encontrando que la S para identificar lesión torácica (fractura o fractura y complicación) es menor al 50 % en todos los casos.
El estudio de Myint et al (31) sobre el rendimiento del juicio clínico de los médicos de urgencias frente a la radiografía de tórax anteroposterior (AP) en la valoración del traumatismo torácico cerrado. En este estudio se incluyen pacientes estables, no intubados, normotensos y sin hipoxia. El juicio clínico tenía una S del 100 % (IC95 % de 66,4 a 100) para detectar cualquier tipo de lesión intratorácica significativa (fractura costal, esternal, dislocación claviculo-esternal, fractura escapular y disociación escapulotorácica, neumotórax, hemotórax, hemoneumotórax, contusión pulmonar y laceración pulmonar) frente a la radiografía de tórax, por lo que concluyen que la mayoría de pacientes que presentan traumatismo torácico cerrado estable no requieren una radiografía de forma rutinaria (31).
Y por último, en el estudio de Paydar et al (32), con 1.008 pacientes con traumatismo cerrado hemodinámicamente estable y examen físico negativo, se señaló que la radiografía portátil AP tiene poco valor.
En un estudio (39), los autores encontraron que la razón principal por la que los médicos de urgencias pedían una radiografía era que esperaban encontrar lesiones, y porque formaba parte de las pruebas estándar a realizar en estos casos. En general, los médicos no esperaban que la radiografía identificara una lesión intratorácica significativa, y cuando éstos estimaban una baja probabilidad de lesión, la tasa real también solía serlo.
Los dos estudios siguientes incluyeron tanto pacientes con traumatismo torácico cerrado como penetrante, aunque presentaban los resultados por separado. El primero (33) pretendía determinar si existía correlación entre los síntomas y el juicio clínico del traumatólogo sobre la necesidad de realizar una radiografía. Se trataba de un estudio prospectivo con datos de 772 pacientes (86 % con traumatismo cerrado). El valor predictivo negativo (VPN) de la opinión del traumatólogo de que la radiografía sería normal era mayor que el de cualquier otro indicador clínico (VPN de 98,2 %; IC95 % de 96,08 a 99,33). El VPN de la opinión del traumatólogo junto con otros criterios clínicos era del 98,4 % (IC95 % de 95,81 a 99,55). Los autores señalaron que así se habrían evitado el 49,9 % de las radiografías (con respecto a los 772 pacientes), lo que habría supuesto un ahorro de unos 100.078 dólares. En pacientes mayores de 16 años, con un GCS (Escala de Coma de Glasgow) mayor o igual que 13 y no intubados, los VPN serían del 97,81 % y 98,10 %, respectivamente.
En el estudio prospectivo de Bokhari et al (34) sobre la precisión del examen físico en el diagnóstico de hemoneumotórax, entre los 523 pacientes con traumatismo cerrado hemodinámicamente estable, se detectaron siete hemoneumotorax (1,3 %). El VPN de la auscultación, el dolor o sensibilidad a la palpación y la taquipnea fue del 100 %, del 99,3 % y del 99,2 %, respectivamente.
A continuación, se resumen resultados sobre el uso del juicio clínico frente a la radiografía para descartar lesión torácica.
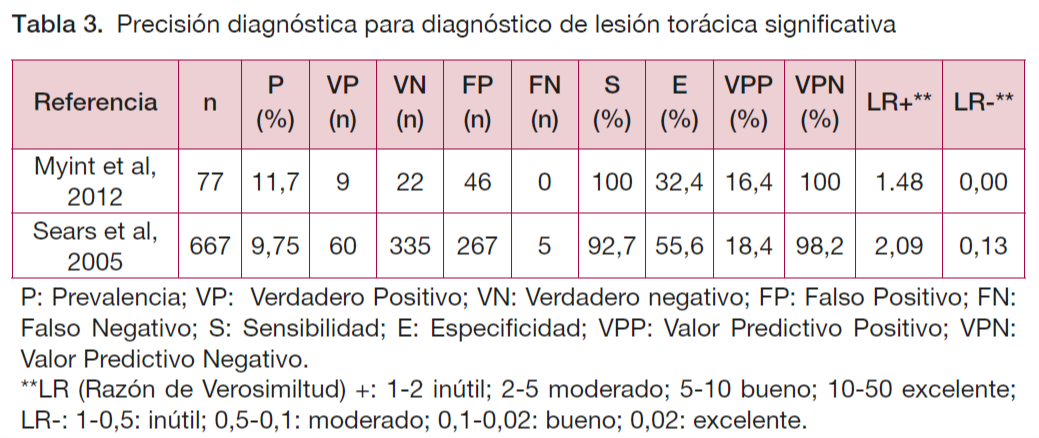
Diagnóstico de lesión torácica significativa
Si se aplicara el juicio clínico para descartar lesión torácica significativa en 1.000 pacientes, y teniendo en cuenta que habría 107 casos, se habrían identificado casi todos los casos (101 casos de 107), por lo que habría 101 VP y 6 casos diagnosticados como FN. Por otro lado, se habrían clasificado 417 pacientes como FP, siendo 476 los VN.
Calidad
moderada/
baja
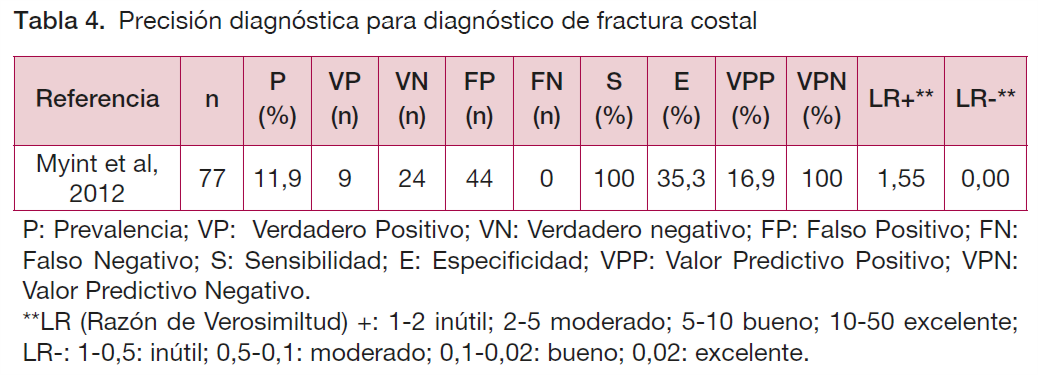
Diagnóstico de fractura costal
Si se aplicara el juicio clínico para descartar fractura costal en 1.000 pacientes, se habrían detectado todos los casos; es decir, no habría FN, y los VP serían 119. Por otro lado, se contaría con 596 FP, que en realidad no tendrían fractura costal.
Calidad
baja para
todos los
desenlaces
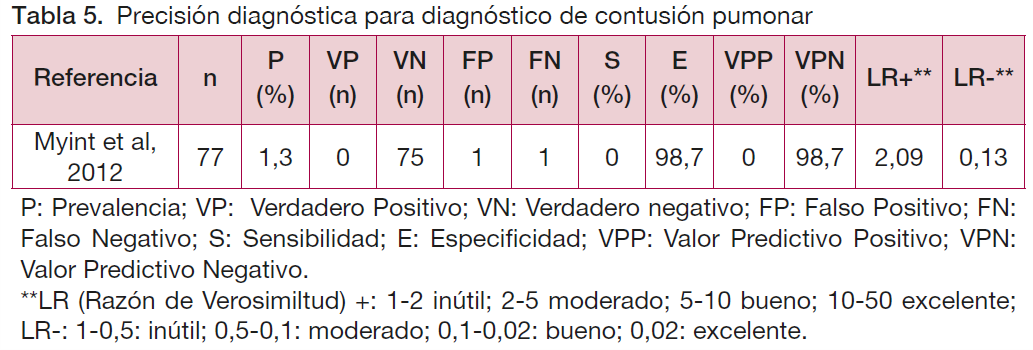
Diagnóstico de contusión pulmonar
En el caso de la contusión pulmonar, al aplicar el juicio clínico se habrían perdido todos los casos, es decir, todos habrían sido clasificados como FN (13 de 1.000). No habría VP. En cuanto a los FP, sólo habría 13 de cada 1.000 pacientes valorados.
Calidad
baja para
todos los
desenlaces
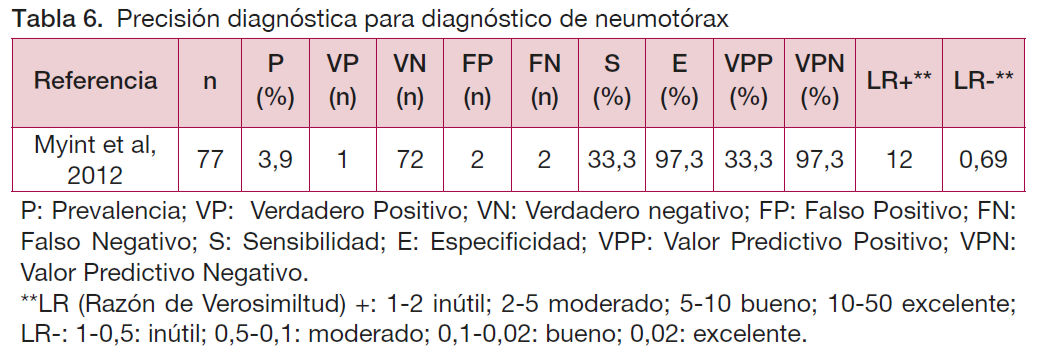
Diagnóstico de neumotórax
En cuanto al diagnóstico de neumotórax, si se aplicara el juicio clínico en 1.000 pacientes, se perderían 26 de los 39 casos, por lo que los FN serían 26 y los VP 13. En cuanto a FP, solo habría 26 en 1.000 pacientes valorados.
Calidad
baja para
todos los
desenlaces
Diagnóstico de hemoneumotórax
En el caso de hemoneumotórax, se detectarían todos los casos. Si se tratara de una muestra de 1.000 pacientes, no habría ningún FN y los VP serían 10. Por otro lado, habría pocos FP (2 en 1.000 pacientes).
Calidad
baja para
todos los
desenlaces
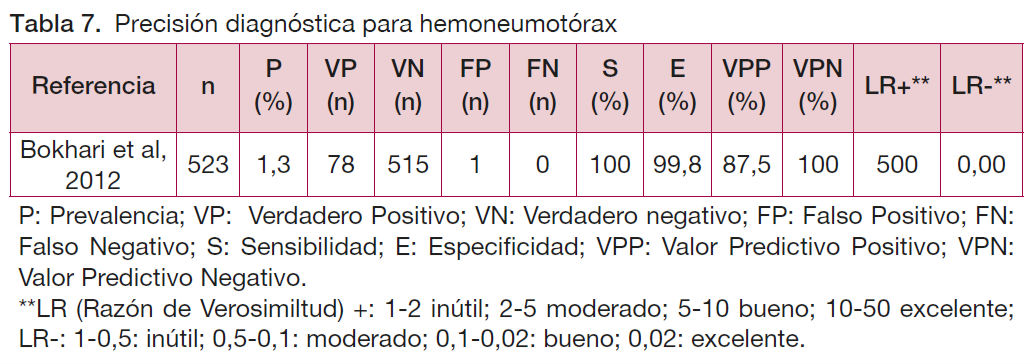
Resultados de la actualización de la búsqueda
En la actualización realizada entre enero de 2017 y enero de 2018, se identificaron 45 referencias, aunque ninguna fue de interés.
En la actualización realizada hasta junio de 2019, se identificó la actualización de la guía de la ACR (40), aunque la recomendación con respecto al uso apropiado de la radiografía PA seguía siendo la misma, por lo que no cambiaría lo discutido anteriormente.
Resumen de la evidencia
| Moderada | La regla NEXUS Chest (que incluye los criterios de presencia de dolor torácico, dolor o sensibilidad a la palpación, presencia de lesión distractora, intoxicación, edad mayor de 60 años, estado mental alterado y mecanismo rápido de deceleración) es capaz de descartar lesión torácica clínicamente significativa evitando la realización de radiografías innecesarias en pacientes con TTCNG (26-29). |
| Baja | El juicio clínico es suficientemente sensible para descartar lesión intratorácia significativa, aunque en los casos de neumotórax y contusión pulmonar la sensibilidad es más baja y no se detectarían todos los casos (31-33;35-37). |
De la evidencia a la recomendación
Los aspectos que han determinado la fuerza y dirección de las recomendaciones han sido los siguientes:
- Calidad global de la evidencia: la confianza en la evidencia sobre el uso de la regla NEXUS-Chest para no realizar radiografías rutinarias es moderada y la confianza en la evidencia sobre el uso del juicio clínico frente a la radiografía rutinaria es baja.
- Balance entre beneficios y riesgos: el balance de los efectos deseados y no deseados probablemente no favorecen la realización de radiografías rutinarias en estos pacientes.
- Utilización de recursos: si se realizaran radiografías de forma rutinaria, se aumentaría la realización de pruebas innecesarias, aumentando el gasto y el número de derivaciones.
- Equidad: las desigualdades en salud probablemente disminuirían.
- Aceptabilidad: la realización de radiografías de forma rutinaria probablemente es aceptable por los agentes implicados. Se trata de una técnica con un uso establecido en este tipo de pacientes. Además, los pacientes pueden demandar la realización de la prueba. Por otro lado, las embarazadas pueden no querer hacerse una radiografía.
- Factibilidad: la implementación de la opción probablemente sea factible.
La radiografía de tórax PA es un método de imagen rápido y sencillo, que nos da información importante de las posibles lesiones derivadas de un traumatismo torácico cerrado y complementa la información aportada por la exploración física. A pesar de que la radiografía de tórax sigue siendo obligatoria en la evaluación primaria de la atención al paciente politraumatizado (protocolo ATLS), en esta guía puede haber un porcentaje de pacientes en los que su realización no esté indicada.
La radiografía de tórax PA es adecuada para el diagnóstico de sospecha de fracturas costales en paciente con traumatismo torácico cerrado leve, aunque éstas solo se visualizan en el 40-50 % de los casos. Aunque el hallazgo de fracturas costales aisladas no va a modificar el tratamiento final (analgesia), la radiografía de tórax PA estaría indicada en pacientes con multimorbilidad que puedan asociar complicaciones tras el traumatismo.
La mayoría de los pacientes jóvenes que presentan un TTCNG, sin deterioro hemodinámico y sin afectación respiratoria (disnea, hipoxia) no requieren una radiografía de tórax de forma rutinaria.
Las lesiones que se pueden producir tras un traumatismo torácico cerrado son variadas, pero solo un pequeño porcentaje de ellas son clínicamente significativas, y aunque la radiografía PA tiene baja S para detectar lesiones potencialmente graves, se considera una prueba de imagen inicial adecuada.
Así, las recomendaciones que se han formulado han sido las siguientes:
Recomendaciones
| Fuerte | Se recomienda no realizar una radiografía de tórax posteroanterior y lateral de manera rutinaria a los pacientes jóvenes con TTCNG. |
| Fuerte | Se recomienda realizar una radiografía de tórax posteroanterior y lateral en aquellos pacientes con TTCNG, si son mayores de 60 años, pudieran estar intoxicados o presentar dolor torácico espontáneo o a la palpación en el momento de la consulta. |
| √ | En pacientes con TTCNG y sospecha de osteoporosis, patología respiratoria, cifoescoliosis, uso de antiagregantes o anticoagulantes, considerar la realización de una radiografía de tórax posteroanterior y lateral de forma rutinaria. |
Consideraciones para la implementación
- El paciente debe ser valorado clínicamente antes de pedir una radiografía.
- Siempre que sea posible se debe realizar una radiografía PA y lateral. En los que no sea factible, se considerará la proyección AP.
5.1.2. Radiografía de parrilla costal
- ¿Se debe realizar una radiografía de parrilla costal para el diagnóstico de fracturas costales en pacientes con TTCNG?
La parrilla costal es una proyección radiológica que, clásicamente, se ha realizado de manera rutinaria conjuntamente con la radiografía PA de tórax en el paciente tipo de esta guía.
Su indicación va dirigida a detectar con mayor S el número, características y localización de las fracturas costales. Requiere ser realizada por personal y equipo adecuado e interpretada por un médico con experiencia y entrenado en valorar esta proyección dada la variabilidad interobservador.
En función de los resultados, se decidirá realizar más pruebas complementarias (TC) o la actitud a seguir (ingreso, colocación de drenaje torácico vs alta hospitalaria).
El objetivo de la búsqueda de la evidencia disponible, es elaborar una recomendación sobre la realización o no de esta proyección en función de si resulta una proyección superior a la radiografía PA y lateral de tórax en cuanto a la S de detección de fractura costal y diagnóstico de complicaciones.
Evidencia científica
Se han identificado ocho estudios relevantes: una guía de la ACR sobre las pruebas adecuadas para valorar pacientes con fractura costal (23), una revisión (24) y seis estudios individuales (41-46).
La ACR señala que puede ser adecuada la realización de radiografías de parrilla costal en pacientes con traumatismo torácico leve (23) (5 puntos de 9). De hecho, en la revisión señalaban que la obtención de radiografías de parrilla costal podía aumentar la S de la radiografía convencional para identificar fracturas costales (24).
En uno de los seis estudios individuales se valoró el impacto del uso de la radiografía de parrilla costal en el manejo del paciente, así como la precisión del médico de urgencias en la interpretación de la radiografía frente al radiólogo (46). El resto de los estudios evaluaban la utilidad de la radiografía de parrilla costal para identificar lesiones costales y complicaciones (41-43;45), aunque tres de ellos también describían el impacto del diagnóstico de fractura costal, tanto en el tratamiento del paciente (41;43) como en su ingreso hospitalario (42).
Solo uno de los seis estudios individuales era prospectivo (41). Cuatro de los estudios comparan la identificación de fractura costal y de complicaciones por la radiografía de parrilla costal frente a la radiografía PA (41;42;44;45), y uno de ellos compara los resultados de ambas técnicas con los de la TC como gold estándar (43).
Los resultados de estos estudios se describen a continuación.
Comparación 1: Radiografía PA frente a Radiografía parrilla costal
Diagnóstico de fratura costal (Radiografía PA vs Radiogafía de parrilla costal)
Si la prevalencia de la fractura costal es de 15,13 % y se aplicaran las pruebas en 1.000 pacientes, habría 152 casos de los cuales 31 no habrían sido diagnosticados con la radiografía PA (serían FN).
Todos los que no tienen fractura costal habrían sido diagnosticados como VN (n=849), no habiendo ningún FP.
Calidad
baja para
todos los
desenlaces
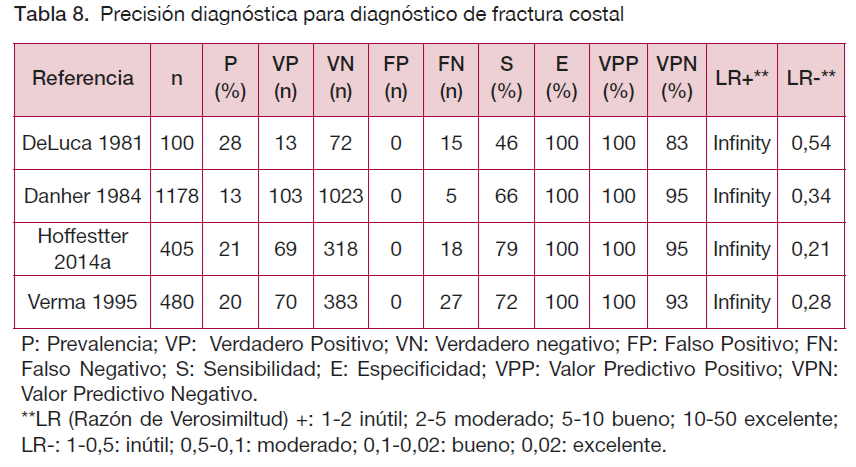
Diagnóstico de complicaciones (Radiografía de parrila costal vs Radiografía PA)
De 1.000 pacientes en los que se habrían realizado las dos pruebas, habría 36 pacientes con complicaciones (prevalencia del 3,63 %), de los cuales 27 habrían sido FN con la radiografía de parrilla costal.
Todos los pacientes sin complicaciones habrían sido diagnosticados correctamente como VN (n=964), por lo que no habría habido FP.
Calidad
moderada
todos los
desenlaces
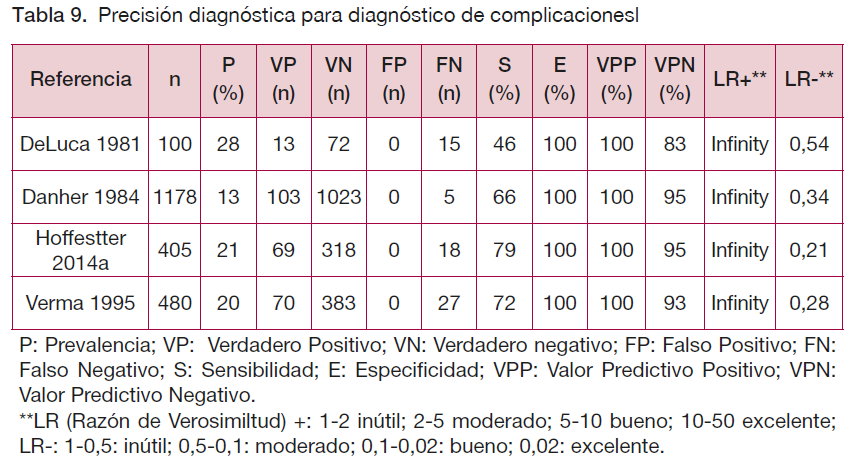
Impacto en el tratamiento del paciente
No se han encontrado diferencias significativas en el tratamiento de pacientes diagnosticados con fractura costal frente a los que no tienen fractura costal (41;43;46), por lo que la realización de dicha prueba no implica cambios en el manejo del paciente.
Calidad
baja
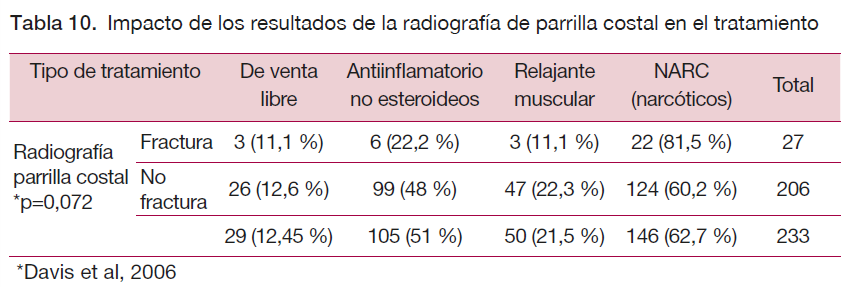

En el estudio De Luca et al (41), el tratamiento sintomático (alivio del dolor) no difiere de forma significativa entre los pacientes con o sin fractura costal (no proporcionan más datos).
De las 155 fracturas costales diagnosticadas en el estudio de Danher et al (42), 52 fueron vistas sólo por la radiografía de parrilla costal (35,5 %). De los 155 pacientes fueron ingresados 44 (28,4 %) (17 en relación con la fractura costal, aunque 15 de ellos con complicaciones asociadas visibles en radiografía de tórax) y 27 por otras lesiones del traumatismo. Los autores señalan que la radiografía de parrilla costal cambia el manejo de 2 de los 1178 pacientes. Sin embargo, uno de estos pacientes era obeso, y el otro un paciente anciano con cinco fracturas costales vistas solo en la radiografía oblicua e ingresado siguiendo la política del centro (ingresar a todo aquel con cuatro o más fracturas costales), sin mayores implicaciones clínicas.
Comparación 2: Radiografía de parrilla costal vs.TC
La radiografía de parrilla costal tiene una S del 82 % para detectar fractura costal frente a la TC, y una S para detectar el número correcto de fracturas costales del 73 %, aunque no se señala el impacto de estos resultados sobre el tratamiento de las fracturas costales identificadas.
Diagnóstico de fractura costal
Si aplicáramos ambas pruebas (radiografía de parrilla costal y TC) en 1000 pacientes, y teniendo en cuenta que habría 392 pacientes con fractura costal, la radiografía de parrilla costal identificaría 321 casos de fractura costal (VP), perdiéndose el diagnóstico en 71 pacientes (FN de la prueba).
Sin embargo, los pacientes sin fractura serían todos correctamente diagnosticados, no habiendo FP.
Calidad
baja para
todos los
desenlaces
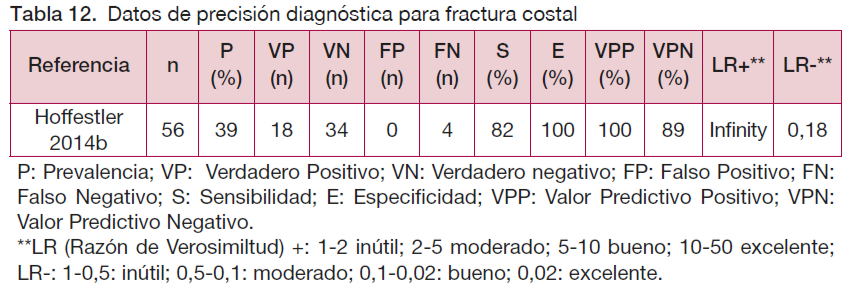
Diagnóstico del nº correcto de fracturas costales
En el caso del diagnóstico del número correcto de fracturas costales, la S de la radiografía de parrilla costal frente a la TC fue del 73 %, por lo que de 56 pacientes a los que se les realizaron ambas pruebas, hubo seis pacientes que presentaban más fracturas costales mediante la TC (FN). Por otro lado, en ningún caso la radiografía de parrilla costal diagnosticaba más fracturas costales que la TC (no hubo FP).
Calidad
baja para
todos los
desenlaces
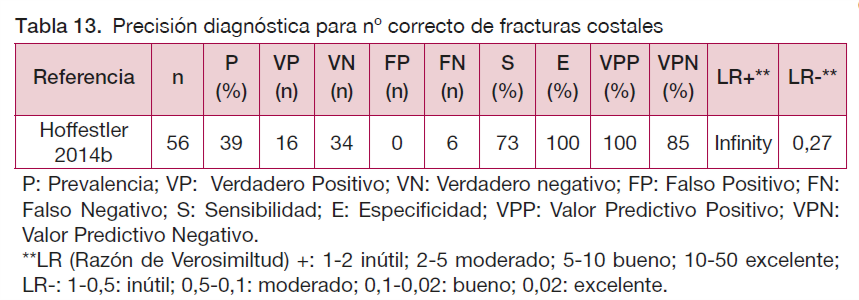
Complicaciones
En este estudio sólo dos de los pacientes con fractura costal presentaron neumotórax, luego había pocos datos para ver las complicaciones (43).
Calidad
baja
Impacto en el tratamiento
No se han encontrado estudios que midan el impacto en el tratamiento de realizar radiografía de parrilla costal frente a la TC.
No hay
estudios
Comparación 3: Radiografía PA vs TC
El único estudio identificado señala que la S para diagnosticar fracturas costales de la radiografía PA frente a la TC es del 47 %, aunque no se proporcionan datos sobre el diagnóstico de complicaciones y del impacto en el manejo del paciente.
Calidad
baja
Resultados de la actualización de las búsquedas
En la actualización realizada entre enero de 2017 y enero de 2018 no se identificaron nuevos estudios relevantes.
En la actualización realizada hasta junio de 2019, se identifican dos estudios. El primero (47) evalúa las características diagnósticas de la radiografía de parrilla costal y de la TC, aunque no está claro cuál es la prueba de referencia con la que se comparan los resultados, por lo que este estudio no se tiene en cuenta. El segundo estudio (48), realizó un cuestionario para valorar las razones que podían influir en la petición de una radiografía de parrilla costal en la valoración inicial del traumatismo torácico leve, observando que las principales razones eran de tipo médico-legales.
Resumen de la evidencia
| Calidad baja | La radiografía PA tiene menor S que la radiografía de parrilla costal para detectar fractura costal, pero mejor S para detectar complicaciones. Sin embargo, no parece que haya diferencias en el tratamiento sintomático del dolor ni en el número de ingresos entre los pacientes que presentan y no presentan fractura costal (41;42;44;45). |
| Calidad baja | La radiografía de parrilla costal tiene una S menor que la TC para el diagnóstico de fractura costal (43). |
| Calidad baja | La radiografía PA es menos sensible que la TC en el diagnóstico de fracturas costales (43). |
De la evidencia científica a la recomendación
Los aspectos que han determinado la fuerza y dirección de las recomendaciones han sido los siguientes:
- Calidad global de la evidencia: la calidad es baja para todas las comparaciones.
- Balance entre beneficios y riesgos: el balance entre los efectos deseados y no deseados probablemente no favorezcan la opción (hacer radiografía de parrilla costal frente a no hacer).
- Utilización de recursos: la realización rutinaria de la radiografía de parrilla costal supone un gasto adicional innecesario, puesto que no está claro si tiene un beneficio adicional.
- Equidad: las desigualdades en salud probablemente aumentarían.
- Aceptabilidad: la aceptabilidad de la opción es incierta.
- Factibilidad: la opción (realización rutinaria de radiografía de parrilla costal) probablemente no sea factible en todos los centros.
La ACR señala como generalmente no adecuada la realización de radiografías de parrilla costal.
Según la evidencia disponible, no se han encontrado diferencias significativas en el tratamiento entre pacientes con fractura costal diagnosticada mediante radiografía de parrilla costal y sin fractura costal, por lo que la realización de la prueba no implica cambios en el manejo del paciente, en el tratamiento sintomático del dolor ni en el número de ingresos.
La proyección PA y lateral no es adecuada para la valoración de las costillas inferiores, por lo que aun en pacientes con movilidad adecuada a los que se les han podido hacer las proyecciones PA y lateral, si hay sospecha de fractura de costillas bajas, podría ser necesario realizar una radiografía de parrilla costal.
Por otro lado, puede que la situación clínica de determinados pacientes contraindique la posición en bipedestación, por lo que serían pacientes subsidiarios de la proyección de tórax AP. La radiografía de parrilla costal podría ser un complemento a la anterior.
Así, las recomendaciones que se han formulado han sido las siguientes:
Recomendaciones
| Fuerte | Se recomienda no realizar una radiografía de parrilla costal de forma rutinaria en pacientes con TTCNG a los que ya se les haya realizado una radiografía de tórax posteroanterior y lateral. |
| √ | Considerar hacer una radiografía de parrilla costal en pacientes con TTCNG y con sospecha de fractura costal baja. |
| √ | Considerar hacer una radiografía de parrilla costal de forma complementaria a la proyección anteroposterior en pacientes con TTCNG y con problemas de movilidad a los que no se les ha podido realizar una proyección posteroanterior y lateral. |
5.1.3. Radiografía esternal
- ¿Está justificado realizar una radiografía de esternón además de una radiografía de tórax de dos proyecciones en la valoración inicial en pacientes con síntomas y signos de traumatismo esternal?
Clásicamente, se ha considerado la fractura de esternón como consecuencia de un traumatismo de alta energía, lo que no corresponderían al paciente tipo de esta guía.
Pero en pacientes de edad avanzada y/o con osteoporosis, la fractura de esternón se puede producir como consecuencia de traumatismos menores (traumatismo torácico anterior, caídas en domicilio…).
La indicación de la radiografía de esternón va dirigida a detectar con mayor S la fractura de esternón.
Al igual que la proyección de la parrilla costal, requiere ser realizada por personal y equipo adecuado e interpretada por un médico con experiencia y entrenado en valorar esta proyección dada la variabilidad interobservador.
El objetivo de esta pregunta es elaborar una recomendación sobre la realización o no de esta proyección, en función de si resulta superior a la radiografía PA y lateral de tórax en cuanto a la S de detección de fractura esternal.
Evidencia científica
La búsqueda obtuvo 329 referencias, de las que se preseleccionaron seis: la revisión de Morley et al (24) y cinco estudios individuales (49-53). Sin embargo, en la revisión no se realizan recomendaciones sobre la radiografía esternal en el diagnóstico y manejo del paciente con sospecha de fractura esternal y/o costal, y de los cinco estudios individuales preseleccionados se descartan tres: uno por tratarse de un caso (49), otro por valorar la utilidad de la ecografía en detectar fractura esternal sólo en pacientes con radiografía esternal y TC negativas (50) y el tercero por evaluar el valor clínico de las fracturas esternales diagnosticadas sólo por TC (51).
Los dos estudios restantes son series de casos que incluyen pacientes a los que se les había realizado una radiografía lateral para el diagnóstico de fractura esternal, sin que se planteara la necesidad de realizar o no dicha prueba y sin que se evaluara si su realización suponía un cambio en el manejo del paciente (52;53).
No hay
estudios
Por otro lado, se realizó una búsqueda sistemática para determinar si la radiografía lateral era capaz de diagnosticar fractura esternal, puesto que en el caso de que esto fuera cierto, no sería necesario añadir la proyección esternal a las proyecciones PA y lateral. De los 35 estudios identificados se seleccionaron ocho, aunque en cuatro de ellos el objetivo no era valorar la utilidad diagnóstica de la radiografía lateral para la fractura esternal, sino que era la técnica diagnóstica que los autores utilizaban para identificar pacientes con fractura esternal a incluir en el estudio (52;54-56).
Entre los cuatro estudios restantes, uno comparaba la radiografía lateral frente a la TC axial (57), otro frente a la TCMD (58) y dos estudios la radiografía lateral frente a la ecografía esternal (59;60).
El único estudio válido (58) evaluaba de forma retrospectiva 87 pacientes a los que se les había realizado una TCMD entre enero de 2009 y noviembre de 2010 (sección de 5 mm de espesor). En 31 de estos pacientes se les hizo además una radiografía lateral de esternón, utilizando la técnica esternal (65+/- 70 kVp, 200mAs). La fractura esternal se diagnosticó en base a los síntomas clínicos y los resultados de todas las pruebas (TC, radiografía etc) en 20 de los 31 pacientes, siendo la S de la radiografía del 70 % y de la TC del 100 %.
Calidad
muy baja
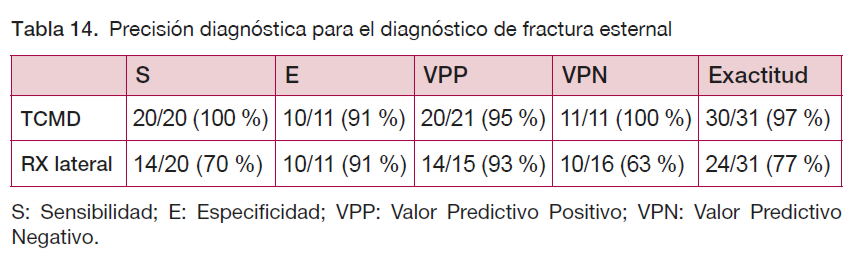
Resultados de la actualización de la búsqueda
En la actualización de la búsqueda no se identificaron referencias de interés.
Resumen de la evidencia
| No hay estudios | No hay estudios que comparen la radiografía esternal frente a la TC, la radiografía PA u otras pruebas de imagen, en el diagnóstico de fractura esternal. |
| Calidad muy baja | La radiografía lateral tiene una S del 70 % para detectar fractura esternal en comparación con la TC (58). |
De la evidencia a la recomendación
Los aspectos que han determinado la fuerza y dirección de las recomendaciones han sido los siguientes:
- Calidad global de la evidencia: no hay estudios que evalúen la capacidad diagnóstica de la radiografía esternal frente a otras pruebas de imagen. La calidad de la evidencia que evalúa la capacidad diagnóstica de la radiografía lateral frente a la TC para el diagnóstico de fractura esternal es muy baja.
- Balance entre beneficios y riesgos: el balance entre los efectos deseados e indeseados es incierto.
- Utilización de recursos: el impacto en el coste de la realización de radiografía esternal rutinaria es incierto.
- Equidad: el impacto en las desigualdades de la opción es incierto.
- Aceptabilidad: la aceptabilidad de la opción es incierta.
- Factibilidad: la factibilidad de la realización rutinaria de radiografía de esternón es incierta.
En los pacientes de nuestra guía la probabilidad de fractura esternal es baja, ya que estas fracturas son un marcador de mecanismo del traumatismo de alta energía. Además, no suelen requerir tratamiento quirúrgico, sólo analgesia y rehabilitación respiratoria. Por otro lado, se considera que la radiografía lateral de tórax es suficiente por sí misma para el diagnóstico de la fractura esternal, de hecho, son muchos los estudios que la utilizan como técnica de diagnóstico para la inclusión de pacientes con fractura esternal. Si la radiografía se realiza con una técnica adecuada permite descartar fracturas esternales desplazadas, que son las que podrían producir los mayores problemas. Si la radiografía detecta fractura esternal, en estos casos habría que realizar una TCMD para descartar lesiones asociadas. Además, la proyección lateral permite diagnosticar la presencia de complicaciones pleuroparenquimatosas.
Como no se han encontrado evidencia para el uso de la radiografía esternal, el grupo ha elaborado una recomendación de tipo consenso en base a su experiencia clínica.
Recomendaciones
| √ | No realizar una radiografía de esternón en los pacientes con TTCNG a los que se les haya realizado previamente una radiografía PA y lateral, aun cuando exista sospecha de fractura esternal. |
| √ | En pacientes con TTCNG en los que por la patología de base presenten una limitación de movilidad que impida colocarse en bipedestación o sedestación, y no sea posible realizar una proyección lateral, se considerará la necesidad de realizar una TC para su diagnóstico. |
5.1.4. Ecografía torácica
- ¿Se debe realizar una ecografía torácica en pacientes con antecedente de TTCNG que acuden a un centro sanitario?
La ecografía es una técnica radiológica inocua, de bajo coste, accesible, portátil, no invasiva y que carece de radiaciones ionizantes, por lo que es ampliamente utilizada como método diagnóstico y es de gran ayuda en la toma de decisiones en la práctica clínica habitual. No obstante, no está exenta de inconvenientes como son la escasa reproductibilidad, a diferencia de otras técnicas radiológicas (radiografía y TC), y la necesidad de capacitación que requiere un tiempo amplio de aprendizaje.
Existen muchos estudios que avalan la utilización de la ecografía en pacientes politraumatizados inestables (ecografía FAST o Ecografía abdominal dedicada al trauma) enfocada al diagnóstico de líquido libre intraperitoneal, pericárdico y pleural.
Nos hemos planteado realizar una revisión sobre si esta técnica de imagen tiene aplicaciones en los pacientes que competen a esta guía, considerando las ventajas e inconvenientes de la misma.
Evidencia científica
En la búsqueda de RS y meta-análisis (MA) sobre el uso de la ecografía en el manejo de traumatismo torácico cerrado, se han seleccionado ocho de las 56 revisiones identificadas. Estas revisiones tratan sobre la utilidad de la ecografía y la radiografía en el diagnóstico de neumotórax (61-64), hemotórax (61;65), contusión pulmonar (66), fractura esternal (67) y fractura costal (68) (esta última en pacientes con traumatismo torácico menor). Por otro lado, está el documento de la ACR sobre los criterios de diagnóstico por imagen apropiados en el traumatismo torácico cerrado (23).
La ACR señala que la ecografía puede ser beneficiosa (5 puntos sobre 9) en el diagnóstico de neumotórax, hemotórax y hemorragia pericárdica en la valoración inicial de pacientes con traumatismo torácico y mecanismo de alta energía. Sin embargo, en pacientes con radiografía AP, examen físico y estado mental normal y mecanismo de no alta energía, la ACR señala que la ecografía no sería generalmente apropiada (1 punto sobre 9). Por otro lado, en pacientes con traumatismo torácico menor y sospecha de fractura costal, la ecografía tampoco sería generalmente apropiada (1 punto de 9) para el diagnóstico de fractura costal (23).
La revisión de Wilkerson y Stone (64) incluye cuatro artículos (69-72) que estudian la ecografía a pie de cama frente a la radiografía AP supina en el diagnóstico de neumotórax tras traumatismo torácico cerrado. La prueba de referencia fue la TC o Rush of air during thoracostomy tube placement. En esta revisión se incluyeron solo estudios prospectivos en los que las ecografías eran realizadas por médicos de la urgencia.
Tanto la revisión de Ebrahimi et al, 2014 (62) como la de Alrajab et al, 2013 (63), tienen en cuenta estudios que incluyen pacientes con neumotórax no solo de origen traumático, sino también de origen iatrogénico, ingresados en Unidad de Cuidados Intensivos (UCI) o con problemas respiratorios.
En cuanto al diagnóstico de hemotórax, hay dos revisiones que incluyen pacientes con traumatismo torácico (61;65). Estas revisiones no seleccionan los estudios en función de qué profesional sanitario realiza la ecografía. En la revisión de Staub (61) no se realiza un análisis de subgrupos para ver el tipo de profesional sanitario que realiza la técnica y si esto influye en la precisión de la prueba.
Los estudios de Racine et al (67) y Lalande et al (68) son informes de Best Evidence Topic (BET), y como tales no son realmente RS, aunque aportan la visión actual de la situación de la ecografía en el diagnóstico de fractura esternal en pacientes con traumatismo torácico cerrado y sospecha de fractura esternal, así como de fractura costal, en este último caso en pacientes con traumatismo torácico menor.
El mayor problema de todas las revisiones identificadas es la alta heterogeneidad encontrada en los datos globales de S y E de la ecografía, así como la alta variabilidad en el diseño de los estudios, la mala calidad y la falta de conocimiento sobre la implicación clínica del diagnóstico, es decir, si se trata de lesiones que implican un cambio o no en el manejo del paciente. Por todo ello, la calidad de la evidencia encontrada será muy baja en todos los casos.
Diagnóstico de neumotórax
Ecografía vs. TC
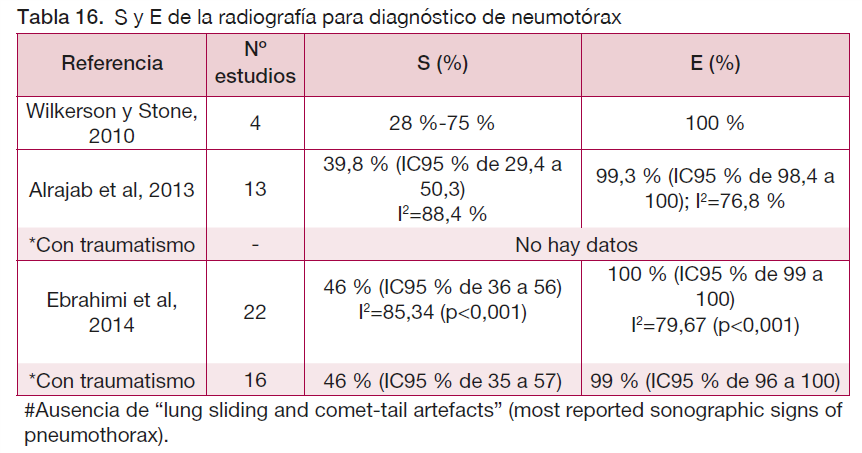
Se han identificado cuatro RS (61-64) que se diferencian en la fecha de publicación, en la exclusión o no de pacientes sin traumatismo y en la inclusión o no de estudios según el profesional sanitario que realiza la prueba. En todos los casos, la ecografía presenta una S entre el 79 y el 87 % y una E entre el 97 y 99 %, respectivamente, frente a la TC, aunque la heterogeneidad es muy alta en todos los casos.
Calidad
muy baja
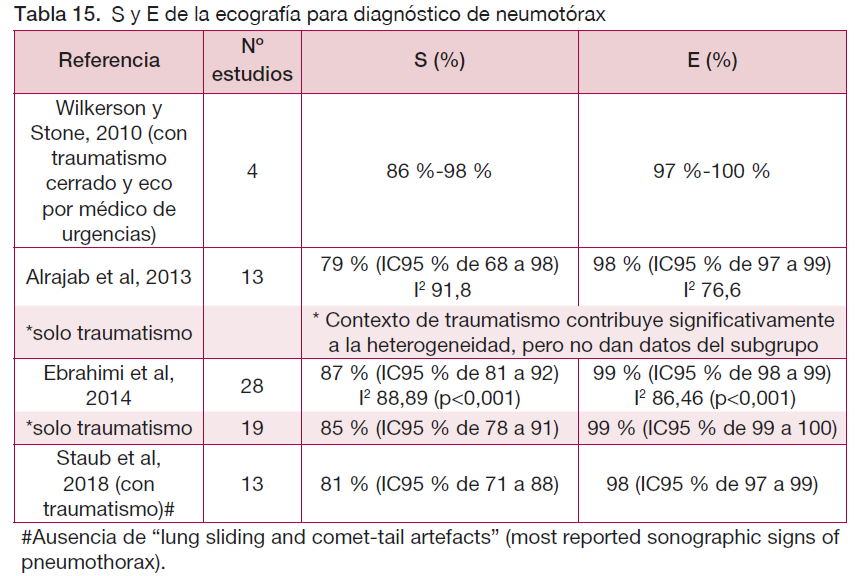
Por otro lado, son tres las revisiones (62-64) que dan datos sobre S y E de la radiografía para el diagnóstico de neumotórax frente a la TC. Suele tratarse de estudios que realizan una radiografía AP, que tiene peores resultados que una radiografía PA en bipedestación. La heterogeneidad entre los estudios también es muy alta (I2 >76 % en todos los casos).
Calidad
muy baja
Diagnóstico de hematórax
En cuanto a las dos revisiones que comparan la S de la ecografía frente a la TC (61;65) para detectar hemotórax, ésta está entre un 60 y 67 %, en comparación a la TC.
Calidad
muy baja

En el caso de la radiografía, en la única revisión identificada (65), la S para detectar hemotórax (frente a la TC) es algo menor que la de la ecografía (S del 54 %).
Calidad
muy baja

Diagnóstico de contusión pulmonar
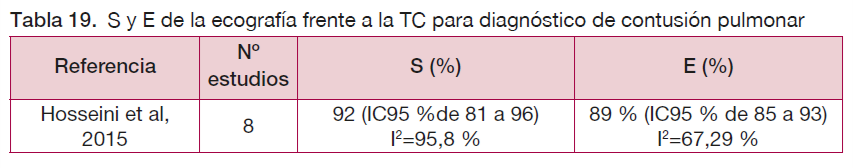
Se ha identificado una revisión de 2015 que estudia la utilidad de la ecografía en pacientes con traumatismo para el diagnóstico de contusión pulmonar (66). La S para la ecografía es del 92 %, mientras que la de la radiografía se sitúa en el 44 %, aunque la heterogeneidad entre estudios sigue siendo muy alta.
Calidad
muy baja

Diagnóstico de fractura esternal
En el BET (67) se señala que puede que la ecografía sea superior a la radiografía en el diagnóstico de fractura esternal, aunque ningún estudio ha valorado claramente la precisión de la ecografía en este contexto.
Los autores identificaron cuatro pequeñas cohortes que favorecen el uso de la ecografía, aunque no hay comparación frente a una prueba de referencia, como la TC o ecografía de seguimiento para demostrar la formación de callo. En la mayoría de los estudios eran los radiólogos los que hacían la prueba, por lo que la aplicación de esta técnica en el contexto de las urgencias estaría disminuida por la validez externa de los resultados.
Diagnóstico de fractura costal en traumatismo torácico menor
En el BET identificado (68), aunque los resultados sugieren que la ecografía es mejor que la radiografía en diagnosticar fractura costal, hacen falta estudios con una prueba de referencia establecida antes de favorecer el uso rutinario de la ecografía.
Resultados actualización de la búsqueda
En la actualización se han identificado cinco nuevas RS sobre el uso de la ecografía (en el diagnóstico urgente del paciente con traumatismo grave), así como la actualización de la guía de la ACR de 2014 (40).
En cuanto a las revisiones, se ha identificado un protocolo de RS Cochrane de 2018 (73) sobre la ecografía frente a la radiografía en posición tumbada para el diagnóstico urgente de neumotórax en pacientes traumatizados, una RS sobre el manejo de la ecografía a pie de cama frente a la TC, resonancia magnética (RM) etc, para el diagnóstico de lesiones toracoabdominales en pacientes tras un traumatismo (74), una RS sobre el uso de la ecografía y radiografía en el diagnóstico de fracturas costales (75) (que llega a conclusiones similares a lo ya descrito anteriormente) y una última revisión sobre el uso de la ecografía en el diagnóstico urgente de neumotórax y hemotórax traumático (61).
En la actualización de la guía de la ACR en pacientes con traumatismo torácico leve se señala que la ecografía torácica sería normalmente no adecuada (40), en la misma línea de lo que se había recogido previamente en la pregunta, por lo que no se producen cambios a lo discutido anteriormente.
Resumen de la evidencia
| Calidad muy baja | La ecografía es superior a la radiografía pero inferior a la TC en el diagnóstico de neumotórax (70;76). En un MA reciente (64) la ecografía presenta una alta S y E (rango de 86 % a 98 % y de 97 % a 100 %, respectivamente), mientras que la radiografía supina muestra una S limitada (rango de 28 % a 75 %) aunque con alta E (100 %). En cuanto al diagnóstico de hemotórax, se señala que la ecografía es igual o más precisa que la radiografía (77;78). |
De la evidencia a la recomendación
Los aspectos que han determinado la fuerza y dirección de las recomendaciones han sido los siguientes:
- Calidad global de la evidencia: La confianza en que la ecografía es mejor que la radiografía o que pueda sustituir a la TC en determinadas situaciones es muy baja.
- Balance entre beneficios y riesgos: el balance entre los efectos deseados y los no deseados es incierto.
- Utilización de recursos: la necesidad de recursos y el aumento de los costes en relación a los beneficios es incierta.
- Equidad: el impacto en las desigualdades es incierto.
- Aceptabilidad: la aceptabilidad de la opción es incierta.
- Factibilidad: la factibilidad de la opción es incierta.
El grupo de trabajo considera que la ecografía en el contexto del TTCNG es una técnica que se está utilizando pero que de momento no es aplicable a los pacientes de la guía, salvo en el contexto de la investigación
| Con la evidencia actualmente disponible, no se puede hacer una recomendación csobre el uso rutinario de la ecografía en pacientes que han sufrido un TTCNG. |
5.1.5. Tomografía computerizada de tórax
- ¿Cuándo es necesario realizar una TC torácica en pacientes con TTCNG?
El traumatismo torácico que compete a esta guía es un motivo de consulta frecuente en los servicios de urgencias. La TC es la técnica de imagen que tiene una mayor S y E para valorar las lesiones que conlleva y sus complicaciones. un así, su uso sistemático no es recomendable. Como contrapartida, el empleo de forma indiscriminada de la TC expone a los pacientes con traumatismos a radiación innecesaria.
Los criterios de utilización de la TC en el traumatismo torácico tienen una alta variabilidad y no existen guías clínico-radiológicas de actuación actualizadas que establezcan indicaciones de cuándo hay que solicitar una TC en este escenario clínico y cuándo se puede obviar de forma segura. Por ello, en muchas ocasiones, se realizan en exceso o los hallazgos encontrados no tienen relevancia clínica al no suponer un cambio en la actitud terapéutica.
Nos planteamos la necesidad de establecer unas pautas basadas en la evidencia y realizar unas recomendaciones de consenso sobre la adecuación de la TC en este contexto clínico.
Evidencia científica
En los criterios de adecuación de la ACR (79) hacen diferentes recomendaciones para pacientes que sufren un traumatismo torácico de alta energía y/o presentan resultados anormales en la radiografía de tórax, así como para los que presentan una radiografía AP normal, examen físico y estado mental normales y/o el mecanismo del traumatismo no ha sido de alta energía. En el último caso, se indica que la TC puede ser apropiada (5 puntos de 9) en algunos casos, y en el primero, que es normalmente útil en todos los casos (8 puntos de 9).
En la búsqueda realizada se identificó una RS (80) sobre los factores de riesgo que predecían en qué pacientes con traumatismo torácico cerrado una TC podía encontrar resultados anormales. Los autores encontraron que: 1) una exploración física anormal (esfuerzo respiratorio anormal, necesidad de ventilación asistida, reducción de la inspiración, coma, dolor a la palpación de la pared torácica) y la existencia de fractura pélvica predicen un resultado anormal en la TC (ORD (Odds Ratio Diagnóstica) de 2,1 a 6,7); 2), que la presencia de cualquier lesión en la radiografía torácica convencional predice un resultado anormal en la TC (ORD de 9,2 a 37) y que 3) la presentación de un resultado anormal en la ecografía torácica es el mejor factor predictor de un resultado anormal en la TC (ORD de 491 a Infinito) (80).
De la búsqueda específica realizada para esta pregunta, se han considerado finalmente 11 estudios.
Reglas de predicción clínica para evitar realizar TC de forma segura
Se han identificado dos reglas de predicción clínica con las que se pretende valorar en qué pacientes con traumatismo torácico cerrado se puede evitar de forma segura la realización de una TC (81-83).
La primera regla se denomina SCRAP (81) y fue desarrollada con los datos de 434 pacientes admitidos en urgencias que: 1) tenían un ISS (Escala de Valoración de la Gravedad) >12, y 2) se les había realizado una TC torácica o presentaban una lesión clínica grave documentada. En este estudio se definió como desenlace final la presencia de lesión torácica grave en la TC (lesión que puede cambiar potencialmente el manejo clínico del paciente, por necesitar una terapia específica o un período de observación hospitalaria). Dicha regla incluía como variables: 1) nivel de saturación de oxígeno menor de 95 % en el aire ambiental, o del 98 % en cualquier suplementación de oxígeno; 2) radiografía torácica anormal; 3) tasa respiratoria menor o igual a 25; 4) auscultación torácica anormal y 5) palpación torácica anormal. La S para descartar lesión torácica grave cuando todos los criterios eran negativos fue del 100 % (IC95 % de 98,4 a 100), la E del 46,9 % (IC95 % de 44,2 a 46,9) y el LR negativo de 0 (IC95 % de 0 a 0,04). En el estudio de validación (180 pacientes), la S para descartar lesión torácica grave fue del 100 % (IC95 % del 96,2 a 100), la E del 44,7 % (IC95 % de 39,5 a 44,7) y el LR negativo de 0 (0 a 0,10).
Los autores señalan que en pacientes con traumatismo torácico grave y traumatismo craneoencefálico leve (GCS mayor que 8), la S de la regla SCRAP para descartar lesión torácica grave era del 100 %, por lo que en pacientes que no cumplían con esos criterios se podría evitar la realización de una TC.
La segunda regla es la del NEXUS Chest CT (82) en sus dos variantes: NEXUS Chest-CT-Major y NEXUS Chest-CT-All. La diferencia entre ambas reside en que la regla NEXUS Chest-Major no incluye el criterio de mecanismo rápido de deceleración. Con la primera regla se pretendía maximizar la S para descartar lesión torácica grave, y con la segunda la de cualquier tipo de lesión torácica.
Para la creación de estas reglas se contó con los datos prospectivos de 11.477 pacientes mayores de 14 años que acudieron a urgencias en el transcurso de las siguientes seis horas tras un traumatismo cerrado y a los que se les había pedido alguna prueba de imagen (Radiografía o TC). Para la derivación de las dos reglas clínicas se incluyeron 6.002 pacientes, y para su validación 5.475.
De los 6.002 pacientes incluidos en la derivación, sólo en 1.873 (31,2 %) casos se habían realizado ambas pruebas. La prevalencia de lesión leve o de cualquier tipo fue del 34,7 % (649 pacientes) y de lesión grave del 7,7 % (144 pacientes).
En el estudio de validación, el 48 % de los pacientes realizaron ambas pruebas diagnósticas, siendo la prevalencia de lesión grave de 4,6 % (120 pacientes) y de cualquier tipo de 26,9 % (706 pacientes).
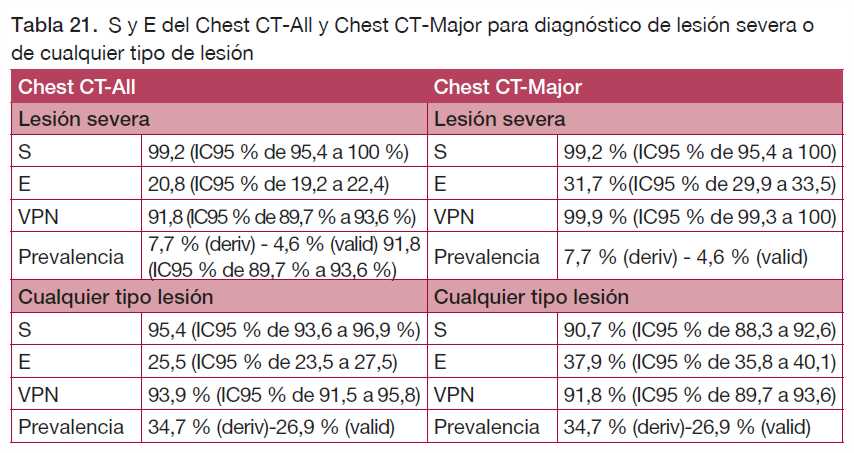
Cuando todos los criterios son negativos, se puede evitar la realización de una TC y descartar la presencia de lesión severa con una S del 99,2 % con ambas reglas (ver tabla 21).
Así, si se aplicara la regla CHEST-CT Major a 1000 pacientes con traumatismo torácico, de los 77 pacientes que presentarían lesión grave clínicamente significativa, 76 (VP) serían diagnosticados correctamente, encontrando un único FN. Por otro lado, el número de FP sería de 630.
En el caso de la regla Chest-CT-All, si ésta se aplicara a 1000 pacientes con traumatismo torácico, de los 347 casos que se encontrarían la regla permitiría diagnosticar 315 (VP), por lo que en este caso el número de FN sería mayor (32 casos por 1.000). En cambio, el número de FP disminuiría, siendo de 405 casos por 1.000.
Calidad
moderada
para todos
los
desenlaces
Según el análisis secundario de los datos obtenidos en los estudios de derivación y validación de la regla NEXUS-Chest-CT (83), cuando se cumple de forma aislada el criterio de presentar una radiografía anormal (tener cualquier lesión torácica (incluyendo la fractura clavicular) o un ensanchamiento mediastínico), la S y E de identificar una lesión clínicamente grave sería del 73,3 % (IC95 % de 68,1 a 78,6 %) y del 83,9 % (IC95 % de 83,6 a 84,2), respectivamente, siendo la prevalencia de presentar cualquier tipo de lesión o de lesión grave en este caso del 60,7 % (IC95 % de 52,2 a 68,6) y del 12,9 % (IC95 % de 8,3 a 19,4), respectivamente.
Si solo se cumpliera un criterio de la regla que no fuera presentar una radiografía anormal, la probabilidad de cualquier lesión o de lesión clínicamente grave sería muy baja (del 16,8 % (IC95 % de 15,2 a 18,6) y del 1,1 % (IC95 % de 0,1 a 1,8), respectivamente). Si se presentaran dos criterios, la prevalencia de cualquier lesión y de lesión grave sería del 25,5 % (IC95 % de 23,1 % a 28,0 %) y del 3,2 % (IC95 % de 2,3 a 4,4), respectivamente, y si se cumplieran tres, serían del 34,9 % (31 %-39 %) y del 2,7 % (1,6 %-4,5 %), respectivamente.
Por lo tanto, cuando la radiografía no es normal se recomienda realizar una TC, y en el caso en el que se cumpla uno o más del resto de los criterios se recomienda discutir entre el médico y el paciente la necesidad de realizar dicha prueba.
Además de las reglas de predicción, se han encontrado siete estudios que valoran lo que aporta realizar una TC en pacientes con traumatismo torácico cerrado. En el primer estudio se analiza la validez del juicio clínico frente a la TC para detectar lesión torácica significativa en pacientes tras un traumatismo cerrado debido a una caída desde una posición sentada o de pie (84). En el segundo, el valor de realizar una TC rutinaria frente a una TC selectiva en pacientes con traumatismo torácico cerrado (85). El tercer estudio compara la precisión de la radiografía frente a la TC a la hora de identificar diferentes tipos de lesiones torácicas (86), el cuarto los factores de riesgo que pueden predecir resultados de TC anormales en pacientes con radiografía normal (87) y los tres restantes la precisión diagnóstica de la TC en el diagnóstico de lesión intratorácica en pacientes con o sin radiografía normal (88-90).
Radiografía de tórax frente a la TC entre pacientes con radiografía normal frente anormal
En referencia a los tres estudios retrospectivos que analizan el valor de realizar una TC según la presencia de resultados anormales o no en la radiografía (88-90), todos concluyen que en pacientes con una radiografía normal el porcentaje de lesión que se identifica es menor que en pacientes que presentan una radiografía anormal, por lo que se recomienda la realización de TC en pacientes que presenten resultados anormales en la radiografía. En todos los casos el mecanismo de lesión fue de alta energía y el ISS de los pacientes era mayor que los contemplados para esta guía.
Morbilidad y mortalidad según el número y localización de fracturas costales identificadas por radiografía
Para el estudio de la asociación entre el número de fracturas costales diagnosticadas mediante radiografía y el riesgo de morbilidad y/o mortalidad de los pacientes con traumatismo torácico cerrado, se identificaron dos revisiones: una RS sobre los factores de riesgo que predicen la aparición de eventos adversos en pacientes mayores con traumatismo torácico cerrado (91) y otra sobre los factores de riesgo que predicen mortalidad en pacientes con traumatismo torácico cerrado (92).
En ambas revisiones, el número de fracturas costales parecía asociarse con una mayor morbilidad y/o mortalidad. En la revisión de Battle et al (92) se encuentra que el número de fracturas costales se asociaba con un mayor riesgo de mortalidad en los pacientes con traumatismo torácico, siendo el OR de 2,02 (IC95 % 1,89 a 2,15) en pacientes con tres o más fracturas costales.
Calidad
baja
Sin embargo, tres de los cuatro estudios incluidos en la revisión no indicaron la prueba utilizada para el diagnóstico del número de fracturas costales (93-95), y solo en el estudio de Lee (96) (poblacional retrospectivo) se señala que el diagnóstico se realizó mediante radiografía inicial.
En la búsqueda de estudios individuales posteriores a la revisión de Battle et al (92) se identificaron 12 estudios (97-108), de los cuales cuatro no señalan la prueba diagnóstica utilizada para cuantificar el número de fracturas costales (97-100), dos estudios utilizaron tanto la radiografía torácica como la TC (107;108), tres utilizaron la TC (101-103) y sólo tres utilizaron la radiografía torácica estándar (104-106). También se identificó un estudio sobre una regla de de predicción posterior (109) en el que se incluyó como variable predictiva el número de fracturas costales.
En el estudio retrospectivo de Battle de 2013 (106), los autores recogieron los datos de 174 pacientes con traumatismo torácico cerrado y se calculó el riesgo de presentar complicaciones, encontrando que la presencia de tres o más fracturas costales se asociaba con un OR ajustado de presentar complicaciones del 3,1 (IC95 % de 1,5 a 6,6). De hecho, en el estudio sobre la derivación y validación de la regla de predicción de complicaciones (definida como mortalidad hospitalaria, morbilidad (incluyendo todas las complicaciones pulmonares como infección torácica, neumonía, hemotórax, neumotórax, efusión pleural o empiema, así como el ingreso en UCI o una estancia hospitalaria prolongada (7 días o más)) en pacientes con traumatismo torácico cerrado del mismo autor (109), los autores encuentran como factores predictivos significativos entre otros al número de fracturas costales, siendo el OR para cada fractura costal adicional de 1,5 (IC95 % de 1,3 a 1,9).
Calidad
moderada
Los otros dos estudios valoran la asociación del número de fracturas costales con la aparición de neumonía posterior al trauma (104;105). En el estudio de Ho et al (104), se observa que la incidencia de neumonía a los 30 días es del 1,6 % (11/709), siendo el HR (ajustado por edad, sexo, diabetes, hipertensión, enfermedad cardiovascular, asma y enfermedad pulmonar obstructiva crónica (EPOC)) de 8,94 (IC95 % de 3,79 a 21,09>; p<0,001) cuando se les compara con pacientes no traumáticos. De hecho, la edad (≥65 años; HRa (Hazard Ratio ajustado) =5.60, IC95 % de 1,97 a 15,89, p<0,001) y la presencia de EPOC (HRa=5,41; IC95 % de 1,02 a 3,59, p<0,001) eran factores de riesgo para el desarrollo de neumonía. La presencia de una o dos fracturas costales aisladas se asociaba con un aumento del riesgo de neumonía con un HRa de 3,97 (IC95 % de 1,09 a 14,44; p<0,001) y de 17,13 (IC95 % de 6,66 a 44,04; p<0,001), respectivamente, aunque los intervalos de confianza son muy amplios.
En el estudio de Chauny et al (105) incluye de forma prospectiva 347 pacientes ingresados en urgencias por lesiones torácicas menores con al menos una costilla, solo seis pacientes desarrollaron neumonía durante el seguimiento. El RR para pacientes con enfermedad pulmonar preexistente y fractura costal diagnosticada radiológicamente era de 8,6 (IC95 % de 1,05 a 70,9). En este estudio prospectivo se revela una baja incidencia de neumonía tardía (a las dos semanas), aunque el estudio apoya el seguimiento específico de pacientes con asma o EPOC y fractura costal.
Calidad
baja
Resultados de la actualización de la búsqueda
En la actualización entre enero de 2017 y enero de 2018, se identificó un estudio que abordaba la variabilidad entre los médicos de urgencias a la hora de pedir una TC (110). En la búsqueda de otra de las preguntas de la guía se identificó otro estudio sobre la adecuación de la TC en pacientes con TTCNG, en el que se señalan de forma descriptiva los factores que podrían asociarse a la presencia de resultados anormales en la TC (111). En este último estudio, se recogen los signos de alarma que podrían orientar a realizar una TC en pacientes con traumatismo torácico.
En la actualización realizada hasta junio de 2019, se identificaron tres estudios más de interés. Safari et al (112), compararon la S y E de las dos reglas TIRC y NEXUS Chest en pacientes con traumatismo torácico cerrado, encontrando una S similar en predecir lesiones intratorácicas tras un traumatismo múltiple cerrado. Por lo tanto, este estudio no cambia las conclusiones de lo ya descrito.
El estudio de Hansen et al (113), donde los autores desarrollaron una nueva medida (TC Score negativo), que cuantifica la frecuencia con la que la TC identifica lesiones importantes, viene a señalar la necesidad de adecuar el uso de esta prueba. Por último, el estudio de Singleton JM et al (114), determinaba si las fracturas costales diagnosticadas solo por TC en pacientes ancianos (media de 84 años) tras una caída se asociaba con el aumento de la utilización de recursos o de mortalidad. A pesar de un aumento en la tasa de ingreso hospitalario (91 % vs.78 %; p=0,02), no hubo diferencias entre los pacientes con o sin fracturas ocultas en la duración de la estancia hospitalaria, el ingreso en UCI o mortalidad intrahospitalaria. Por ello se concluye que la edad en sí misma no sería un criterio para realizar una TC, lo que estaría de acuerdo con los criterios propuestos por la regla NEXUS Chest.
Resumen de la evidencia
| Regla NEXUS Chest | |
|---|---|
| Calidad moderada | Tanto cuando se aplican las reglas NEXUS Chest-CT Major como la NEXUS Chest All, y todos los criterios de la regla son negativos, se puede evitar la realización de una TC y descartar la presencia de lesión severa con una S del 99,2 % (82). |
| Calidad moderada | En la regla NEXUS Chest, cuando se cumple de forma aislada el criterio de presentar una radiografía anormal, la S y E de identificar una lesión clínicamente grave sería del 73,3 % (IC95 % de 68,1 a 78,6 %) y del 83,9 % (IC95 % de 83,6 a 84,2), respectivamente. Si solo se cumpliera un criterio de la regla que no fuera una radiografía anormal, la probabilidad de cualquier lesión o de lesión clínicamente grave sería muy baja (del 16,8 % y del 1,1 %, respectivamente). Si se presentaran dos criterios, las prevalencias serían del 25,5 % y del 3,2 %, respectivamente, y si se cumplieran tres, del 34,9 (31 %-39 %) y 2,7 %, respectivamente (83). |
| Tres o más fracturas costales | |
| Calidad baja | La presencia de tres o más fracturas costales (OR de 2,02) se asocia con un mayor riesgo de mortalidad en pacientes con traumatismo torácico (92). |
| Calidad moderada | La presenciad de tres o más fracturas en radiografía se asocia con mayor prevalencia de complicaciones asociadas (OR por cada fractura costal adicional de 1,5; IC95 % de 1,3 a 1,9) (109). |
| Calidad baja | La presencia de al menos una fractura costal se asocia con un mayor riesgo de neumonía, sobre todo si hay enfermedad pulmonar preexistente (104;105). |
De la evidencia a la recomendación
Los aspectos que han determinado la fuerza y dirección de las recomendaciones han sido los siguientes:
- Calidad global de la evidencia: calidad baja-moderada, tanto para pacientes con radiografía normal como anormal. La evidencia acerca del riesgo de complicaciones y/o mortalidad asociada a la presencia de tres o más fracturas costales diagnosticadas por radiografía es de calidad baja-moderada.
- Balance entre beneficios y riesgos:
- Pacientes con radiografía normal: probablemente los efectos no deseables superan los deseables.
- Pacientes con radiografía anormal: probablemente los efectos deseables superan los no deseables.
- Utilización de recursos: los costes y recursos necesarios para una TC rutinaria superaría a los beneficios.
- Equidad: las desigualdades probablemente aumentarían si se recomendara realizar una TC rutinaria en todos los pacientes, puesto que no en todos los centros se podría ofrecer.
- Aceptabilidad: la aceptabilidad de la opción es incierta.
- Factibilidad: la realización de una TC torácica rutinaria probablemente no sería factible.
El grupo de trabajo considera que en los pacientes objeto de la guía la realización de una TC debe ser poco frecuente o excepcional. Los criterios de adecuación de la ACR (79) establecen un grado de adecuación de 5 sobre 9 en los traumatismos en los que no existe un mecanismo de alta energía (radiografía de tórax, examen físico y nivel de conciencia normales).
De las dos reglas de predicción clínica (RPC) que establecen unos criterios cuya ausencia permite excluir la necesidad de realizar una TC con seguridad, se descarta la regla SCARP (por ser desarrollada para pacientes con traumatismo torácico grave y traumatismo cranoencefálico no grave). Se extrapolan los resultados de la regla NEXUS Chest CT, que incluye como criterios sensibilidad esternal, escapular, de la pared torácica o de la zona torácica, lesión distractora, mecanismo rápido de deceleración y el resultado radiográfico anormal. El criterio aislado que tiene más S y E para detectar lesión torácica grave o cualquier tipo de lesión es la radiografía anormal.
Si solo se cumpliera un criterio de la regla NEXUS-Chest-CT que no fuera el de presentar una radiografía anormal, la probabilidad de cualquier lesión o de lesión clínicamente grave sería muy baja. Por lo tanto, cuando la radiografía es anormal se recomienda realizar una TC. En el caso en el que la radiografía es normal, pero se cumpla uno o más del resto de los criterios, se recomienda individualizar la necesidad de realizar dicha prueba.
Se han extrapolado los resultados de la guía NEXUS-Chest y otros estudios retrospectivos, ya que el riesgo de cualquier tipo de lesión o de lesión grave es muy bajo en los pacientes que competen a esta guía. Si el criterio de radiografía normal se asocia con una exploración física y análisis de sangre normales, la fuerza de la recomendación de no hacer la TC sería aún mayor. En el caso de existir discordancia clínico-radiológica, se ha establecido por consenso la consideración de realizar la TC de forma individualizada.
No se ha encontrado evidencia en cuanto a la indicación de la TC según el número de fracturas visibles en la radiografía de tórax PA y lateral. Los estudios hacen referencia a la relación entre el número de fracturas y la morbi-mortalidad, encontrando asociación entre ésta y la existencia de tres o más fracturas, edad igual o superior a 65 años, presencia de multimorbilidad (enfermedad cardiovascular, asma y EPOC), uso previo de anticoagulantes y niveles de saturación oxígeno bajos. Por ello, acordamos por consenso mantener el hallazgo radiológico de tres o más fracturas costales en la radiografía de tórax PA y lateral como uno de los criterios para indicar la realización de la TC.
Con respecto a la locación de las fracturas, la afectación de cualquiera de las tres primeras costillas es un indicador de un traumatismo de alta energía. Aunque es poco probable que los pacientes de nuestra guía presenten fracturas costales en esta localización, si existen se recomienda la realización de una TC.
En resumen, las recomendaciones que se han realizado han sido las siguientes:
Recomendaciones
| Fuerte | Se recomienda no realizar una TC torácica en pacientes con TTCNG y con radiografía PA y lateral normal, salvo que exista una discordancia clínica-radiológica evidente. |
| Fuerte | Se recomienda no realizar una TC torácica en pacientes con TTCNG que presenten menos de tres fracturas costales en radiografía PA y lateral, salvo que se trate de la primera a la tercera costilla. |
| Débil | Se sugiere valorar de forma individualizada realizar una TC torácica en pacientes con TTCNG cuando se presentan los siguientes hallazgos en la radiografía convencional de tórax:
|
| √ | En casos de pacientes con TTCNG y con fracturas costales bajas, considerar la posibilidad de realizar una TC si se sopechan lesiones abdominales. |
| √ | Considerar la posibilidad de realizar una TC a aquellos pacientes con TTCNG en los que existan limitaciones para la realización o correcta interpretación de la radiografía simple. |
Consideraciones para la implementación
- Los centros que no dispongan de TC deberían derivar al paciente a otro centro que disponga de ella.
5.2. Otras pruebas diagnósticas
5.2.1. Análisis de sangre
Preguntas a responder:
- ¿Cuándo es deseable realizar un análisis de sangre en pacientes con antecedente de TTCNG?
Actualmente, en los servicios de urgencia se solicitan gran cantidad de pruebas analíticas de forma rutinaria, pero frecuentemente los hallazgos no influyen en el manejo del paciente.
La realización de análisis de rutina en nuestro paciente no aporta mayor valor diagnóstico a la exploración física y anamnesis detallada y se asocia a un aumento de costes, riesgos y de la estancia en los servicios de urgencias.
La realización de análisis y sus resultados no deben demorar la realización de pruebas de imagen que aportan mayor precisión diagnóstica en la detección de lesiones ocultas tras un traumatismo torácico de no alta energía.
El uso rutinario de una bioquímica sanguínea o un estudio de coagulación tienen un valor limitado en la evaluación de pacientes con TTCNG.
Evidencia científica
Se preseleccionaron tres estudios: un artículo que estudia la disminución en la solicitud de peticiones analíticas tras la implementación de un algoritmo en pacientes con traumatismo y pacientes que van a ser intervenidos quirúrgicamente (115), un análisis retrospectivo (116) con pacientes ASA 1 (Sistema de clasificación de la American Society of Anesthesiologists (ASA), paciente sano y asintomático) que van a ser sometidos a cirugía ortopédica menor o moderada y un último estudio de costes que pretende determinar el ahorro y la seguridad de limitar las pruebas de laboratorio en pacientes que han sufrido un traumatismo (117).
A través de los miembros del grupo de trabajo y de los colaboradores expertos, se han identificado otros cuatro estudios, tres de ellos relacionados con el alto coste y el poco impacto de los análisis rutinarios en el manejo del paciente con traumatismo (sobre todo traumatismo menor) (118-120) y el último (121) relacionado con el aumento del número de flebotomías y su impacto en el desarrollo de anemia y de la necesidad de transfusiones de sangre tras un traumatismo.
El estudio de Chu UB et al (118), de tipo antes y después, compara la realización de análisis rutinario (grupo I) frente a análisis a criterio clínico (grupo II) en el manejo inicial del paciente con traumatismo, encontrando una reducción significativa en el número de análisis realizados (93 % frente al 27 % de pacientes del grupo I y II, respectivamente) sin diferencias en el porcentaje de pacientes en que el análisis conlleva a una intervención (7 % vs 8 %), mortalidad (8 % vs 9 %), duración de la estancia hospitalaria (6,9 ± 9 días vs 3,04 ± 7), y un ahorro importante de costes (calculado en 1,5 millones de $ en 1 año, teniendo en cuenta que en tres meses el ahorro total supondría 378.945 $, con una n de 603 pacientes).
En el estudio de Tasse et al (119) que analizaba el impacto de la realización rutinaria de estudios radiológicos y análisis en todos los pacientes traumáticos atendidos en un período de tres meses, encontraron que el número de test con resultados anormales era muy bajo para todos los análisis realizados (121). Ikegami et al (120) también observaron que en el subgrupo de traumatismo leve, aunque la petición de análisis era frecuente, la presencia de resultados positivos no lo era (<1 %) en comparación con pacientes con traumatismo grave o potencialmente grave.
Por último, el estudio de Branco et al (121) que compara los datos de una serie de pacientes admitidos en un centro de traumatismo de nivel 1 (entre marzo y abril de 2004) con otra serie de pacientes admitidos en el mismo período durante 2009, encontró que no había diferencias demográficas o clínicas en el número de días de ingreso hospitalario o de ingreso en UCI o en mortalidad. Sin embargo, entre 2004 y 2009, la media del número de análisis sí aumentó de forma significativa (de 21,2 ± 32,5 a 28,5 ± 44,4; p = 0,003), así como el volumen de sangre extraída durante la estancia hospitalaria (de 144,4 ± 191,2 ml a 187,3 ± 265,1 ml; p=0,025) y los costes de laboratorio, que aumentaron en un 25 % por al aumento del número de análisis solicitados.
Calidad
muy baja
para todos
los desenlaces
Para elaborar el algoritmo de petición de análisis de sangre en los pacientes objeto de la guía, se ha tenido en cuenta el artículo de Faulkner et al (115), en el que se describe una serie de recomendaciones consensuadas para determinar en qué pacientes admitidos en unidades de traumatismo o ingresos ortopédicos se debe realizar un análisis. El algoritmo propuesto fue adaptado por los miembros del grupo de trabajo de la guía, puesto que los pacientes a los que ésta se dirige no son exactamente los mismos.
Así, se ha eliminado la petición de PCR (proteína C reactiva), puesto que no son pacientes que vayan a ser sometidos a cirugía, sino pacientes con TTCNG.
Se ha eliminado también la parte del algoritmo orientado a pacientes con sepsis o shock precoz. También se ha eliminado la edad como factor independiente para realizar una analítica, puesto que a pesar de ésta se asocia con la presencia de mayor multimorbilidad, no se ha encontrado evidencia que la sustente como criterio que en sí mismo indique la necesidad o beneficio de llevar a cabo una analítica (incluso en las principales guías en el preoperatorio no se considera la edad un criterio para solicitar dicha prueba) (122-124).
En la búsqueda realizada sobre la asociación entre fractura costal con lesión intra-abdominal se encontraron tres estudios que describían un mayor riesgo de lesión intra-abdominal en pacientes con fracturas costales, localizadas sobre todo en la parte derecha y entre la octava y duodécima costilla (125-127). También se han encontrado estudios que describen la asociación entre enzimas hepáticas alteradas y la presencia de lesión hepática en pacientes con traumatismo abdominal. Por lo tanto, se mantiene la petición del perfil hepático, en los casos en los que se sospeche de lesión hepática.
Teniendo en cuenta todo esto, así como las recomendaciones realizadas para las preguntas sobre la petición de enzimas cardíacas y la gasometría arterial, el algoritmo final que se propone es el siguiente (Figura 1):

Resumen de la evidencia
| Calidad muy baja | La realización de análisis de rutina frente a su realización según criterio clínico no aporta beneficios en cuanto a la reducción de mortalidad, estancia hospitalaria o de intervenciones en pacientes con traumatismo, por lo que supone además un gasto innecesario (118-121). |
De la evidencia a la recomendación
Los aspectos que han determinado la fuerza y dirección de las recomendaciones han sido los siguientes:
- Calidad global de la evidencia: la calidad de la evidencia es muy baja. Los estudios identificados son en pacientes con traumatismo cerrado en general y describen el impacto de realizar análisis de forma rutinaria, tanto en el manejo clínico (mortalidad, morbilidad, cambio en el manejo, etc.) como en los costes para la organización.
- Balance entre beneficios y riesgos: realizar análisis de forma rutinaria no parece ofrecer beneficios en el manejo del paciente traumático y tiene un alto coste.
- Utilización de recursos: dos estudios recogen el gasto que se podría haber evitado al pedir análisis sólo cuando éstos están clínicamente indicados. En el estudio de Chu et al (118) se calcula que el ahorro anual podría situarse en torno a 1,5 millones de dólares (teniendo en cuenta que el ahorro en tres meses sería de 378.945 dólares con una n de 603 pacientes con traumatismo cerrado que acuden a urgencias). En el estudio de Tasse et al, en un hospital que registra 1.500 pacientes traumáticos al año, se observa que, con una n de 410 pacientes, evitar hemogramas rutinarios tendría un ahorro potencial de 20.986 dólares, y la determinación de electrolitos y creatinina de 56.391 dólares. Asimismo, evitar Tiempo de Protrombina (TP)/ Tiempo de tromboplastina (TTP) rutinarios tendría un ahorro de 20.158 dólares.
- Equidad: las desigualdades probablemente aumentarían. Si se recomienda realizar análisis rutinarios en todos los pacientes con traumatismo, puede que algunos centros sanitarios no los puedan realizar.
- Aceptabilidad: probablemente la opción sea aceptada por los implicados.
- Factibilidad: probablemente la realización de análisis de rutina sea factible.
El resultado del análisis rutinario en pacientes con TTCNG, mecanismo de lesión de baja energía, sin historial médico significativo y que no tomen anticoagulantes o antiagregantes es normal la mayoría de las veces y no cambia el manejo. Además, está asociado a un aumento de los costes, riesgo y estancias, por lo que no se recomienda.
Sin embargo, los pacientes con multimorbilidad o tratamientos crónicos sí pueden tener alteraciones en el análisis que requieran de monitorización y ajustes de tratamiento. A los que toman anticoagulantes y antiagregantes se precisa un análisis basal para su control evolutivo.
Cuando hay historia o sospecha de lesión hepática, sí que está indicada la realización de test de función hepática, puesto que la elevación de las transaminasas está relacionada con su existencia y severidad. Por ello, las recomendaciones que se han realizado son las siguientes.
Recomendaciones
| Débil | Se sugiere no realizar análisis de forma rutinaria en pacientes con TTCNG con o sin lesiones leves asociadas y que no presentan historia médica significativa. |
| √ | Pedir hematometría, urea, creatinina y electrolitos en cualquier paciente con TTCNG y multimorbilidad significativa. |
| Débil | Se sugiere solicitar perfil hepático si existe sospecha de traumatismo hepático. |
| √ | En caso de que exista historia de discrasia sanguínea, o el paciente con TTCNG tome medicación anticoagulante, añadir a lo anterior un perfil básico de coagulación. |
5.2.2. ECG y medición de enzimas cardíacas
Preguntas a responder:
- En pacientes con TTCNG, ¿se debe pedir un ECG (electrocardiograma) y la medición de enzimas cardíacas?
El traumatismo torácico, y más concretamente el que sucede sobre la zona precordial (asociada o no a fractura esternal), puede asociarse a contusión miocárdica. En pacientes con traumatismo grave puede existir una alta prevalencia de esta complicación, mientras que en el paciente objeto de esta guía ocurrirá excepcionalmente.
Clínicamente, la contusión miocárdica puede ser asintomática o manifestarse en forma de arritmias malignas o fallo cardíaco grave, pudiendo suponer en casos extremos un peligro vital.
Para su diagnóstico se utiliza habitualmente el electrocardiagrama y la medición analítica de las enzimas cardiacas (creatina quinasa (CK) e isoenzimas, troponina I (TnI), troponina T (TnT…), pudiendo ser complementaria la realización de un ecocardiograma para descartar lesiones cardiacas estructurales o evaluar la repercusión sobre la función miocárdica. Sin embargo, se desconoce si el electrocardiograma es una técnica realmente sensible para descartar la contusión miocárdica en pacientes traumáticos o si es necesario o no pedir la determinación analítica de marcadores de daño miocárdico de forma sistemática, o sólo cuando éste resulte estar alterado.
Evidencia científica
La gravedad de la contusión cardiaca es la que puede determinar un mayor riesgo de desarrollar complicaciones cardíacas tras un traumatismo torácico cerrado. Sin embargo, la mayoría de los estudios tratan de cuantificar el número de pacientes que presentan contusión cardiaca y no complicaciones cardíacas, utilizando para ello diferentes definiciones que incluyen o no la medición de niveles de enzimas cardíacas (CK-MB o la Troponina I o T) o la presencia de alteraciones en el electrocardiograma o en la ecocardiografía. Lo que realmente sería interesante conocer es el riesgo de desarrollar complicaciones tras un traumatismo torácico, y no tanto el porcentaje de pacientes que presentan contusión miocárdica, ya que en la mayoría de los casos ésta no tiene mayores consecuencias.
Se ha identificado una GPC sobre el manejo de pacientes con traumatismo torácico cerrado y sospecha de lesión cardiaca cerrada (128) que se ha utilizado como punto de partida para realizar la búsqueda RS posteriores. Así, se ha identificado una RS posterior sobre el VPN de la troponina cardíaca para predecir eventos cardíacos adversos en pacientes con traumatismo torácico cerrado (129). También se ha realizado una búsqueda de estudios individuales para esta pregunta recuperando 178 referencias, aunque ninguna de ellas fue relevante para responder a la pregunta.
En la guía identificada se incluyen cinco estudios (53;130-133), de los que cuatro concluyen que la fractura esternal no es un marcador de contusión miocárdica en sí misma (53;131-133).
En cuanto a la realización de ECG y enzimas cardíacas, son cuatro los estudios primarios que combinan el el uso de ambos tests. El primero de ellos (134) encontró que las únicas variables que predecían de forma significativa eventos electrocardiográficos clínicamente significativos (arritmias malignas) eran un nivel de troponina T > 0,20 micro g/L y la presencia de alteraciones iniciales en el ECG, aunque la S y E de ambos test era muy baja (del 27 % y 91 %, respectivamente, para la troponina T (Valor Predictivo Positivo (VPP) y VPN del 64 % y 68 %) y del 38 % y de 93 %, respectivamente para el electrocardiograma inicial (VPP y VPN de 77 % y 72 %). Tras un análisis de regresión logística, se obtuvo una ecuación que era capaz de clasificar de forma correcta el 74 % de los casos (chi squared = 14,124, p= 0,0069). Así, un paciente con una alteración en la ECG basal clínicamente significativa y resultados positivos para la Troponina T tenía una probabilidad del 64 % de desarrollar un resultado electrocardiográfico significativo. Por otro lado, la probabilidad de un paciente que solo presentaba positivo uno de los dos test se situaba entre el 21 y 44 %.
De los otros tres estudios señalados dos son estudios de los mismos autores. El estudio de Velmahos et al (137), incluye los datos de los pacientes del estudio de Salim et al (136), por lo que este último no ha sido considerado. En el estudio de Velmahos et al, se quiso determinar si la combinación del electrocardiograma y la troponina I (TnI) podía servir como marcador fiable de presencia o ausencia de lesión cardiaca cerrada significativa (definida como presencia de shock cardiogénico, arritmias que requerían tratamiento o déficits estructurales postraumáticos). En este estudio, se diagnosticó traumatismo cardíaco significativo en 44 de los 333 pacientes (13,2 %) (137).
Asimismo, de los 80 pacientes que presentaban valores anormales de TnI y ECG alterado, 27 (36 %) desarrollaron lesión significativa. De 122 pacientes que presentaban alteraciones en uno de los dos test, presentaron lesión significativa en el 7 % (5/67) y el 22 % (12/55) de los casos, respectivamente. De los 131 pacientes con resultados normales para los dos test ninguno desarrolló lesión cardiaca cerrada significativa (ver Tabla 22 y Figura 2).
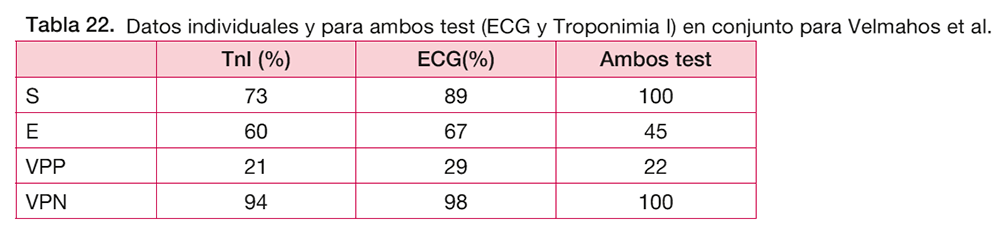
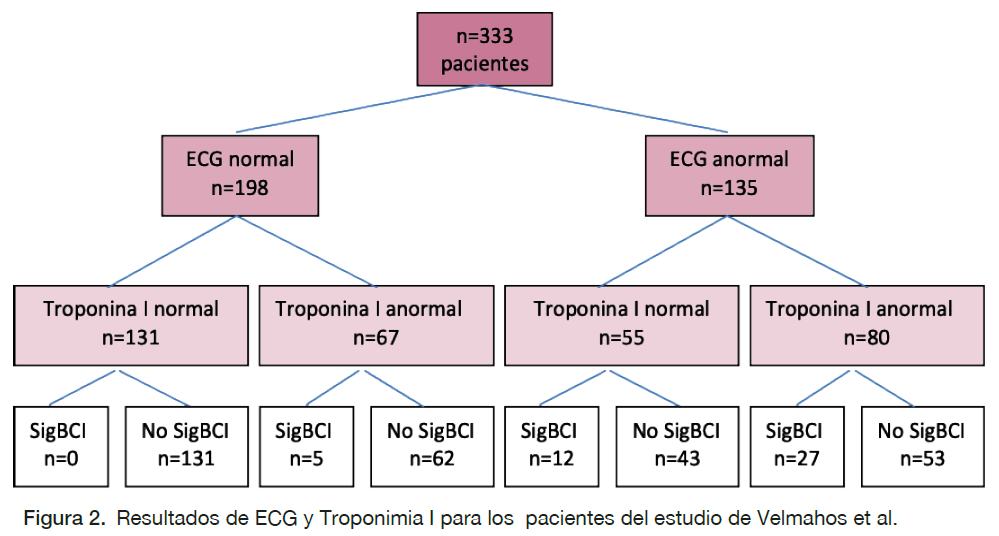
Esto significa que, si se aplicaran ambos test en 1.000 pacientes con sospecha de lesión cardíaca significativa, y la prevalencia de ésta fuera del 13,2 %, no se escaparía ningún caso (0 FN), aunque habría 475 FP.
Calidad
baja
para todos
los desenlaces
El cuarto estudio identificado es el estudio de Collins et al (142), que cuenta con 66 pacientes con un traumatismo torácico cerrado no intubados y normotensos, con dolor torácico o dolor esternal. Los autores de este estudio realizan a todos los pacientes un ECG y una radiografía de tórax, y midiendo las enzimas cardíacas entre cuatro y seis horas tras el trauma. Sólo se diagnosticó lesión cardiaca significativa en dos pacientes (3 %) (pacientes con disfunción ventricular izquierda que requirió tratamiento inotrópico), pertenecientes al grupo de 10 pacientes con valores de troponina alterados. 40 pacientes presentaron resultados normales para el ECG y troponina y los 16 restantes, un ECG alterado, pero con valores de troponina normales. En estos últimos dos grupos no se registraron complicaciones cardíacas significativas. La prevalencia de lesión cardiaca cerrada significativa en este estudio fue muy baja (3 %). La radiografía fue normal en 2/3 de los pacientes, y no hubo arritmias que necesitaran tratamiento.
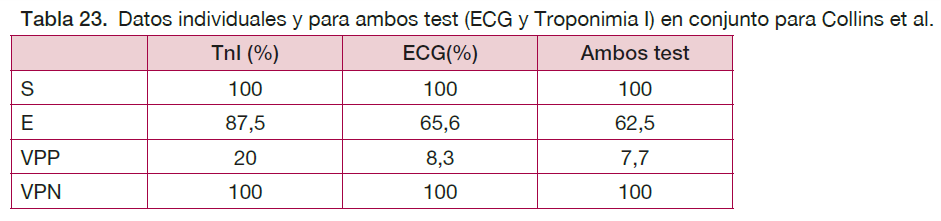
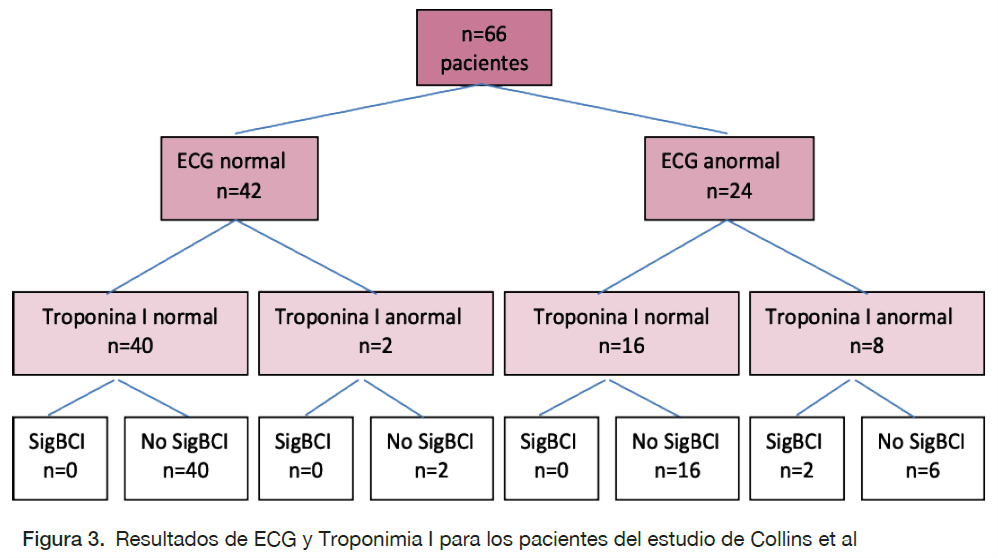
Esto significa que, si se aplicaran ambos test en 1.000 pacientes con sospecha de lesión cardíaca significativa, y siendo la prevalencia del 3,1 %, no se escaparía ningún caso (0 FN), y el número de FP sería de 364. Los VN serían 606 de 1.000.
Calidad
baja
para todos
los desenlaces
Resumen de la evidencia
| Calidad baja | La combinación del ECG y la medición de troponina I permite descartar lesión cardíaca significativa, pero tiene un alto número de FP (137). En el estudio de Collins et al, más cercano a los pacientes objeto de la guía, el ECG por sí solo también permite descartar lesión cardíaca significativa (142). |
De la evidencia a la recomendación
Los aspectos que han determinado la fuerza y dirección de las recomendaciones han sido los siguientes:
- Calidad global de la evidencia: baja.
- Balance entre beneficios y riesgos: según el estudio de Collins et al, con la realización solo de un ECG se podría descartar la presencia de lesión cardíaca significativa, pero en el de Velmahos, que incluye pacientes más graves, se señala que podría haber casos no diagnosticados si no se incluye también la medición de Troponina I. Hay que tener en cuenta que pueden existir casos de contusión miocárdica con riesgo de compromiso vital, por lo que no diagnosticar uno de ellos puede ser muy perjudicial.
- Utilización de recursos: La determinación analítica de las enzimas cardiacas puede ser costosa.
- Equidad: las desigualdades reducirían por disminuir la variabilidad entre los centros.
- Aceptabilidad: es probable que tanto médicos como pacientes vean como inaceptable no diagnosticar una contusión miocárdica dada su potencial gravedad.
- Factibilidad: En nuestro medio, la implementación de la medición de troponina y la realización de ECG puede obligar a derivar a pacientes a centros sanitarios donde se realice la determinación analítica de marcadores de daño miocárdico.
Tanto el electrocardiograma como la determinación analítica de marcadores de daño miocárdico poseen un VPN del 100 %. En el análisis de la literatura, se objetiva que la prevalencia de lesión cardiaca significativa para pacientes con ISS bajo, como en este caso, es muy bajo, lo que junto al alto VPN del electrocardiograma llevaría a la determinación innecesaria de Troponina I en muchos de los pacientes. Además, es altamente improbable la existencia de una lesión significativa en un paciente con TTCNG que se encuentre asintomático en las primeras 24 horas y además tuviese un electrocardiograma normal. Por ello se han formulado las siguientes recomendaciones:
Recomendaciones
| Débil | Se sugiere realizar un electrocardiograma a todos los pacientes con TTCNG cuyo mecanismo lesional implique un golpe contundente sobre la región precordial, asocie o no fractura esternal. En el caso de que éste se encuentre alterado o exista discordancia clínica, se realizará una determinación analítica de Troponina I. Así mismo, cuando la determinación inicial muestre cifras normales, se sugiere repetir la determinación pasadas como mínimo seis horas después del traumatismo. |
| Fuerte | Se recomienda no realizar la medición analítica sistematica de CK e isoenzimas (CK-MB) en pacientes con TTCNG. |
Consideraciones para la implementación
- Los centros que no dispongan de TC deberían derivar al paciente a otro centro que disponga de ella.
5.2.3. Pulsioximetría frente a gasometría arterial
- ¿Se puede utilizar la pulsioximetría en vez de la gasometría arterial en pacientes con TTCNG?
Para valorar el estado de oxigenación de un paciente de manera precisa se recomienda realizar un análisis de sangre arterial y medir la presión parcial de oxígeno (PaO2) de la misma. Para ello, se debe de extraer una muestra de sangre arterial, con las molestias, los riesgos y los costes que conlleva. Se define hipoxemia cuando la presión parcial de oxígeno es inferior a 80 mmHg, y cuando disminuye de 60 mmHg hablamos de insuficiencia respiratoria, situación en la que se puede comprometer el aporte de oxígeno a los tejidos repercutiendo en el metabolismo celular (hipoxia).
Por otro lado, disponemos de los pulsioxímetros, aparatos que nos cuantifican el porcentaje de saturación de oxígeno de la hemoglobina en sangre (SpO2) de una manera no invasiva con ayuda de métodos fotoeléctricos. Gracias al desarrollo de estos dispositivos y el conocimiento de la correlación entre la saturación de oxígeno con la presión parcial de oxígeno -que viene determinada por la curva de disociación de la oxihemoglobina-, se ha disminuido la cantidad de punciones arteriales para cuantificar la PaO2 permitiendo una monitorización –no invasiva y fiable- del estado de oxigenación de los pacientes.
El punto de corte de 60 mmHg de la PaO2 lo determina la morfología de la curva de disociación de la hemoglobina y corresponde a una saturación de oxigeno arterial del 90 %. Por debajo de este punto, pequeñas disminuciones en la saturación de oxigeno conllevan a variaciones sustanciales de la PaO2.
Es importante objetivar el nivel de oxígeno de los pacientes, ya que en situaciones de insuficiencia respiratoria aguda se debe de iniciar oxigenoterapia junto con el resto de tratamientos que el paciente precise, en función de la causa desencadenante de dicha situación.
No debemos olvidar que para que la pulsioximetría sea fiable se debe de realizar con aparatos homologados y de calidad y que la interpretación de los resultados debe de ser analizada por un profesional adiestrado para minimizar el error de la medición por los factores limitantes conocidos, como pueden ser la baja temperatura de la zona donde se coloca el pulsioxímetro, el esmalte de uñas, una mala perfusión periférica, etc.
Evidencia científica
Se ha identificado una GPC de la Sociedad Torácica de Australia y Nueva Zelanda de 2013 (143) en la que se realizan una serie de recomendaciones prácticas para la implementación de dicha técnica.
En la búsqueda de RS realizada sólo se identificó una revisión de interés (144), que buscaba:
- Describir la fuerza de la asociación de la saturación de oxígeno arterial medida por pulsioximetría frente al estándar de gasometría arterial medida por co-oximetría.
- Examinar cómo afectan varios factores a esta relación.
- Describir un estimador agregado para el sesgo y la precisión entre la saturación de oxígeno medida por pulsioximetría y por el estándar.
Sin embargo, lo que se quiere es conocer el punto de corte a partir del cual la pulsioximetría tiene la mejor S y E para detectar hipoxemia en el paciente. Por ello, se ha realizado una búsqueda de estudios individuales sobre las curvas ROC (Receiver Operating Characteristic) en pacientes con sospecha de hipoxemia.
De cuatro (145-148) referencias preseleccionadas, se incluyeron finalmente dos, puesto que el artículo de Lee et al (147) incluía pacientes más graves (preoxigenados con O2 al 100 %, algunos hipotensos y/o anémicos) y el de Kohyama et al (148) pacientes en UCI que, por sus características propias (hipertensión pulmonar), difieren de la población general.
Los dos artículos seleccionados incluyeron pacientes con EPOC (145;146). El primero (145) es un análisis de subgrupos de un estudio prospectivo realizado en un Servicio de Urgencias (por muestreo de conveniencia). El objetivo de este estudio era determinar la correlación y el grado de acuerdo entre la saturación de oxígeno arterial y la saturación medida por pulsioximetría en urgencias, así como el punto de corte del cribado de lo que definen hipoxia sistémica significativa (PaO2 (presión parcial de oxígeno arterial <60 mmHg) en pacientes con EPOC.
El segundo estudio (146) es un estudio transversal anidado en una cohorte prospectiva (IRYSS-COPD) con el fin de validar los puntos de corte para detectar hipoxemia con alta probabilidad, determinar si la saturación de oxígeno medida por pulsioximetría se correlacionaba con hipoxemia o fallo respiratorio en los pacientes con exacerbaciones agudas de EPOC e identificar posibles factores de confusión en esta relación. En este estudio cabe destacar que se excluyeron pacientes con una saturación >92 % al llegar a urgencias, pacientes con valores altamente discordantes (como PaO2 arterial <60 mm Hg y saturación >90 %) (en el 6,3 % de los episodios) o aquellos con PaO2>100Hg (82 pacientes: 2,85 %).
En ambos estudios parece que la S es de un 100 %, lo que implica que no hay FN (no se escapa ninguna hipoxemia utilizando un punto de corte para la pulsioximetría del 92 % o del 90 %, según el estudio). Esto significa que en estos pacientes se evitaría realizar una gasometría arterial. En cuanto a los FP, estos disminuyen conforme aumenta la prevalencia de hipoxemia en la población en la que se aplica la prueba, siendo de 120 sobre 1.000 y de 81 sobre 1.000 cuando la prevalencia era del 14 % y del 49,4 %, respectivamente.
Calidad
baja
para todos
los
desenlaces
Resumen de la evidencia
| Calidad baja | La pulsioximetría no produce FN cuando se utiliza un punto de corte entre el 90 % y el 92 % (145;146). |
| No hay estudios | No se sabe el impacto que tiene el uso de la pulsioximetría en los desenlaces del paciente. |
De la evidencia a la recomendación
Los aspectos que han determinado la fuerza y dirección de las recomendaciones han sido los siguientes:
- Calidad global de la evidencia: la confianza en la calidad de la evidencia es baja.
- Balance entre beneficios y riesgos: los efectos deseados probablemente superan los efectos no deseados en la mayoría de los escenarios.
- Utilización de recursos: los recursos requeridos probablemente sean pequeños y el incremento del coste en relación a los beneficios también.
- Equidad: las desigualdades probablemente reducirían.
- Aceptabilidad: opción probablemente aceptable por los agentes implicados.
- Factibilidad: la implementación de la opción probablemente sea factible
Dado que existe una correlación entre la SpO2 de 92 % con la probabilidad de padecer insuficiencia respiratoria (PaO2 menor de 60 mmHg), aunque la calidad de la evidencia es baja, como se trata de un método diagnóstico poco invasivo y fiable, recomendamos la realización en la valoración inicial a todos los pacientes que presenten un TTCNG. En función del resultado, se deberá valorar la necesidad de implementar oxigeno suplementario. Así, las recomendaciones serían las siguientes.
Recomendaciones
| Fuerte | Se recomienda realizar pulsioximetría a todos los pacientes con TTCNG en la atención inicial. |
| Débil | En caso de una lectura inferior al 92 %, se sugiere valorar la realización de una gasometría arterial basal. |
| √ | Teniendo en cuenta la existencia de factores que pueden alterar los resultados de la medición (extremidad fría, laca de uñas, alteración de la perfusión o grandes fumadores, entre otros), cuando los valores son discordantes con la clínica deberían validarse los resultados mediante gasometría arterial basal. |
Consideraciones para la implementación
A la hora de implementar de manera rutinaria el uso de los pulsioxiometros hay que tener en cuenta la importancia del mantenimiento correcto de los dispositivos que se emplean -sobre todo cuando se utilizan sensores reutilizables- y de las limitaciones de su uso como son los siguientes:
- Sospecha de intoxicación por inhalación de monóxido de carbono o dishemoglobinemias, se deberían validar las mediciones mediante gasometría arterial ya que absorben longitudes de ondas similares a la oxihemoglobina pudiendo magnificar su valor.
- El valor de SpO2 (Saturación periférica de Oxígeno) puede ser normal a pesar de la existencia de anomalías en la ventilación alveolar (indicadas por arterial CO2 tension o estado ácido-base (indicado por pH), particularmente si el paciente está con oxigenoterapia suplementaria. El artefacto en la señal se puede dar por movimiento del paciente o del sensor, factor a tener en cuenta en las mediciones.
- El color de la piel, la utilización de laca de uñas o la presencia de acropaquia son factores que pueden alterar la precisión de la medición.
Bibliografía 5. Diagnóstico
23. Henry TS, Kirsch J, Kanne JP, Chung JH, Donnelly EF, Ginsburg ME, et al. ACR Appropriateness Criteria(R) rib fractures. J Thorac Imaging. 2014;29(6):364-6.
24. Morley EJ, Johnson S, Leibner E, Shahid J. Emergency department evaluation and management of blunt chest and lung trauma (Trauma CME). Emerg Med Pract. 2016;18(6):1-20.
25. Rossen B, Laursen NO, Just S. Chest radiography after minor chest trauma. Acta Radiol. 1987;28(1):53-4.
26. Rodriguez RM, Hendey GW, Marek G, Dery RA, Bjoring A. A pilot study to derive clinical variables for selective chest radiography in blunt trauma patients. Ann Emerg Med. 2006;47(5):415-8.
27. Rodriguez RM, Hendey GW, Mower W, Kea B, Fortman J, Merchant G, et al. Derivation of a decision instrument for selective chest radiography in blunt trauma. J Trauma. 2011;71(3):549-53.
28. Rodriguez RM, Anglin D, Langdorf MI, Baumann BM, Hendey GW, Bradley RN, et al. NEXU S chest: validation of a decision instrument for selective chest imaging in blunt trauma. JAMA Surg. 2013;148(10):940-6.
29. Raja AS, Lanning J, Gower A, Langdorf MI, Nishijima DK, Baumann BM, et al. Prevalence of Chest Injury With the Presence of NEXUS Chest Criteria: Data to Inform Shared Decision making About Imaging Use. Ann Emerg Med. 2016;68(2):222-6.
30. Asgarzadeh S, Feizi B, Sarabandi F, Asgarzadeh M. Thoracic injury rule out criteria in prediction of traumatic intra-thoracic injuries; a validation study. Emerg (Tehran). 2017;5(1):e27
31. Myint KS, French S, Williams-Johnson J, Williams E, Johnson P, Reid MO, et al. Role of routine chest radiographs in the evaluation of patients with stable blunt chest trauma--a prospective analysis. West Indian Med J. 2012;61(1):64-72.
32. (Paydar S, Johari HG, Ghaffarpasand F, Shahidian D, Dehbozorgi A, Ziaeian B, et al. The role of routine chest radiography in initial evaluation of stable blunt trauma patients. Am J Emerg Med. 2012;30(1):1-4.
33. Sears BW, Luchette FA, Esposito TJ, Dickson EL, Grant M, Santaniello JM, et al. Old fashion clinical judgment in the era of protocols: is mandatory chest X-ray necessary in injured patients? J Trauma. 2005;59(2):324-30.
34. Bokhari F, Brakenridge S, Nagy K, Roberts R, Smith R, Joseph K, et al. Prospective evaluation of the sensitivity of physical examination in chest trauma. J Trauma. 2002;53(6):1135-8.
35. Dubinsky I, Low A. Non-life-threatening blunt chest trauma: appropriate investigation and treatment. Am J Emerg Med. 1997;15(3):240-3.
36. Dunlop MG, Beattie TF, Preston PG, Steedman DJ. Clinical assessment and radiograph following blunt chest trauma. Arch Emerg Med. 1989;6(2):125-7.
37. Nejati A, Khalaj S, Azizkhani R, Shahryarian S, Kolahdouzan M, Hossein MS. Evaluating validity of clinical criteria for requesting chest X-rays in trauma patients referred to emergency room. Adv Biomed Res. 2012;1:22.
38. Forouzanfar MM, Safari S, Niazazari M, Baratloo A, Hashemi B, Hatamabadi HR, et al. Clinical decision rule to prevent unnecessary chest X-ray in patients with blunt multiple traumas. Emerg Med Australas. 2014;26(6):561-6.
39. Calderon G, Perez D, Fortman J, Kea B, Rodriguez RM. Provider perceptions concerning use of chest x-ray studies in adult blunt trauma assessments. J Emerg Med. 2012;43(4):568-74.
40. Henry TS, Donnelly EF, Boiselle PM, Crabtree TD, Iannettoni MD, Johnson GB, et al. ACR Appropriateness Criteria((R)) Rib Fractures. J Am Coll Radiol. 2019;16(5S):S227-S234.
41. De Luca SA, Rhea JT, O’Malley TO. Radiographic evaluation of rib fractures. AJR Am J Roentgenol. 1982;138(1):91-2.
42. Danher J, Eyes BE, Kumar K. Oblique rib views after blunt chest trauma: An unnecessary routine? BMJ. 1984;289(6454):1271.
43. Hoffstetter P, Dornia C, Schafer S, Wagner M, Dendl LM, Stroszczynski C, et al. Diagnostic significance of rib series in minor thorax trauma compared to plain chest film and computed tomography. J Trauma Manag Outcomes. 2014;8:10.
44. Hoffstetter P, Dornia C, Wagner M, Al Suwaidi MH, Niessen C, Dendl LM, et al. Clinical significance of conventional rib series in patients with minor thoracic trauma. Rofo. 2014;186(9):876-80.
45. Verma SM, Hawkins HH, Colglazier S, Kraemer LA, Wiot JF. The clinical utility of rib detail films in the evaluation of trauma. Emergency Radiology. 1995;2(5):264-6.
46. Davis S, Affatato A. Blunt chest trauma: utility of radiological evaluation and effect on treatment patterns. Am J Emerg Med. 2006;24(4):482-6.
47. Sano A. Rib Radiography versus Chest Computed Tomography in the Diagnosis of Rib Fractures. Thorac Cardiovasc Surg. 2018;66(8):693-6.
48. Tack D, Louage F, Van MA, Howarth N, Gevenois PA. Radiation protection: Factors influencing compliance to referral guidelines in minor chest trauma. Eur Radiol. 2018;28(4):1420-6.
49. Casey R, Emde K. Displaced fractured sternum following blunt chest trauma. JEN: Journal of Emergency Nursing. 2008;34(1):83-5.
50. Lee WS, Kim YH, Chee HK, Lee SA. Ultrasonographic evaluation of costal cartilage fractures unnoticed by the conventional radiographic study and multidetector computed tomography. Eur J Trauma Emerg Surg. 2012;38(1):37-42.
51. Perez MR, Rodriguez RM, Baumann BM, Langdorf MI, Anglin D, Bradley RN, et al. Sternal fracture in the age of pan-scan. Injury. 2015;46(7):1324-7.
52. Sarquis G, Velez SE, Suizer A, Reche F. [Diagnostic and therapeutic options for traumatic sternal fractures]. Rev Fac Cien Med Univ Nac Cordoba. 2003;60(1):13-8.
53. Sadaba JR, Oswal D, Munsch CM. Management of isolated sternal fractures: determining the risk of blunt cardiac injury. Ann R Coll Surg Engl. 2000;82(3):162-6.
54. Kouritas VK, Zisis C, Vahlas K, Roussakis AG, Bellenis I. Isolated sternal fractures treated on an outpatient basis. Am J Emerg Med. 2013;31(1):227-30.
55. Buckman R, Trooskin SZ, Flancbaum L, Chandler J. The significance of stable patients with sternal fractures. Surg Gynecol Obstet. 1987;164(3):261-5.
56. Bar I, Friedman T, Rudis E, Shargal Y, Friedman M, Elami A. Isolated sternal fracture--a benign condition? Isr Med Assoc J. 2003;5(2):105-6.
57. Huggett JM, Roszler MH. CT findings of sternal fracture. Injury. 1998;29(8):623-6.
58. Kim EY, Yang HJ, Sung YM, Hwang KH, Kim JH, Kim HS. Sternal fracture in the emergency department: diagnostic value of multidetector CT with sagittal and coronal reconstruction images. Eur J Radiol. 2012;81(5):e708-e711.
59. You JS, Chung YE, Kim D, Park S, Chung SP. Role of sonography in the emergency room to diagnose sternal fractures. J Clin Ultrasound. 2010;38(3):135-7.
60. Engin G, Yekeler E, Guloglu R, Acunas B, Acunas G. US versus conventional radiography in the diagnosis of sternal fractures. Acta Radiol. 2000;41(3):296-9.
61. Staub LJ, Biscaro RRM, Kaszubowski E, Maurici R. Chest ultrasonography for the emergency diagnosis of traumatic pneumothorax and haemothorax: A systematic review and meta-analysis. Injury. 2018;49(3):457-66.
62. Ebrahimi A, Yousefifard M, Mohammad KH, Rasouli HR, Asady H, Moghadas JA, et al. Diagnostic Accuracy of Chest Ultrasonography versus Chest Radiography for Identification of Pneumothorax: A Systematic Review and Meta-Analysis. Tanaffos. 2014;13(4):29-40.
63. Alrajab S, Youssef AM, Akkus NI, Caldito G. Pleural ultrasonography versus chest radiography for the diagnosis of pneumothorax: review of the literature and meta-analysis. Crit Care. 2013;17(5):R208.
64. Wilkerson RG, Stone MB. Sensitivity of bedside ultrasound and supine anteroposterior chest radiographs for the identification of pneumothorax after blunt trauma. Acad Emerg Med. 2010;17(1):11-7.
65. Rahimi-Movaghar V, Yousefifard M, Ghelichkhani P, Baikpour M, Tafakhori A, Asady H, et al. Application of ultrasonography and radiography in detection of hemothorax; a systematic review and meta-analysis. Emerg (Tehran). 2016;4(3):116-26.
66. Hosseini M, Ghelichkhani P, Baikpour M, Tafakhori A, Asady H, Ghanbari MJH, et al. Diagnostic accuracy of ultrasonography and radiography in detection of pulmonary contusion; a systematic review and meta-analysis. Emerg (Tehran). 2015;3(4):127-36.
67. Racine S, Drake D. BET 3: Bedside ultrasound for the diagnosis of sternal fracture. Emerg Med J. 2015;32(12):971-2.
68. Lalande E, Wylie K. Towards evidence-based emergency medicine: best BETs from the Manchester Royal Infirmary. BET 1: Ultrasound in the diagnosis of rib fractures. Emerg Med. J 2014;31(2):169-70.
69. Blaivas M, Lyon M, Duggal S. A prospective comparison of supine chest radiography and bedside ultrasound for the diagnosis of traumatic pneumothorax. Acad Emerg Med. 2005;12(9):844-9.
70. Soldati G, Testa A, Pignataro G, Portale G, Biasucci DG, Leone A, et al. The ultrasonographic deep sulcus sign in traumatic pneumothorax. Ultrasound Med Biol. 2006;32(8):1157-63.
71. Soldati G, Testa A, Sher S, Pignataro G, La SM, Silveri NG. Occult traumatic pneumothorax: diagnostic accuracy of lung ultrasonography in the emergency department. Chest. 2008;133(1):204-11.
72. Zhang M, Liu ZH, Yang JX, Gan JX, Xu SW, You XD, et al. Rapid detection of pneumothorax by ultrasonography in patients with multiple trauma. Crit Care. 2006;10(4):R112.
73. Chan KK, Joo DA, Mcrae AD, Takwoingi Y, Premji ZA, Lang E, et al. Chest ultrasonography versus supine chest radiography for diagnosis of pneumothorax in trauma patients in the emergency department. Cochrane Database Syst Rev. 2018;2018(5):CD013031.
74. Stengel D, Leisterer J, Ferrada P, Ekkernkamp A, Mutze S, Hoenning A. Point-of-care ultrasonography for diagnosing thoracoabdominal injuries in patients with blunt trauma. Cochrane Database Syst Rev. 2018 Dec 12;12:CD012669.
75. Battle C, Hayward S, Eggert S, Evans PA. Comparison of the use of lung ultrasound and chest radiography in the diagnosis of rib fractures: a systematic review. Emerg Med J. 2019;36(3):185-90.
76. Kirkpatrick AW, Sirois M, Laupland KB, Liu D, Rowan K, Ball CG, et al. Hand-held thoracic sonography for detecting post-traumatic pneumothoraces: the Extended Focused Assessment with Sonography for Trauma (EFAST). J Trauma. 2004;57(2):288-95.
77. Matsushima K, Frankel HL. Beyond focused assessment with sonography for trauma: ultrasound creep in the trauma resuscitation area and beyond. Curr Opin Crit Care. 2011;17(6):606-12.
78. Brooks A, Davies B, Smethhurst M, Connolly J. Emergency ultrasound in the acute assessment of haemothorax. Emerg Med J. 2004;21(1):44-6.
79. Chung JH, Cox CW, Mohammed TL, Kirsch J, Brown K, Dyer DS, et al. ACR appropriateness criteria blunt chest trauma. J Am Coll Radiol. 2014;11(4):345-51.
80. Brink M, Deunk J, Dekker HM, Kool DR, Edwards MJ, van Vugt AB, et al. Added value of routine chest MDCT after blunt trauma: evaluation of additional findings and impact on patient management. AJR Am J Roentgenol. 2008;190(6):1591-8.
81. Payrastre J, Upadhye S, Worster A, Lin D, Kahnamoui K, Patterson H, et al. The SCRAP Rule: The derivation and internal validation of a clinical decision rule for computed tomography of the chest in blunt thoracic trauma. CJEM. 2012;14(6):344-53.
82. Rodriguez RM, Langdorf MI, Nishijima D, Baumann BM, Hendey GW, Medak AJ, et al. Derivation and validation of two decision instruments for selective chest CT in blunt trauma: a multicenter prospective observational study (NEXUS Chest CT). PLoS Med. 2015;12(10):e1001883.
83. Raja AS, Mower WR, Nishijima DK, Hendey GW, Baumann BM, Medak AJ, et al. Prevalence and Diagnostic Performance of Isolated and Combined NEXUS Chest CT Decision Criteria. Acad Emerg Med. 2016;23(8):863-9.
84. Lavingia KS, Collins JN, Soult MC, Terzian WH, Weireter LJ, Britt LD. Torso Computed Tomography Can Be Bypassed after Thorough Trauma Bay Examination of Patients Who Fall from Standing. Am Surg. 2015;81(8):798-801.
85. Corbacioglu SK, Er E, Aslan S, Seviner M, Aksel G, Dogan NO, et al. The significance of routine thoracic computed tomography in patients with blunt chest trauma. Injury. 2015;46(5):849-53.
86. Chardoli M, Hasan-Ghaliaee T, Akbari H, Rahimi-Movaghar V. Accuracy of chest radiography versus chest computed tomography in hemodynamically stable patients with blunt chest trauma. Chin J Traumatol. 2013;16(6):351-4.
87. Kaiser ML, Whealon MD, Barrios C, Jr., Dobson SC, Malinoski DJ, Dolich MO, et al. Risk factors for traumatic injury findings on thoracic computed tomography among patients with blunt trauma having a normal chest radiograph. Arch Surg. 2011;146(4):459-63.
88. Kea B, Gamarallage R, Vairamuthu H, Fortman J, Lunney K, Hendey GW, et al. What is the clinical significance of chest CT when the chest x-ray result is normal in patients with blunt trauma? Am J Emerg Med. 2013;31(8):1268-73.
89. Barrios C, Malinoski D, Dolich M, Lekawa M, Hoyt D, Cinat M. Utility of thoracic computed tomography after blunt trauma: when is chest radiograph enough? Am Surg. 2009;75(10):966-9.
90. Lopes JA, Frankel HL, Bokhari SJ, Bank M, Tandon M, Rabinovici R. The trauma bay chest radiograph in stable blunt-trauma patients: do we really need it? Am Surg. 2006;72(1):31-4. 91. Sawa J, Green RS, Thoma B, Erdogan M, Davis PJ. Risk factors for adverse outcomes in older adults with blunt chest trauma: A systematic review. CJEM. 2017;11;1-9.
92. Battle CE, Hutchings H, Evans PA. Risk factors that predict mortality in patients with blunt chest wall trauma: a systematic review and meta-analysis. Injury. 2012;43(1):8-17.
93. Flagel BT, Luchette FA, Reed RL, Esposito TJ, Davis KA, Santaniello JM, et al. Half-a-dozen ribs: the breakpoint for mortality. Surgery. 2005;138(4):717-23.
94. Lien YC, Chen CH, Lin HC. Risk factors for 24-hour mortality after traumatic rib fractures owing to motor vehicle accidents: a nationwide population-based study. Ann Thorac Surg. 2009;88(4):1124-30.
95. Liman ST, Kuzucu A, Tastepe AI, Ulasan GN, Topcu S. Chest injury due to blunt trauma. Eur J Cardiothorac Surg. 2003;23(3):374-8.
96. Lee RB, Bass SM, Morris JA, Jr., MacKenzie EJ. Three or more rib fractures as an indicator for transfer to a Level I trauma center: a population-based study. J Trauma. 1990;30(6):689-94.
97. Manay P, Satoskar RR, Karthik V, Prajapati RP. Studying Morbidity and Predicting Mortality in Patients with Blunt Chest Trauma using a Novel Clinical Score. J Emerg Trauma Shock. 2017;10(3):128-33.
98. Whitson BA, McGonigal MD, Anderson CP, Dries DJ. Increasing numbers of rib fractures do not worsen outcome: an analysis of the national trauma data bank. Am Surg. 2013;79(2):140-50.
99. Avila Martinez RJ, Hernandez VA, Marron FC, Hermoso AF, Martinez S, I, Mariscal de AA, et al. Evolution and complications of chest trauma. Arch Bronconeumol. 2013;49(5):177-80.
100. Freixinet J, Beltrán J, Miguel Rodríguez P, Juliá G, Hussein M, Gil R, et al. Indicadores de gravedad en los traumatismos torácicos. Arch Bronconeumol. 2008;44(5):257-62.
101. Murphy CE, Raja AS, Baumann BM, Medak AJ, Langdorf MI, Nishijima DK, et al. Rib Fracture Diagnosis in the Panscan Era. Ann Emerg Med. 2017;70(6):904-9.
102. Chapman BC, Herbert B, Rodil M, Salotto J, Stovall RT, Biffl W, et al. RibScore: A novel radiographic score based on fracture pattern that predicts pneumonia, respiratory failure, and tracheostomy. J Trauma Acute Care Surg. 2016;80(1):95-101.
103. Tsai YM, Lin KH, Huang TW, Chen CY, Hong ZJ, Hsu SD. Outcomes of patients with blunt chest trauma encountered at emergency department and possible risk factors affecting mortality. Journal of Medical Sciences (Taiwan). 2017;37(3):97-101.
104. Ho SW, Teng YH, Yang SF, Yeh HW, Wang YH, Chou MC, et al. Risk of pneumonia in patients with isolated minor rib fractures: a nationwide cohort study. BMJ Open. 2017;13;7(1):e013029.
105. Chauny JM, Emond M, Plourde M, Guimont C, Le SN, Vanier L, et al. Patients with rib fractures do not develop delayed pneumonia: a prospective, multicenter cohort study of minor thoracic injury. Ann Emerg Med. 2012;60(6):726-31.
106. Battle CE, Hutchings HF, James KF, Evans PA. The risk factors for the development of complications during the recovery phase following blunt chest wall trauma: a retrospective study. Injury. 2013;44(9):1171-6.
107. Chien CY, Chen YH, Han ST, Blaney GN, Huang TS, Chen KF. The number of displaced rib fractures is more predictive for complications in chest trauma patients. Scand J Trauma Resusc Emerg Med. 2017;25(1):19.
108. Dhillon TS, Galante JM, Salcedo ES, Utter GH. Characteristics of chest wall injuries that predict postrecovery pulmonary symptoms: A secondary analysis of data from a randomized trial. J Trauma Acute Care Surg. 2015;79(2):179-86.
109. Battle C, Hutchings H, Lovett S, Bouamra O, Jones S, Sen A, et al. Predicting outcomes after blunt chest wall trauma: development and external validation of a new prognostic model. Crit Care. 2014;18(3):R98.
110. James MK, Lee SW, Minneman JA, Moore MD, Klein TR, Robitsek RJ, et al. Variability in CT imaging of blunt trauma among ED physicians, surgical residents, and trauma surgeons. J Surg Res. 2017;213:6-15.
111. Garcia de Pereda de Blas, Carreras AM, Carbajo AS, Arana-Arri E. Is it adequate to carry out a chest-CT in patients with mild-moderate chest trauma? Radiologia. 2018;;60(4):347-50.
112. Safari S, Radfar F, Baratloo A. Thoracic injury rule out criteria and NEXUS chest in predicting the risk of traumatic intra-thoracic injuries: A diagnostic accuracy study. Injury. 2018;49(5):959-62.
113. Hansen CK, Strayer RJ, Shy BD, Kessler S, Givre S, Shah KH. Prevalence of negative CT scans in a level one trauma center. Eur J Trauma Emerg Surg. 2018;44(1):29-33.
114. Singleton JM, Bilello LA, Canham LS, Levenson RB, Lopez GJ, Tadiri SP, et al. Chest computed tomography imaging utility for radiographically occult rib fractures in elderly fall-injured patients. Journal of Trauma and Acute Care Surgery. 2019;86(5):838-43.
115. Faulkner A, Reidy M, Scicluna G, Love GJ, Joss J. Blood tests: One too many? Evaluating blood requesting guidance developed for acute patients admitted to trauma and orthopaedic units. Injury. 2016;47(3):685-90.
116. Alazzawi S, De Rover WB, Leary T, Hallam PJ. Patients undergoing blood tests before minor/moderate trauma surgery: a retrospective review. JRSM Short Rep. 2012;3(6):39.
117. Jacobs IA, Kelly K, Valenziano C, Chevinsky AH, Pawar J, Jones C. Cost savings associated with changes in routine laboratory tests ordered for victims of trauma. Am Surg. 2000;66(6):579-84.
118. Chu UB, Clevenger FW, Imami ER, Lampard SD, Frykberg ER, Tepas JJ, III. The impact of selective laboratory evaluation on utilization of laboratory resources and patient care in a level-I trauma center. Am J Surg. 1996;172(5):558-62.
119. Tasse JL, Janzen ML, Ahmed NA, Chung RS. Screening laboratory and radiology panels for trauma patients have low utility and are not cost effective. J Trauma. 2008;65(5):1114-6.
120. Ikegami Y, Suzuki T, Nemoto C, Tsukada Y, Tase C. Usefulness of initial diagnostic tests carried out in the emergency department for blunt trauma. Acute Med Surg. 2014;1(2):70-5.
121. Branco BC, Inaba K, Doughty R, Brooks J, Barmparas G, Shulman I, et al. The increasing burden of phlebotomy in the development of anaemia and need for blood transfusion amongst trauma patients. Injury. 2012;43(1):78-83.
122. National Guideline Centre (UK). Preoperative Tests (Update): Routine Preoperative Tests for Elective Surgery. London: National Institute for Health and Care Excellence (UK). 2016.
123. Martin SK, Cifu AS. Routine Preoperative Laboratory Tests for Elective Surgery. JAMA. 2017;318(6):567-8.
124. De HS, Staender S, Fritsch G, Hinkelbein J, Afshari A, Bettelli G, et al. Pre-operative evaluation of adults undergoing elective noncardiac surgery: Updated guideline from the European Society of Anaesthesiology. Eur J Anaesthesiol. 2018;35(6):407-65.
125. Bhattacharya B, Fieber J, Schuster K, Davis K, Maung A. “Occult” rib fractures diagnosed on computed tomography scan only are still a risk factor for solid organ injury. J Emerg Trauma Shock. 2015;8(3):140-3.
126. Rostas JW, Lively TB, Brevard SB, Simmons JD, Frotan MA, Gonzalez RP. Rib fractures and their association With solid organ injury: higher rib fractures have greater significance for solid organ injury screening. Am J Surg. 2017;213(4):791-7.
127. Al-Hassani A, Abdulrahman H, Afifi I, Almadani A, Al-Den A, Al-Kuwari A, et al. Rib fracture patterns predict thoracic chest wall and abdominal solid organ injury. Am Surg. 2010;76(8):888-91.
128. Clancy K, Velopulos C, Bilaniuk JW, Collier B, Crowley W, Kurek S, et al. Screening for blunt cardiac injury: an Eastern Association for the Surgery of Trauma practice management guideline. J Trauma Acute Care Surg. 2012;73(5 Suppl 4):S301-S306.
129. Guild CS, deShazo M, Geraci SA. Negative predictive value of cardiac troponin for predicting adverse cardiac events following blunt chest trauma. South Med J. 2014;107(1):52-6.
130. Wiener Y, Achildiev B, Karni T, Halevi A. Echocardiogram in sternal fracture. Am J Emerg Med. 2001;19(5):403-5.
131. Athanassiadi K, Gerazounis M, Moustardas M, Metaxas E. Sternal fractures: retrospective analysis of 100 cases. World J Surg. 2002;26(10):1243-6.
132. Rashid MA, Ortenwall P, Wikstrom T. Cardiovascular injuries associated with sternal fractures. Eur J Surg. 2001;167(4):243-8.
133. Chiu WC, D’Amelio LF, Hammond JS. Sternal fractures in blunt chest trauma: a practical algorithm for management. Am J Emerg Med. 1997;15(3):252-5.
134. Fulda GJ, Giberson F, Hailstone D, Law A, Stillabower M. An evaluation of serum troponin T and signal-averaged electrocardiography in predicting electrocardiographic abnormalities after blunt chest trauma. J Trauma. 1997;43(2):304-10.
135. Garcia-Fernandez MA, Lopez-Perez JM, Perez-Castellano N, Quero LF, Virgos-Lamela A, Otero-Ferreiro A, et al. Role of transesophageal echocardiography in the assessment of patients with blunt chest trauma: correlation of echocardiographic findings with the electrocardiogram and creatine kinase monoclonal antibody measurements. Am Heart J. 1998;135(3):476-81.
136. Salim A, Velmahos GC, Jindal A, Chan L, Vassiliu P, Belzberg H, et al. Clinically significant blunt cardiac trauma: role of serum troponin levels combined with electrocardiographic findings. J Trauma. 2001;50(2):237-43.
137. Velmahos GC, Karaiskakis M, Salim A, Toutouzas KG, Murray J, Asensio J, et al. Normal electrocardiography and serum troponin I levels preclude the presence of clinically significant blunt cardiac injury. J Trauma. 2003;54(1):45-50.
138. Nagy KK, Krosner SM, Roberts RR, Joseph KT, Smith RF, Barrett J. Determining which patients require evaluation for blunt cardiac injury following blunt chest trauma. World J Surg. 2001;25(1):108-11.
139. Swaanenburg JC, Klaase JM, DeJongste MJ, Zimmerman KW, ten Duis HJ. Troponin I, troponin T, CKMB-activity and CKMB-mass as markers for the detection of myocardial contusion in patients who experienced blunt trauma. Clin Chim Acta. 1998;272(2):171-81.
140. Bertinchant JP, Polge A, Mohty D, Nguyen-Ngoc-Lam R, Estorc J, Cohendy R, et al. Evaluation of incidence, clinical significance, and prognostic value of circulating cardiac troponin I and T elevation in hemodynamically stable patients with suspected myocardial contusion after blunt chest trauma. J Trauma. 2000;48(5):924-31.
141. Rajan GP, Zellweger R. Cardiac troponin I as a predictor of arrhythmia and ventricular dysfunction in trauma patients with myocardial contusion. J Trauma. 2004;57(4):801-8.
142. Collins JN, Cole FJ, Weireter LJ, Riblet JL, Britt LD. The usefulness of serum troponin levels in evaluating cardiac injury. Am Surg. 2001;67(9):821-5.
143. Pretto JJ, Roebuck T, Beckert L, Hamilton G. Clinical use of pulse oximetry: official guidelines from the Thoracic Society of Australia and New Zealand. Respirology. 2014;19(1):38-46.
144. Jensen LA, Onyskiw JE, Prasad NG. Meta-analysis of arterial oxygen saturation monitoring by pulse oximetry in adults. Heart Lung. 1998;27(6):387-408.
145. Kelly AM, McAlpine R, Kyle E. How accurate are pulse oximeters in patients with acute exacerbations of chronic obstructive airways disease? Respir ed. 2001;95(5):336-40. 202 GUÍAS DE PRÁCTICA CLÍNICA EN EL SNS.
146. Garcia-Gutierrez S, Unzurrunzaga A, Arostegui I, Quintana JM, Pulido E, Gallardo MS, et al. The Use of Pulse Oximetry to Determine Hypoxemia in Acute Exacerbations of COPD. COPD. 2015;12(6):613-20.






