7.1. Modelos de atención a la depresión y principios generales de manejo
7.1.1. El modelo escalonado
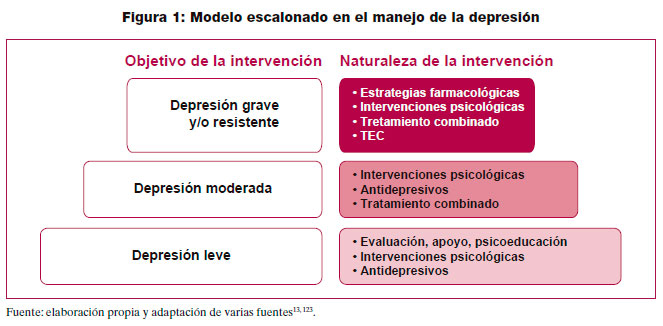
Los modelos escalonados de tratamiento se han desarrollado con el objetivo de maximizar la eficiencia mediante la proporción de las intervenciones menos intensivas según el estado y evolución del paciente. A pesar de que el escalonamiento de las intervenciones según la complejidad y gravedad de las patologías está implícito en general en la atención sanitaria, los sistemas escalonados son un intento de formalizar un continuo en la atención prestada y mejorar la eficiencia13. Se ha propuesto que este modelo es el adecuado para el manejo de la depresión por diferentes razones. Entre las más importantes se han destacado la evidencia de equivalencia de resultados entre intervenciones de diferente intensidad, la promoción del uso eficiente de los recursos y la aceptabilidad de la intensificación de intervenciones según la gravedad tanto por parte de los profesionales como de los pacientes122 . A pesar de que las aproximaciones escalonadas de manejo comparten un planteamiento similar, la implantación y organización de los modelos de atención escalonada depende de las características y asistencia concretas de cada sistema sanitario, pero es un modelo característico de los servicios públicos de salud donde la atención primaria constituye la puerta de entrada, como es en España121. Algunas de las premisas de las que parte este de modelo son la potenciación del trabajo multidisciplinar y la colaboración entre atención primaria y especializada. La atención se estratifica de modo que el primer escalón propuesto es la intervención menos intensiva en atención primaria, y en aquellos casos en los que no se consigue la respuesta adecuada tras intensificar la intervención, el nivel asistencial más apropiado sería el especializado123. Este modelo de tratamiento es habitualmente propuesto por el NICE, y en el caso de la depresión, tanto la guía sobre la depresión en el adulto como la de depresión en enfermedades crónicas han organizado sus recomendaciones de manejo según este modelo13. En España, también se ha propuesto como un modelo de organización de los servicios para el manejo de la depresión123.
7.1.2. La atención colaborativa
Los modelos de atención colaborativa, basados en el Chronic Care Model, han sido aplicados para mejorar el manejo de la depresión en atención primaria, observándose su efectividad a la hora de mejorar el proceso asistencial y los resultados clínicos127. Este modelo de atención potencia la intervención de las care manager, que generalmente son enfermeras, cuya función principal es mejorar el bienestar y la calidad de vida de las personas con depresión, planificando cuidados enfermeros en función de sus necesidades y realizar funciones de integración y coordinación de las intervenciones de los diferentes profesionales (médicos de familia, psiquiatras, psicólogos, trabajadores sociales y otros profesionales de la salud) para vertebrar una mejor asistencia sanitaria y calidad de cuidados al paciente.
- Inclusión de cambios organizativos y asistenciales en el sistema de prestación de servicios de salud.
- Desarrollo del rol de la enfermera, como gestora de casos y coordinadora de la atención.
- Continuidad del cuidado a través del seguimiento clínico del paciente.
Resumen de la evidencia
|
1+
|
A pesar de que los modelos de atención escalonada han sido recomendados por diferentes organizaciones, no existen muchos estudios centrados específicamente en evaluar los resultados de su adopción en el manejo de la depresión. En general, la evidencia de su efectividad es limitada, aunque su inclusión como parte de modelos más complejos de atención colaborativa se ha asociado con mejores resultados en salud y de prescripción de tratamientos13,121. |
|
1+
|
La mayoría de las revisiones sistemáticas sobre atención colaborativa han puesto de manifiesto que estos modelos son más efectivos que la atención habitual y señalan mayor eficiencia cuando se combina con la atención escalonada. Sin embargo es necesario tener en cuenta que existe una gran diversidad en los estudios en los modelos específicos evaluados, el número y tipo de intervenciones y los agentes implicados, por lo que continúa siendo difícil extraer conclusiones definitivas121,128. |
|
1+
|
En España, el modelo INDI (Interventions for Depression Improvement, programa multicomponente basado en los principios generales del modelo de atención al paciente crónico) ha sido evaluado mediante un ensayo controlado aleatorizado en el que se compararon sus resultados frente a la atención habitual de los pacientes con depresión observándose unas tasas de respuesta y de remisión de la depresión un 15-20% más altas en los pacientes atendidos según el modelo INDI desde los 3 meses y durante 1 año de seguimiento124. Este modelo también ha mostrado un favorable cociente coste-utilidad, con mejores resultados incrementales para la intervención, tanto de utilidad como de efectividad clínica129. |
Recomendaciones
|
Modelos de atención
|
|
|
B
|
Se recomienda que el manejo de la depresión en el adulto se realice siguiendo un modelo de atención escalonada y de colaboración entre atención primaria y salud mental, de forma que las intervenciones y tratamientos se vayan intensificando según el estado y la evolución del paciente. |
|
Recomendaciones generales de tratamiento
|
|
|
√
|
El tratamiento de la depresión en el adulto debería ser integral y abarcar todas las intervenciones psicoterapéuticas, psicosociales y farmacológicas que puedan mejorar el bienestar y la capacidad funcional. |
|
√
|
El manejo de la depresión debería incluir psicoeducación, apoyo individual y familiar, coordinación con otros profesionales, atención a las comorbilidades y monitorización regular del estado mental y físico. |
|
√
|
La selección inicial de la modalidad y el ámbito de tratamiento se debería realizar en función de los hallazgos clínicos y de otros factores, como la historia previa, la disponibilidad de los tratamientos, la preferencia de los pacientes y la capacidad de apoyo y contención del entorno. |
|
DGPC
|
Se recomienda establecer un plan de seguimiento estructurado del paciente. La frecuencia de la evaluación y monitorización de síntomas debería realizarse en función de la gravedad del cuadro, comorbilidad asociada, cooperación con el tratamiento, apoyo social y frecuencia y gravedad de los efectos secundarios del tratamiento prescrito. |
|
Q
|
Se recomienda que el paciente y, contando con su consentimiento, también sus familiares y allegados, tengan un papel activo en la toma de decisiones sobre el tratamiento y el desarrollo del plan de cuidados. |
|
Q
|
Se recomienda ofrecer apoyo al paciente y a su familia para el desarrollo de estrategias de afrontamiento. Se informará sobre la existencia de asociaciones para pacientes que puedan ser de ayuda y los recursos con los que pueda contar. |
|
DGPC
|
Se recomienda apoyar la información verbal con documentos escritos cuando sea posible. |
- La existencia de factores comunes a todos los tratamientos psicológicos (variables del terapeuta y del paciente, relación terapéutica), que si bien son factores esenciales de las psicoterapias, afectan potencialmente a los resultados obtenidos tanto en el grupo experimental como en el grupo control.
- Los tratamientos psicológicos no siempre están estandarizados por lo que pueden existir diferencias individuales y pequeñas variaciones que influyen en el resultado. No obstante, cada vez hay más manuales estandarizados de tratamiento.
- En la mayoría de los estudios el grupo de comparación sigue el tratamiento habitual o atención convencional, pero no se define de forma operativa, lo que dificulta la comparación entre grupos.
Además de las dificultades anteriormente citadas, un problema común a la investigación sobre los diferentes tratamientos en la depresión es que las medidas de resultados suelen basarse en mejoras en determinadas escalas, no siempre las mismas, y en general se incluyen poco medidas de resultados que incluyan la funcionalidad del paciente.
7.2.1. Terapias cognitivo-conductuales
La terapia cognitiva, desarrollada originalmente por A. T. Beck y formalizada a finales de los años 70 para ser aplicada en la depresión90, ha resultado ser la modalidad de terapia psicológica más frecuentemente estudiada en este trastorno134. La intervención se centra en la modificación de conductas disfuncionales, pensamientos negativos distorsionados asociados a situaciones específicas y actitudes desadaptativas relacionadas con la depresión. El terapeuta adopta un estilo educativo, buscando la colaboración del paciente, de manera que pueda aprender a reconocer sus patrones de pensamiento negativo y reevaluarlo. Este enfoque requiere que el paciente practique sus nuevas habilidades entre sesiones mediante tareas para casa y ensaye nuevas conductas. Habitualmente la terapia cognitiva incluye más o menos técnicas conductuales; de ahí la denominación de terapia cognitivo-conductual (TCC). Por otra parte, bajo la denominación de TCC existe una gama diferente de intervenciones que comparten la asunción teórica básica de que la mayor parte de la conducta humana es aprendida y que la actividad cognitiva determina el comportamiento. La TCC adopta un formato estructurado, es limitada en el tiempo y se basa en el modelo cognitivo-conductual de los trastornos afectivos. Ha sido evaluada en una diversidad de contextos (atención primaria, especializada, pacientes hospitalizados), comparada principalmente con tratamiento farmacológico y en diferentes muestras de pacientes135. La duración más frecuente oscila entre 15-20 sesiones de 50 minutos y de frecuencia aproximadamente semanal, aunque también hay estudios que adoptan formatos más breves (entre 6-8 sesiones) y se asume que la duración de la terapia puede prolongarse en caso de mayor gravedad o comorbilidad asociada. La TCC en formato grupal también es empleada en pacientes con depresión mayor. La TCC grupal es altamente estructurada y tiene un fuerte componente psicoeducativo. Suele organizarse en 12 sesiones de dos horas realizadas a lo largo de 8 semanas13. La terapia cognitiva basada en la conciencia plena o mindfulness (Mindfulness-based cognitive therapy, MBCT) es una variante de la TCC en formato grupal, diseñada específicamente para la prevención de recaídas o recurrencias. Se desarrolla en 8 sesiones grupales de frecuencia semanal y dos horas de duración, centradas en la detección y el desarrollo de habilidades para hacer frente a las sensaciones corporales, pensamientos y sentimientos asociados a las recaídas13.
7.2.2. Activación conductual
La activación conductual es una terapia estructurada y breve en la que se emplean diferentes técnicas conductuales encaminadas a lograr que el paciente con depresión aprenda a organizar su vida y cambiar su entorno para recuperar el reforzamiento positivo148,149.
7.2.3. Terapia de solución de problemas
La asociación entre la depresión y el déficit de solución de problemas sociales es ampliamente reconocida. La terapia de solución de problemas (TSP) es una terapia estructurada y limitada en el tiempo que se centra en mejorar las estrategias de afrontamiento y el desarrollo de conductas para enfrentarse a problemas específicos13.
7.2.4 Terapia incluyendo a la pareja
El abordaje psicoterapéutico incluyendo a la pareja es una intervención psicológica que tiene como objetivo ayudar a entender a los participantes la importancia de la interacción con los demás en el desarrollo y mantenimiento de los síntomas y por lo tanto, intenta cambiar la naturaleza de estas interacciones con la finalidad de conseguir relaciones basadas en el apoyo y la reducción del nivel de conflictos13. Aunque no es un tratamiento específicamente desarrollado para el tratamiento de la depresión, algunos autores destacan su indicación en la depresión por la influencia que la pareja puede tener en el inicio, mantenimiento o exacerbación y resolución de un episodio de depresión13.
7.2.5. Terapia interpersonal
La terapia interpersonal fue desarrollada por Klerman y Weissman152 como tratamiento para la depresión, aunque su uso se ha extendido a otros trastornos mentales. Se centra en las relaciones actuales y en los procesos interpersonales y el objetivo es reducir los síntomas a través de la resolución o afrontamiento de áreas problemáticas.
7.2.6. Counselling
El counselling o consejo psicológico fue inicialmente desarrollado por Carl Rogers154, aunque actualmente se ha convertido en un término más genérico que incluye diferentes intervenciones que tienen por objetivo dotar a las personas con capacidades que les permitan explorar, descubrir y buscar formas de bienestar.
7.2.7. Terapia psicodinámica breve
La terapia psicodinámica deriva del modelo psicodinámico/psicoanalítico, donde el paciente y el terapeuta exploran los conflictos actuales y pasados del paciente y se centran en su interpretación y trabajo sobre ellos13,155.
7.2.8. Otras intervenciones psicoterapéuticas
Como parte del abordaje psicoterapéutico de la depresión, se han desarrollado otras intervenciones menos intensivas que requieren una menor frecuencia y duración en la participación de los profesionales, o la implicación de profesionales con menor nivel de especialización. Suelen incluirse en este grupo de intervenciones la terapia cognitivo-conductual computarizada (TCC-C) y la autoayuda guiada13,156. En una directriz publicada por el NHS sobre la mejora del acceso a los tratamientos psicológicos, se agrupan todos estos tratamiento bajo el calificativo de terapias de baja intensidad y las definen como “aquellas que emplean enfoques menos complejos que la psicoterapia, en los que el contacto con los pacientes es más breve y que puede ser llevado a cabo por profesionales con menor grado de especialización, utilizando métodos no tradicionales como el teléfono o internet”157. Según esta definición, la intensidad es definida por las siguientes características: la complejidad de la intervención, la duración del contacto con los profesionales, el nivel de cualificación de los mismos y el formato de la intervención156. Otra definición de intervenciones de baja intensidad destaca su orientación al aumento del volumen de acceso a las mismas158. En esta revisión se incluyen los estudios en los que la TCC-C y la autoayuda guiada se emplean como tratamiento de la depresión o de sus síntomas, si bien la mayor parte de ellos son realizados con muestras de pacientes con depresión leve o con síntomas depresivos según alguna escala (usualmente BDI). Muchos de ellos se han llevado a cabo en el Reino Unido, como respuesta a una recomendación de investigación realizada por el NICE, y con materiales que, hasta donde conocemos, no han sido validados al castellano (por ejemplo el Programa Beating the Blues, que consiste en 8 sesiones de 50 minutos semanales de TCC-C).
Resumen de la evidencia
|
1+
|
En una revisión sistemática que evaluó todos aquellos ensayos clínicos aleatorizados que compararon una intervención psicoterapéutica (terapia cognitivo-conductual, terapia de resolución de problemas, terapia psicodinámica, entrenamiento en habilidades sociales, counselling, terapia interpersonal y activación conductual) con un grupo control (lista de espera, atención habitual o placebo) en adultos con depresión mayor, se encontró que las psicoterapias fueron superiores a estar en lista de espera, con un tamaño de efecto moderado-alto. Sin embargo, los resultados no mostraron diferencias al comparar las diferentes intervenciones entre sí, ni entre formatos individuales y grupales133. |
|
Terapias cognitivo-conductuales
|
|
|
1+
|
La TCC obtuvo puntuaciones similares al tratamiento farmacológico antidepresivo (fundamentalmente ISRS y ADT) en las escalas HRSD y BDI, tanto al finalizar el tratamiento como al mes de seguimiento, mientras que a los 12 meses de tratamiento se observó cierta superioridad de la TCC13. |
|
1+
|
La TCC presentó menor riesgo de discontinuación, en términos de abandono precoz del tratamiento, que el tratamiento antidepresivo farmacológico, y menores tasas de recaídas al año de seguimiento13. |
|
3
|
No se encontraron diferencias entre la TCC y la terapia interpersonal o la activación conductual en las escalas HRSD y BDI al final del tratamiento. No se pueden establecer conclusiones definitivas sobre la eficacia relativa de la TCC frente a la terapia psicodinámica breve13. |
|
3
|
En comparación con pacientes en lista de espera, la TCC fue más efectiva tanto en escalas autoinformadas como heteroinformadas13. |
|
1+
|
El tratamiento combinado de TCC + antidepresivos tiene menor riesgo de discontinuación que los antidepresivos solos y reduce de forma significativa la puntuación en escalas tanto autoaplicadas como heteroaplicadas. Sin embargo, no se observó ningún beneficio en añadir tratamiento antidepresivo a la TCC al finalizar el tratamiento o al mes. La evidencia de eficacia del tratamiento combinado a 6 y 12 meses es limitada13. |
|
1+
|
Un metanálisis y análisis secuencial de ensayos clínicos aleatorizados comparó los efectos de la TCC frente al tratamiento habitual en la depresión mayor y mostró que la TCC redujo significativamente los síntomas depresivos medidos con la escala de Hamilton, pero no con el BDI138. |
|
1+
|
Otro metanálisis y análisis secuencial de ensayos clínicos aleatorizados comparó los efectos de la TCC frente a la no intervención en el trastorno depresivo mayor y mostró que la TCC redujo significativamente los síntomas depresivos medidos con la escala de Hamilton, aunque el análisis secuencial no pudo confirmar estos resultados. Con la escala BDI se observó una reducción significativa en las puntuaciones, confirmando los resultados el análisis secuencial139. |
|
1+
|
Otro metanálisis comparó la TCC con la TIP en el tratamiento de la depresión mayor, sin diferencias en la puntuaciones de la escalas de HRSD ni BDI, al finalizar el tratamiento. El análisis secuencial de los ensayos mostró que son necesarios más estudios para confirmar la existencia de un efecto diferencial140. |
|
1+
|
La TCC en formato grupal (programa Coping with Depression Programme), en comparación con estar en lista de espera o tratamiento habitual, redujo significativamente la puntuación de escalas de depresión al final del tratamiento y a los 6 meses de seguimiento13. |
|
1+
|
Un metanálisis observó que la TCC grupal se asoció con una reducción de síntomas de depresión al finalizar el tratamiento (con heterogeneidad significativa) y a los 6 meses, en comparación con el grupo control. Más allá de los 6 meses, la TCC en formato grupal no se asoció con un efecto persistente de reducción de los síntomas. Sin embargo se asoció con una baja tasa de recaídas141. |
|
1+
|
Un ensayo controlado de 10 semanas de duración aleatorizó 368 pacientes con depresión menor, distimia y depresión mayor leve-moderada a recibir sertralina, TCC grupal, autoayuda guiada, sertralina o TCC grupal a elección del paciente o placebo. La eficacia global se midió mediante escalas de depresión, observándose la superioridad de la sertralina frente al placebo y de la TCC grupal frente a la autoayuda guiada142. |
|
1+
|
Un ECA con seguimiento a cinco años encontró que la terapia cognitiva breve en formato grupal en pacientes en remisión tras una variedad de tratamientos, fue más eficaz en la prevención de recaídas que el tratamiento habitual143. |
|
1+
|
El tratamiento combinado de Mindfulness-based cognitive therapy (MBCT) con el tratamiento habitual del médico de atención primaria mostró significativamente menor riesgo de recaídas y mayor riesgo de discontinuación, en comparación con el tratamiento habitual13. |
|
1+
|
La comparación de MBCT con tratamiento antidepresivo farmacológico mostró un efecto entre medio y moderado a la hora de reducir la puntuación de las escalas de depresión al mes y a los 15 meses de seguimiento a favor de la psicoterapia13. |
|
1+
|
En dos ECA, la combinación de MBCT + tratamiento habitual (que permitía fármacos antidepresivos) redujo de forma significativa el porcentaje de recurrencia/ recaída a las 56 semanas, en comparación con el grupo tratamiento habitual144 y los pacientes refirieron menos síntomas depresivos, ansiedad y rumiación e incrementaron sus habilidades de atención plena en comparación con el grupo de sólo tratamiento habitual145. En otro estudio146, continuar con tratamiento farmacológico o sustituirlo por MBCT redujo en un 73% la probabilidad de recaída. Por último, la MBCT fue superior al tratamiento habitual en la reducción de la reactividad al estrés social y que las mejoras en la reactividad emocional estuvieron mediadas por los síntomas depresivos147. |
|
Activación conductual
|
|
|
1+
|
No se observaron diferencias clínicamente relevantes en la puntuación de escalas de depresión, tanto autoaplicadas como heteroaplicadas, entre la activación conductual y la TCC o el placebo, al final del tratamiento13. |
|
1+
|
En comparación con la terapia breve, la activación conductual tiene menor riesgo de discontinuación y frente a la terapia de apoyo, obtuvo mejores resultados en las puntuaciones de la escala BDI al final del tratamiento13. |
|
1+
|
En pacientes con depresión moderada-grave, no se encontraron diferencias significativas entre la activación conductual y el tratamiento antidepresivo en el riesgo de discontinuación, puntuaciones en las escalas de depresión o número de recaídas al año de tratamiento13. |
|
1+
|
La activación conductual fue más eficaz que el tratamiento habitual en atención primaria, tanto en la mejoría de la sintomatología depresiva como en los niveles de funcionalidad laboral y social150. |
|
Solución de problemas
|
|
|
1+
|
La terapia de solución de problemas, en comparación con placebo, redujo significativamente la puntuación de escalas de depresión heteroaplicadas o autoaplicadas. Sin embargo, no se encontraron diferencias significativas cuando se comparó con antidepresivos o cuando la combinación de terapia de solución de problemas se comparó sólo con estos últimos13. |
|
Terapia incluyendo la pareja
|
|
|
1+
|
En comparación con la lista de espera, dos estudios encontraron que la terapia incluyendo a la pareja redujo de forma significativa la puntuación de escalas de depresión autoaplicadas al final del tratamiento13. |
|
1+
|
En comparación con la TCC, dos estudios no observaron diferencias significativas en el riesgo de discontinuación o en las puntuaciones de escalas de depresión al final del tratamiento (BDI o HRSD) o a los 6 meses (BDI). En comparación con la TIP, los resultados no son concluyentes13. |
|
1+
|
En comparación con estar en lista de espera, la terapia incluyendo a la pareja en mujeres con depresión mayor o distimia mejora el distréss psicológico, la carga de la depresión y la implicación en el proceso151. |
|
Terapia interpersonal
|
|
|
1+
|
La guía del NICE incluyó cuatro estudios que compararon la TCC con la TIP sin encontrar diferencias clínicamente relevantes en las puntuaciones de escalas de depresión al final del tratamiento13. |
|
1+
|
Sólo un estudio comparó la TIP con el placebo, observando un menor riesgo de discontinuación y una reducción significativa de las puntuaciones de escalas de depresión heteroaplicadas al finalizar el tratamiento13. |
|
1+
|
En comparación con los cuidados habituales en atención primaria (incluyendo medicación), cuatro estudios mostraron un efecto significativo de la TIP sobre las puntuaciones de escalas de depresión autoaplicadas al final del tratamiento y a los 3 y 9 meses de seguimiento, y sobre escalas heteroaplicadas a los 3 y 9 meses13. |
|
1+
|
Dos estudios que compararon la TIP con el tratamiento antidepresivo farmacológico no encontraron diferencias significativas entre ambos grupos en las escalas BDI y HRSD al final del tratamiento13. |
|
1+
|
En un estudio, la combinación de TIP más antidepresivos disminuyó significativamente las puntuaciones de escalas de depresión heteroaplicadas cuando se comparó con la TIP sola, y en otro, el tratamiento combinado en comparación con sólo antidepresivos mostró un efecto significativo en las puntuaciones de escalas de depresión heteroaplicadas al final del tratamiento13. |
|
1+
|
Un ECA realizado con el objetivo de evaluar el efecto de las preferencias de tratamiento en la eficacia de la TIP y del tratamiento farmacológico (escitalopram) puso de manifiesto que en ambos grupos el grado de preferencia se relaciona con la eficacia del tratamiento153. |
|
Counselling
|
|
|
1+
|
La evidencia sobre counselling es limitada y basada en pacientes con depresión mayor leve-moderada. Un estudio con limitaciones metodológicas comparó la efectividad del counselling con los antidepresivos sin encontrar diferencias significativas13. |
|
1+
|
Otro estudio comparó la combinación del counselling y los cuidados del médico de atención primaria con sólo estos últimos, sin encontrar tampoco diferencias13. |
|
1+
|
La comparación con la TCC se evaluó en un estudio, aunque el pequeño tamaño de la muestra no permite extraer conclusiones definitivas sobre la efectividad relativa de los tratamientos13. |
|
1+
|
Dos estudios compararon dos variantes de la intervención: en el primero, se comparó counselling centrado en el paciente con counselling centrado en las emociones, obteniendo mejores resultados esta última modalidad. En el segundo, se comparó la efectividad del counselling centrado en el paciente vs en el proceso, sin encontrarse diferencias significativas13. |
|
Terapia psicodinámica breve
|
|
|
1+
|
La terapia psicodinámica breve es menos eficaz que los fármacos antidepresivos en reducir las puntuaciones de escalas de depresión heteroaplicadas al final del tratamiento13. |
|
1+
|
En comparación con la activación conductual, la terapia psicodinámica breve presenta un elevado y significativo riesgo de discontinuación, mientras que en comparación con la lista de espera, un estudio mostró un significativo efecto sobre las puntuaciones de escalas de depresión heteroaplicadas y un efecto similar al compararla con la terapia de apoyo13. |
|
1+
|
En pacientes con depresión menor o distimia, añadir terapia psicodinámica al tratamiento antidepresivo reduce significativamente las puntuaciones de escalas de depresión heteroaplicadas a los 24 y 48 meses de seguimiento, en comparación con sólo tratamiento farmacológico13. |
|
1+
|
En pacientes diagnosticados de depresión mayor con o sin trastorno de la personalidad comórbido, la terapia psicodinámica parece ser más eficaz en este último caso, aunque el pequeño tamaño muestral no permite conclusiones firmes13. |
|
Terapia cognitivo-conductual computarizada
|
|
|
1+
|
Existe evidencia de eficacia en la mejoría de síntomas depresivos a corto plazo de la TCC-C en comparación con la TCC grupal, terapia de solución de problemas, tratamiento habitual, psicoeducación, grupo de discusión y lista de espera13,159-161. |
|
1+
|
En un estudio la terapia la TCC-C obtuvo resultados de eficacia similares a la terapia de solución de problemas, aunque ésta obtuvo una mejoría significativamente más rápida161. |
|
1+
|
El tratamiento individualizado, en el que el terapeuta adapta los contenidos, es más eficaz que el tratamiento TCC-C estandarizado, sobre todo en pacientes con mayor gravedad de depresión y presencia de comorbilidad162. |
|
1+
|
En comparación con la lista de espera, tanto la TCC-C con la participación de clínicos como la llevada a cabo por técnicos supervisados obtuvieron una reducción significativa de síntomas de depresión163. |
|
1+
|
En un estudio que comparó la TCC-C con dos formas diferentes de autoayuda basada en la TCC se puso de manifiesto una mejoría significativa tanto en los síntomas de depresión como en ansiedad, aunque no se obtuvieron diferencias significativas entre las diferentes intervenciones164. |
|
Autoayuda guiada
|
|
|
1+
|
La autoayuda guiada es una intervención eficaz para personas con depresión leve o con síntomas subclínicos de depresión, aunque no existe evidencia de su eficacia a largo plazo13. |
|
1+
|
La autoayuda guiada con apoyo individual de corta duración es más eficaz que la de larga duración y no existe evidencia concluyente sobre la autoayuda guiada con apoyo en formato grupal13. |
|
1+
|
En un estudio se sugiere que la eficacia de la autoayuda puede mantenerse con el contacto con los profesionales o prescindiendo del mismo a los 6 meses posttratamiento166. |
|
1+
|
La autoayuda guiada y la relajación unidos al tratamiento habitual de la depresión mejoraron significativamente los síntomas depresivos medidos con la HRSD y las distorsiones cognitivas. No se encontraron diferencias entre ambas intervenciones (tratamiento habitual+autoayuda vs tratamiento habitual+relajación)167. |
|
1+
|
No existe evidencia suficiente sobre el efecto de las intervenciones psicosociales de baja intensidad a largo plazo ni en la prevención de recaídas13,168. |
Recomendaciones
|
√
|
Se debería garantizar la disponibilidad de tratamiento psicoterapéutico para los pacientes que lo necesiten. |
|
B
|
En la depresión leve-moderada se recomienda considerar un tratamiento psicológico breve (como la terapia cognitivo-conductual o la terapia de solución de problemas) 6 a 8 sesiones durante 10-12 semanas. |
|
B
|
El tratamiento psicológico de elección en la depresión moderada-grave es la terapia cognitivo-conductual o la terapia interpersonal, 16 a 20 sesiones durante 5 meses. |
|
B
|
Deben considerarse la terapia cognitivo-conductual para aquellos pacientes con respuesta inadecuada a otras intervenciones o con una historia previa de recaídas y/o presencia de síntomas residuales. |
|
C
|
Se recomienda que la terapia electroconvulsiva sea administrada siempre por profesionales experimentados, tras una evaluación física y psiquiátrica y en un entorno hospitalario, siendo indispensable el consentimiento informado. |
|
B
|
Para los pacientes con depresión crónica y/o recurrente se recomienda el tratamiento combinado de fármacos y terapia cognitivo-conductual. |
7.3. Tratamiento farmacológico
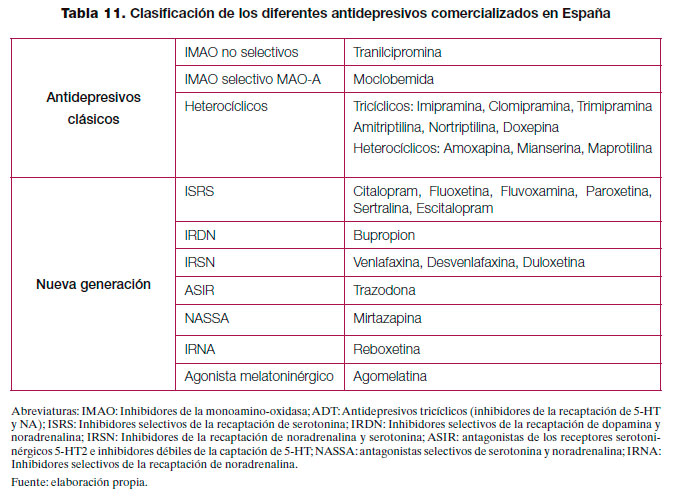
Los antidepresivos son fármacos dirigidos a mejorar los síntomas asociados a la depresión y existen diferentes tipos según su estructura química y su mecanismo de acción (tabla 11). Hay un tiempo de latencia en el comienzo de sus efectos terapéuticos que puede ser de 2 a 4 semanas, aunque algunos estudios señalan una respuesta más temprana, especialmente en aquellos pacientes que al final alcanzan la remisión del cuadro169.
7.3.1. Perfil de efectos adversos e interacciones
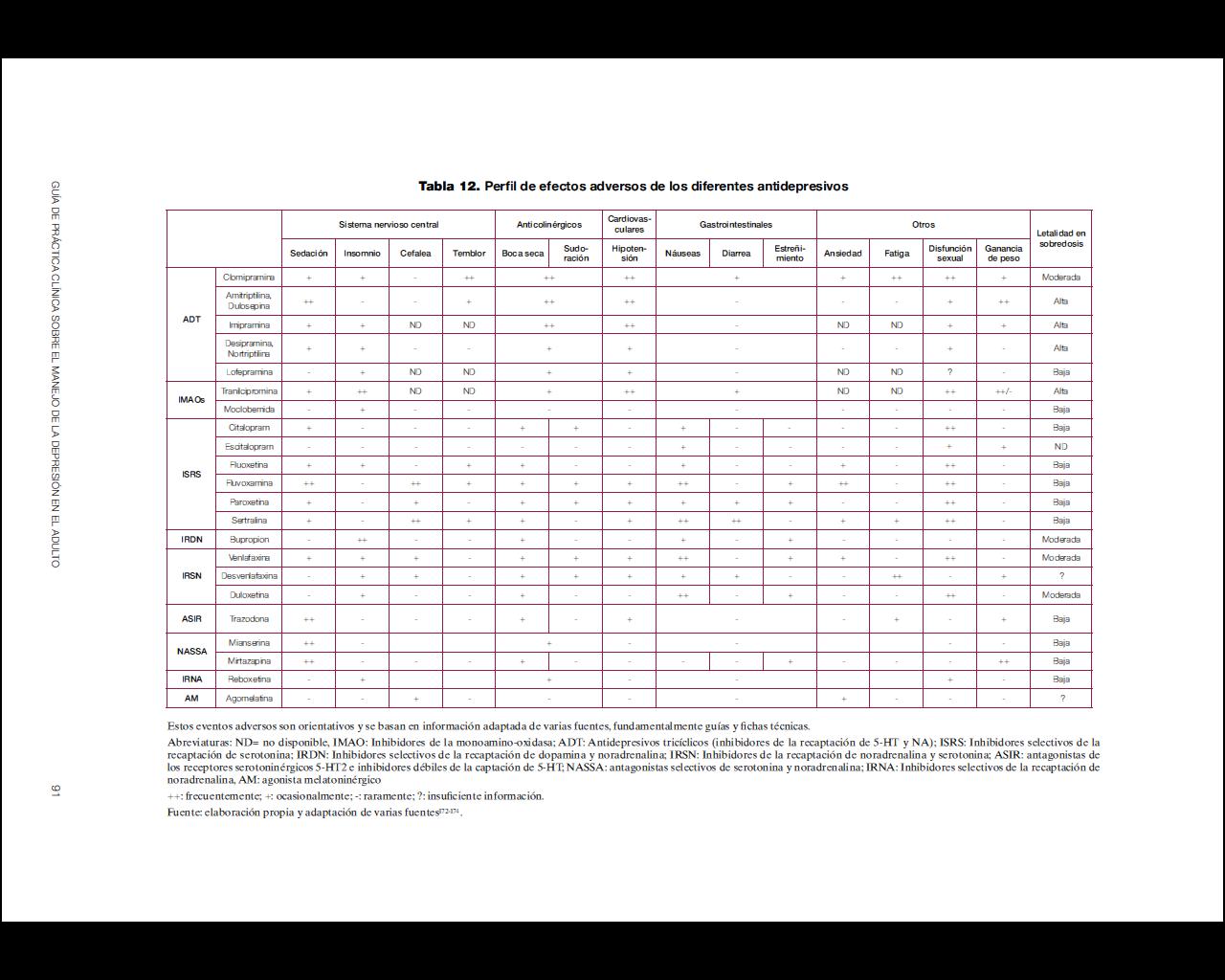
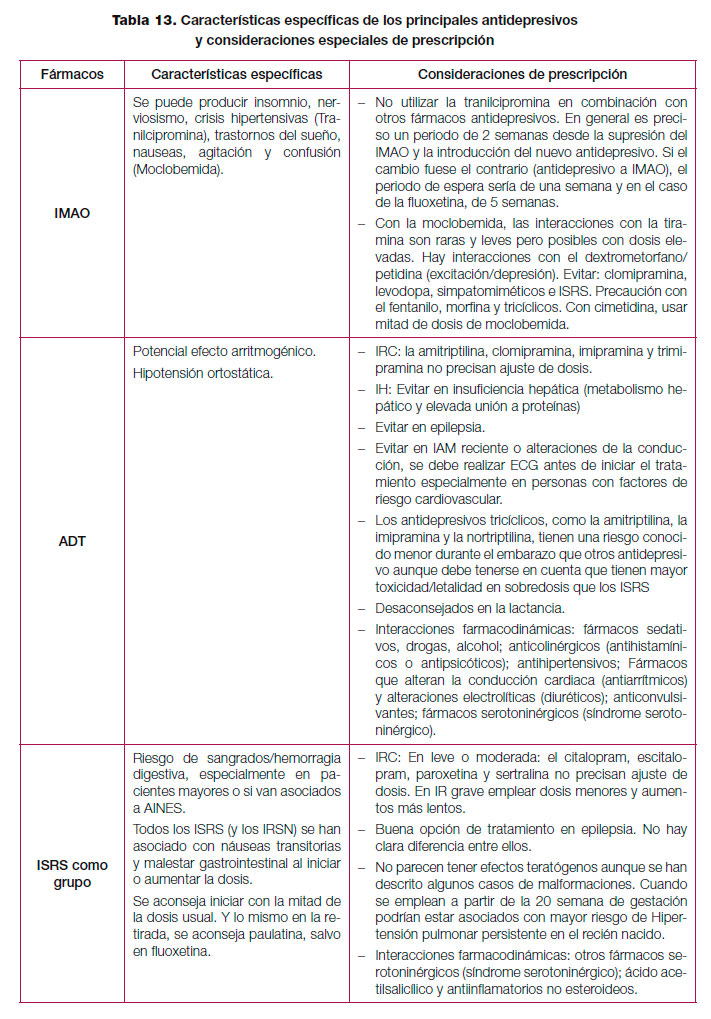
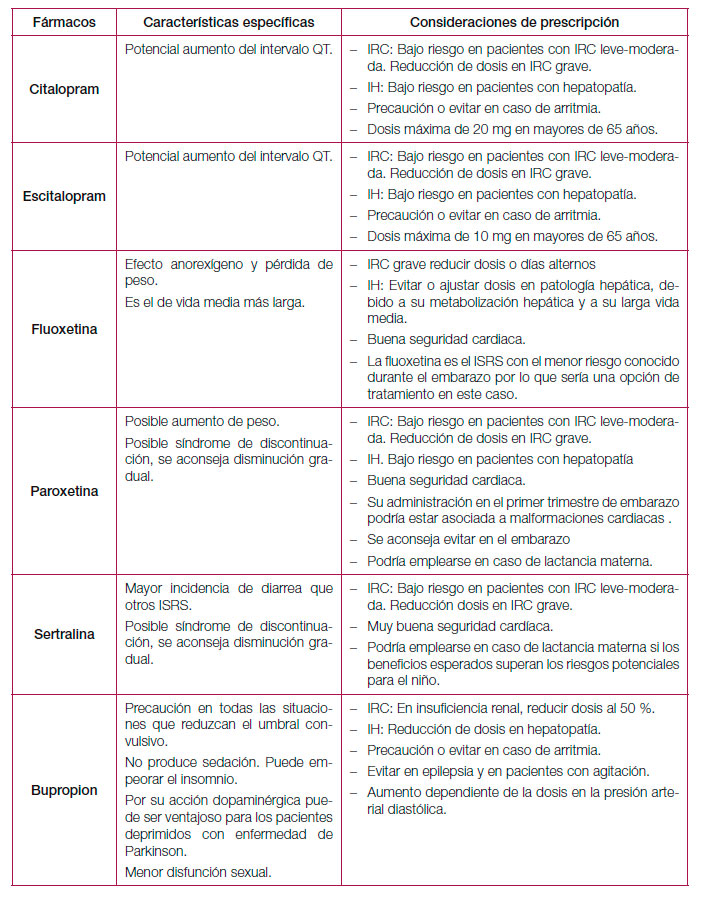
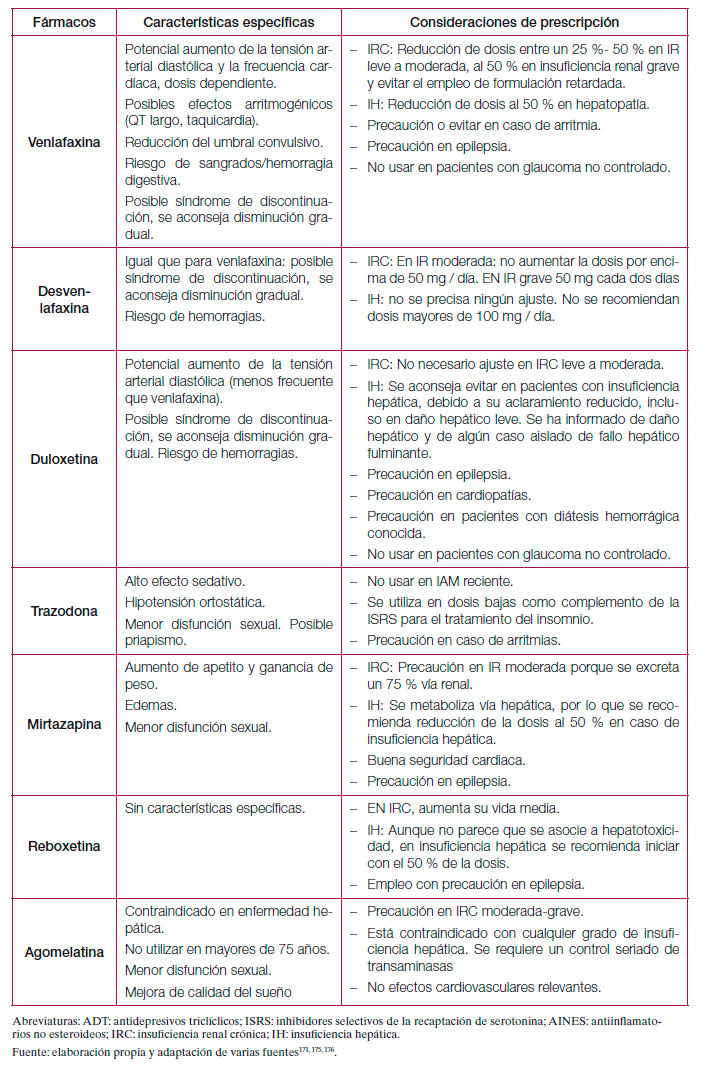
Los antidepresivos clásicos o de primera generación pueden presentar efectos secundarios que son mal tolerados por los pacientes e interaccionan de forma importante con otros fármacos o alimentos por lo que, en la actualidad, los antidepresivos de nueva generación son los más prescritos170. En la tabla 12 se resume el perfil de efectos adversos de los diferentes antidepresivos y en la tabla 13 algunos efectos específicos y otras consideraciones especiales de prescripción. Por último, y debido a la variabilidad existente, en el anexo 3 se muestran las presentaciones y costes de los principales antidepresivos comercializados en España. Respecto a las interacciones, las farmacodinámicas tienen que ver con la alteración del efecto de un fármaco debido a competencia, potenciación o alteración de sus mecanismos fisiológicos. Este tipo de interacciones es fácil de predecir conociendo las propiedades farmacológicas de los diferentes antidepresivos (ver tabla 13)171. Las interacciones farmacocinéticas de los antidepresivos se producen por inhibición de las enzimas del sistema citocromo hepático P450 implicadas en el metabolismo de la mayoría de los fármacos psicótropos y no psicótropos. Así, la inhibición de una enzima especifica de este sistema produce un aumento de los niveles plasmáticos (con posible toxicidad) de aquellos fármacos metabolizados por dicha enzima. La fluvoxamina, fluoxetina y paroxetina tendrían un elevado potencial de inhibición de algunos de los isoenzimas de este sistema, mientras que otros antidepresivos como el citalopram, mianserina, mirtazapina, reboxetina o venlafaxina sería mínimo171. Como norma general, se recomienda elegir los antidepresivos que presenten menor interferencia con el metabolismo de otros fármacos, especialmente en el caso de pacientes polimedicados172. Tabla 12. Perfil de efectos adversos de los diferentes antidepresivos.
7.3.2. Eficacia y seguridad de los fármacos antidepresivos
- En general, en los estudios participan un número relativamente pequeño de pacientes y durante un periodo de tiempo limitado. La selección de los pacientes es muy estricta, con exclusión, habitualmente, de aquellos con comorbilidades. Además, el seguimiento es muy riguroso y en condiciones controladas, lo que limita la generalización de los resultados a la práctica clínica habitual.
- Ciertos efectos adversos poco frecuentes pueden observarse únicamente cuando un gran número de personas ha utilizado un medicamento durante un periodo de tiempo prolongado.
- No siempre las dosis que se contrastan son las más adecuadas para el medicamento comparador, ni las supuestamente equipotentes.
- Posible existencia de conflictos de interés al ser financiados los estudios, en muchas ocasiones, por la propia empresa fabricante.
- En ocasiones puede haber sesgos de publicación científica al publicar los datos obtenidos en un estudio dependiendo de la naturaleza y dirección de sus resultados.
- Algunas de las diferencias en la eficacia entre los antidepresivos de primera y segunda generación tienen que ver en parte con aspectos metodológicos, puesto que en las últimas tres décadas se han producido mejoras en el diseño y calidad de los estudios que se han traducido en menores diferencias, sobre todo en comparación en el placebo.
- La utilización de muestras con un mayor número de sujetos pero más heterogéneas desde una perspectiva clínica también podría explicar la dificultad de encontrar diferencias en eficacia entre antidepresivos y de constatar menores diferencias respecto a placebo.
- Evaluación de respuesta y remisión al tratamiento únicamente con puntuaciones en escalas como la HRSD o el BDI, que si bien son instrumentos con adecuadas propiedades psicométricas, distan de ser óptimas como única variable para evaluar la eficacia de un fármaco.
7.3.2.1. Eficacia y seguridad de los antidepresivos tricíclicos
El mecanismo de acción de los antidepresivos tricíclicos (ADT) o antidepresivos de primera generación consiste en inhibir la recaptación de serotonina y noradrenalina. Aunque todos los ADT bloquean la recaptación de ambas monoaminas, algunos son más selectivos que otros y así, la clomipramina es más serotoninérgica y la imipramina más noradrenérgica. Todos los ADT provocan efectos secundarios anticolinérgicos en diferentes grados (boca seca, visión borrosa, estreñimiento, retención urinaria y sudoración), sedación e hipotensión postural, por lo que es necesario comenzar con dosis bajas e ir incrementándolas progresivamente13. Para abordar la eficacia y seguridad de los ADT en el tratamiento de la depresión mayor se efectuó una búsqueda de guías de práctica clínica, revisiones sistemáticas, metanálisis y estudios primarios, realizándose una selección de artículos específicamente para estos fármacos. La GPC que incluyó un mayor número de estudios sobre ADT fue la elaborada por el NICE13. En este apartado, los autores verificaron la falta de nueva evidencia sustancial desde la publicación de la guía original en 2004. Otras revisiones sistemáticas posteriores tampoco incluyeron nuevos estudios177,178.
Antidepresivos tricíclicos frente al placebo
Antidepresivos tricíclicos frente a otros fármacos antidepresivos
Aunque la amitriptilina no fue el primer ADT, ni es el mejor tolerado o el más prescrito, es el medicamento estándar contra el que se comparan los nuevos antidepresivos respecto a eficacia y tolerabilidad. Este es el motivo por el que la guía del NICE estableció dos subapartados, uno en el que evaluó la amitriptilina y otro en el que incluyó como comparador cualquier otro ADT.
Resumen de la evidencia
|
Antidepresivos tricíclicos frente a placebo
|
|
|
1+
|
Los antidepresivos tricíclicos son más eficaces que el placebo, tanto en respuesta como en remisión, aunque presentan mayor probabilidad de provocar efectos secundarios y de abandono precoz del tratamiento13,178. |
|
1+
|
Cuando se comparan con placebo, los antidepresivos tricíclicos muestran mayor eficacia que cada uno de los distintos grupos de antidepresivos y que el conjunto de ellos177. |
|
1+
|
De entre todos los antidepresivos tricíclicos, la amitriptilina es el más eficaz frente al placebo, seguida por la imipramina177. |
|
Antidepresivos tricíclicos frente a otros fármacos antidepresivos
|
|
|
1+
|
No se han observado diferencias clínicamente relevantes entre la amitriptilina y otros antidepresivos (incluyendo ISRS) al evaluar la tasa de respuesta. Sin embargo, los pacientes tratados con otros antidepresivos presentaron menos efectos secundarios y menor probabilidad de abandonar el estudio13. |
|
1+
|
Tampoco se ha observado una diferencia clínicamente relevante entre los antidepresivos tricíclicos (diferentes de la amitriptilina) y otros antidepresivos en la tasa de respuesta ni en la de remisión, aunque sí diferencias relevantes favorables a otros antidepresivos en reducir la probabilidad de abandonar el estudio precozmente debido a efectos secundarios13. |
|
1+
|
Otra revisión sistemática no encontró diferencias entre los antidepresivos tricíclicos y los ISRS, ni en tasa de respuesta ni de remisión. Sin embargo, los ISRS mostraron menores tasas de abandono y de efectos adversos que los tricíclicos178. |
7.3.2.2. Eficacia y seguridad de los inhibidores de la monoamino oxidasa
Los inhibidores selectivos de la monoaminooxidasa (IMAO) ejercen su efecto terapéutico mediante la unión reversible o irreversible a la monoamino oxidasa, enzima responsable del catabolismo de la noradrenalina y serotonina. Todos los IMAO tienen el potencial de inducir crisis hipertensivas si se ingieren alimentos que contienen tiramina (que también se metaboliza por la monoamino oxidasa) o si se prescriben fármacos que aumentan la neurotransmisión monoaminérgica. Los inhibidores reversibles de la monoamino oxidasa (RIMA), como la moclobemida, tienen una probabilidad mucho menor de causar crisis hipertensivas y en general no son necesarias restricciones dietéticas. Estas restricciones, las interacciones farmacológicas potencialmente graves y la disponibilidad de antidepresivos más seguros han llevado a que la prescripción de los IMAO irreversibles sea poco frecuente, incluso en los pacientes hospitalizados. Sin embargo, los IMAO son todavía citados como los antidepresivos más eficaces para el tratamiento de la depresión atípica13. Los dos únicos IMAO comercializados actualmente en España son la moclobemida y la tranilcipromina. Para abordar la eficacia y seguridad de los IMAO en el tratamiento de la depresión mayor se ha actualizado la GPC elaborada por el NICE13, que evalúa la moclobemida y la fenelzina y, al igual que con los antidepresivos tricíclicos, sus autores utilizaron la búsqueda bibliográfica de la edición de 2004 de la guía debido a la falta de nueva evidencia. Debido a que la fenelzina no está comercializada en España se ha eliminado de este apartado. Por otra parte, se ha incluido una revisión sobre la selegilina que, aunque en España no está aprobada para el tratamiento de la depresión, se utiliza en ocasiones como uso compasivo.
Moclobemida
Es un inhibidor reversible de la monoamino oxidasa A, en contraposición a los IMAO tradicionales que inhiben irreversiblemente ambas MAO, por lo que no requiere restricciones en la dieta, las interacciones medicamentosas que pueden llevar a una crisis hipertensiva son menos importantes y se necesita un periodo de lavado más corto cuando se quiere cambiar a otro antidepresivo. En general es bien tolerada, con pocos efectos anticolinérgicos.
Selegilina
La selegilina es un IMAO que inhibe selectivamente la MAO B, responsable de la degradación de la dopamina. Su indicación es la enfermedad de Parkinson, como monoterapia en estadios iniciales o como coadyuvante de la levodopa. En España no está aprobada la indicación para el tratamiento de la depresión.
Resumen de la evidencia
|
IMAO frente a placebo
|
|
|
1+
|
Se ha observado una diferencia clínicamente relevante favorable a la moclobemida, tanto en la tasa de respuesta como en la reducción de síntomas de depresión al final del tratamiento. No hubo diferencias clínicamente relevantes entre la moclobemida y el placebo en reducir la probabilidad de abandono precoz del tratamiento13. |
|
1+
|
La selegilina ha mostrado una tasa de respuesta un 33% mayor que el placebo177. |
|
IMAO frente a otros antidepresivos
|
|
|
1+
|
Frente a otros antidepresivos (ADT e ISRS), la moclobemida no presentó diferencias clínicamente relevantes ni en tasa de respuesta ni de remisión13. |
|
1+
|
La moclobemida tiene menos probabilidad de abandono del tratamiento debido a efectos secundarios que los ISRS y especialmente que los ADT13. |
7.3.2.3. Eficacia y seguridad de los ISRS y otros antidepresivos de nueva generación
Los ISRS y el resto de antidepresivos de nueva generación son un grupo heterogéneo de fármacos que actúa a través de sus efectos sobre los neurotransmisores serotonina, noradrenalina y dopamina. Aunque la eficacia de los antidepresivos de primera y nueva generación es muy similar, los de primera generación pueden producir efectos secundarios peor tolerados y presentan mayor riesgo de letalidad en sobredosis y de interacción con otros fármacos. Debido a ello, actualmente el papel de los nuevos antidepresivos en el tratamiento de la depresión mayor es crucial.
Comparación entre ISRS
Existen numerosos ECAs que han tenido como objetivo comparar la eficacia de los diferentes ISRS entre sí.
- Escitalopram vs citalopram: en esta comparación se incluyeron 5 estudios publicados con 1802 pacientes y el OR fue favorable al escitalopram. El NNT para ganar una respuesta adicional a las 8 semanas con escitalopram en comparación con el citalopram fue de 13. Sin embargo cabe destacar que en los análisis de comparaciones mixtas, teniendo en cuenta la eficacia del escitalopram y el citalopram frente al resto de antidepresivos ISRS y otros, no se encontraron diferencias significativas en la tasa de respuesta.
- Sertralina vs fluoxetina: en 4 estudios con 940 pacientes, el OR de la respuesta fue favorable a la sertralina y el NNT para ganar una respuesta adicional a las 6-12 semanas de tratamiento con sertralina fue de 13.
Comparación entre ISRS y otros antidepresivos de nueva generación
- ISRS (fluoxetina, paroxetina, citalopram, sertralina) vs venlafaxina XR: en un ECA multicéntrico de diseño abierto con 1385 pacientes se comparó la eficacia de diferentes ISRS frente a la venlafaxina XR. A las 25 semanas de tratamiento las tasas de remisión fueron similares en ambos grupos, aunque algunas variables secundarias (Clinical Global Impression y Quick Inventory Depressive Simptomatology-Self-Report) fueron favorables a la venlafaxina XR. Cabe destacar que se produjeron un 49% de pérdidas aunque los motivos de abandono fueron similares en ambos grupos181.
- ISRS (citalopram, fluoxetina, paroxetina, sertralina) vs duloxetina: en un ECA de diseño abierto se comparó la duloxetina con 4 ISRS genéricos a elección del médico. La variable primaria fue la eficacia medida con la escala Quick Inventory Depressive Simptomatology-Self-Report y a las 12 semanas no se encontraron diferencias significativas en ambos grupos en el porcentaje de remisión182.
- Paroxetina vs bupropion: en un ECA con 74 pacientes con depresión mayor y elevado riesgo de suicidio se evaluó la eficacia de estos antidepresivos en la reducción de la ideación o conducta suicida. Como variable secundaria emplearon el HRSD-17 (puntuación total sin el ítem de ideación suicida). No se encontraron diferencias en la conducta suicida ni en la gravedad de la depresión, aunque los pacientes con mayores niveles de ideación suicida al inicio del estudio y tratados con paroxetina obtuvieron una mejoría significativa en esta variable en comparación con los tratados con bupropion183.
Comparación entre otros antidepresivos de segunda generación
Desvenlafaxina
La desvenlafaxina es un antidepresivo recientemente autorizado y comercializado en España184. Al igual que la venlafaxina, es un potente inhibidor de la recaptación de serotonina y noradrenalina y débil inhibidor de la recaptación de dopamina. En su revisión sistemática, la AHRQ incluyó 3 ECAs que compararon la desvenlafaxina con la duloxetina como tratamiento de la fase aguda de la depresión mayor, y con el escitalopram y placebo para la prevención de recaídas. En el metanálisis se concluyó que la eficacia de la desvenlafaxina es similar a la de los otros antidepresivos de segunda generación170,179. Los estudios incluidos se describen a continuación:
Seguridad y aceptabilidad de los ISRS y otros antidepresivos de segunda generación
- La venlafaxina se asocia a un incremento del 52% de la incidencia de vómitos en relación a otros ISRS.
- La mirtazapina produce un mayor aumento de peso que el resto de los antidepresivos de segunda generación, siendo la ganancia media de peso entre 1 y 3 kg tras 6-8 semanas de tratamiento.
- La sertralina produce mayores tasas de diarrea, con una incidencia del 8% superior que otros antidepresivos (bupropion, citalopram, fluoxetina, fluvoxamina, mirtazapina, paroxetina, venlafaxina).
- La trazodona se asocia con un incremento del 16% de somnolencia, en comparación con bupropion, fluoxetina, mirtazapina, paroxetina y venlafaxina.
Resumen de la evidencia
|
1+
|
Al comparar la eficacia de los antidepresivos ISRS entre sí se han observado algunas diferencias estadísticamente significativas aunque de dudosa relevancia clínica170,179. La comparación entre diferentes ISRS (escitalopram vs paroxetina, fluoxetina vs sertralina, y fluvoxamina vs sertralina) no ha mostrado diferencias significativas en el mantenimiento de la respuesta o en alcanzar la remisión170,179. |
|
1+
|
No se han observado diferencias significativas en la eficacia de los ISRS frente a otros antidepresivos de segunda generación (IRDN, ISRN, ASIR, NASSA)170,179. |
|
1+
|
Aunque algunos estudios han señalado que la mirtazapina podría presentar mayor rapidez de acción que otros ISRS (citalopram, fluoxetina, paroxetina y sertralina), su eficacia antidepresiva no es mayor. La tasa de respuesta es similar a las 4 semanas y para encontrar una respuesta adicional en la primera o segunda semana, el NNT es de 7170,179. |
|
1+
|
La comparación entre diferentes ISRS y la venlafaxina XR no mostró diferencias en las tasas de remisión, aunque algunas variables secundarias fueron favorables a la venlafaxina XR181. |
|
1+
|
No se encontraron diferencias en la eficacia entre los ISRS y la duloxetina182. |
|
1+
|
En pacientes con depresión mayor y elevado riesgo de suicidio, no se encontraron diferencias entre la paroxetina y el bupropion en la conducta suicida ni en la gravedad de la depresión, aunque los pacientes con mayores niveles de ideación suicida al inicio del estudio y tratados con paroxetina obtuvieron una mejoría significativa en comparación con los tratados con bupropion183. |
|
1+
|
La comparación entre antidepresivos de segunda generación (duloxetina vs desvenlafaxina, mirtazapina vs desvenlafaxina, mirtazapina vs trazodona, venlafaxina vs bupropion y bupropion vs trazodona) no mostró diferencias significativas en la tasa de respuesta. Tampoco entre la trazodona y la venlafaxina en la prevención de recaídas o recurrencias170,179. |
|
1+
|
No se han observado diferencias en las tasas de respuesta ni de remisión entre la desvenlafaxina y la duloxetina185. Tampoco se han encontrado diferencias en las tasas de recaída entre la desvenlafaxina y el escitalopram186. |
|
1+
|
Aproximadamente, el 63% de los pacientes a tratamiento con antidepresivos de segunda generación sufren eventos adversos leves a lo largo del tratamiento (diarrea, mareos, boca seca, fatiga, cefalea, náuseas, disfunción sexual, sudoración, temblores, aumento de peso). En general, en las comparaciones entre antidepresivos individuales no hubo diferencias en la intensidad de los eventos adversos, aunque entre algunos, la frecuencia fue diferente170,172,173,179. |
|
3
|
En un estudio observacional realizado en España, el 59% de los pacientes tratados con antidepresivos de segunda generación presentó disfunción sexual170,179. |
|
1+
|
El bupropion provoca menores tasas de disfunción sexual que el escitalopram, fluoxetina, paroxetina y sertralina; mientras que las tasas de la paroxetina son superiores a las de otros antidepresivos de segunda generación170,179. |
|
1+
|
Los ISRS y antidepresivos de segunda generación no parecen asociarse a un incremento del riesgo de suicidio en adultos170,172,179. |
7.3.2.4. Eficacia y seguridad de la reboxetina
Es un inhibidor relativamente selectivo de la recaptación de noradrenalina. Puede producir efectos secundarios como insomnio, vértigo, boca seca, estreñimiento, y disminuir los niveles séricos de potasio. Debido a que el informe de la AHRQ no incluyó la reboxetina en su revisión, se efectuó una búsqueda de guías de práctica clínica, revisiones sistemáticas y estudios primarios, realizándose una selección de artículos específicamente para este fármaco. Los documentos recuperados fueron la GPC sobre depresión elaborada por NICE13 y dos revisiones sistemáticas elaboradas por el Institute for Quality and Efficiency in Health Care (IQWiG)189,190 y por Cipriani et al.191. Posteriormente se realizó una búsqueda bibliográfica de ensayos clínicos aleatorizados para completar las anteriores búsquedas, siendo el único ensayo clínico aleatorizado recuperado el de Wiles et al.192.
Reboxetina frente a placebo
Reboxetina frente a otros antidepresivos
Resumen de la evidencia
|
Reboxetina frente a placebo
|
|
|
1+
|
Tres ECA observaron una diferencia clínicamente relevante favorable a la reboxetina sobre el placebo en la tasa de respuesta y sólo alguna evidencia en relación a la tasa de remisión13. |
|
1+
|
Una revisión sistemática posterior de ECA publicados y no publicados no observó diferencias estadísticamente significativas entre la reboxetina y el placebo en la tasa de respuesta ni en la consecución de remisión al final del tratamiento189,190. |
|
1+
|
La reboxetina se asoció a mayores tasas de efectos adversos y de abandonos que el placebo189,190. |
|
Reboxetina frente a otros antidepresivos
|
|
|
1+
|
Tres ECA no observaron diferencias clínicamente relevantes entre la reboxetina y otros antidepresivos en las tasas de respuesta o de remisión, ni en la reducción de síntomas de depresión al final del tratamiento13. |
|
1+
|
Una revisión sistemática observó que la reboxetina obtuvo una tasa de remisión significativamente inferior que los ISRS189,190. |
|
1+
|
Un metanálisis observó que la reboxetina fue significativamente menos eficaz que 11 antidepresivos191 y un ECA no mostró que el tratamiento con reboxetina confiriese alguna ventaja sobre los ISRS en pacientes con depresión grave en Atención Primaria192. |
|
1+
|
No se observaron diferencias entre la reboxetina y otros antidepresivos, como los ISRS, en efectos adversos13,189,190, aunque fue peor tolerada que el bupropion, citalopram, escitalopram, fluoxetina y sertralina individualmente191. |
7.3.2.5. Eficacia y seguridad de la agomelatina
Es un antidepresivo con un mecanismo de acción diferente, ya que es un agonista de los receptores de melatonina (MT1 y MT2) y antagonista de los receptores serotoninérgicos 5-HT2c. No posee afinidad por los receptores adrenérgicos a o ß, histaminérgicos, colinérgicos, dopaminérgicos o benzodiacepínicos193. Obtuvo la aprobación de la EMEA en 2009 como tratamiento de la depresión mayor en el adulto, aunque asociada a un plan de gestión de riesgos debido a la posibilidad de producir daño hepático. Está pendiente de la aprobación por parte de la FDA. En España está aprobada su indicación en el tratamiento de episodios de depresión mayor en adultos y la dosis recomendada es de 25 mg/ día, aunque se puede aumentar hasta 50 mg/día. La guía de depresión mayor de NICE13 no incluyó la agomelatina en su revisión de tratamiento farmacológico al no tener licencia en el Reino Unido en ese momento. Por su parte, la guía canadiense, debido a su perfil de eventos adversos, la sitúa como un antidepresivo de primera elección173.
Eficacia frente a placebo
Eficacia frente a otros antidepresivos
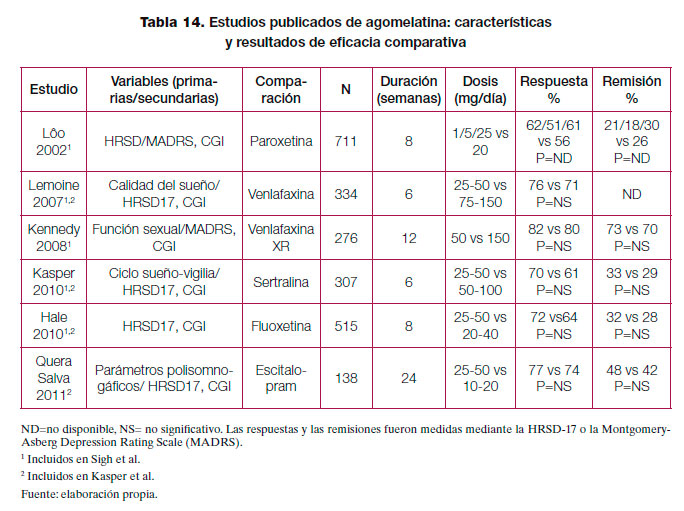
Seguridad y aceptabilidad: perfil de efectos adversos
Función sexual
Sueño
En pacientes tratados con agomelatina se observó una mejoría significativa en la calidad subjetiva del sueño, en comparación con venlafaxina213
En comparación con sertralina, se encontraron diferencias a favor de la agomelatina en la eficiencia y latencia del sueño medidos mediante actigrafía, aunque no se encontraron diferencias significativas en la amplitud del ritmo sueño-vigilia211.
En comparación con el escitalopram, la agomelatina se asoció con una reducción de la latencia del sueño REM, preservando el número de ciclos de sueño. Además, la evaluación con escalas analógicas visuales indicó que el tratamiento con agomelatina redujo el adormecimiento diurno215.
Síntomas de discontinuación
Un ECA219 estudió la discontinuación abrupta en pacientes que habían recibido 12 semanas de tratamiento con agomelatina (25 mg/ día) o paroxetina (20 mg/día). En el grupo que recibió agomelatina no se encontraron síntomas de discontinuación, ni en la primera ni en la segunda semana tras la interrupción. En el grupo que recibió paroxetina, los síntomas de discontinuación tras la primera semana fueron significativamente más altos que en el grupo de agomelatina, aunque no en la segunda.
Función hepática
Existe riesgo de elevación de las transaminasas en pacientes tratados con agomelatina. Se han encontrado elevaciones (triplicando los valores normales) en un 1,4% de los pacientes con la dosis de 50 mg/ día, en un 1% con la dosis de 25 mg/día y en el 0,7% con placebo. Aunque se ha descrito que algunos casos de elevación de transaminasas no se asociaron con signos de daño hepático y las reacciones hepáticas graves (10 veces el límite normal) fueron informadas de forma menos frecuente218, actualmente está contraindicado con cualquier grado de insuficiencia hepática y se requiere un control seriado de transaminasas.
- Al inicio del tratamiento con agomelatina.
- A las 3 semanas, 6 semanas (final de la fase aguda), 12 semanas y 24 semanas (final de la fase de mantenimiento), y de forma periódica posteriormente.
- Cuando se aumente la dosis de agomelatina, con la misma periodicidad que se sigue al inicio del tratamiento.
- Cuando esté clínicamente indicado.
- A cualquier paciente que presente un aumento de transaminasas séricas se le deben repetir las pruebas de función hepática en las siguientes 48 horas.
- El tratamiento debe interrumpirse inmediatamente si el aumento de transaminasas séricas sobrepasa 3 veces el límite superior del rango normal, o si los pacientes presentan síntomas o signos sugestivos de un posible daño hepático (coluria, acolia, ictericia, dolor en hipocondrio derecho o fatiga repentina inexplicable y prolongada).
- Se recomienda tener precaución al prescribir agomelatina a pacientes con niveles elevados de transaminasas antes del tratamiento o que presenten factores de riesgo de daño hepático (obesidad o sobrepeso, esteatosis hepática no alcohólica, consumo considerable de alcohol, uso concomitante de otros fármacos potencialmente hepatotóxicos o diabetes).
Resumen de la evidencia
|
1+
|
La agomelatina es más eficaz que placebo en el tratamiento de la depresión mayor moderada-grave, tanto en la fase aguda199 como en la prevención de recaídas209. |
|
1+
|
Los pacientes más jóvenes y los que presentan mayor número de episodios previos y menor duración de los mismos responden más favorablemente a la agomelatina que al placebo199. |
|
1+
|
La agomelatina es más eficaz que otros comparadores activos (paroxetina, venlafaxina, venlafaxina XR, sertralina, fluoxetina y escitalopram)199,214, aunque el tamaño del efecto obtenido hace cuestionar la relevancia clínica de estos resultados199. |
|
1+
|
En un ECA, la agomelatina fue más eficaz que la venlafaxina en la reducción de la anhedonia, aunque no en la reducción de los síntomas de depresión o ansiedad216. |
|
3
|
Un estudio prospectivo observacional en 3317 pacientes diagnosticados de depresión mayor y a tratamiento con agomelatina mostró a las 12 semanas una disminución en la puntuación de la escala MADRS de 18,3 puntos, con un 65,8% de respondedores y un 54,8% de remitentes. Alrededor del 80% de pacientes mejoraron la dificultad de conciliar el sueño y los despertares nocturnos, así como la somnolencia diurna217. |
|
1+
|
Los efectos adversos más comunes de la agomelatina están presentes en menos del 15% de los pacientes y son ligeramente superiores con la dosis de 50 mg/día que con la de 25 mg/día218. |
|
1+
|
En ensayos clínicos, las pérdidas debido a los efectos adversos fueron significativamente menores en los grupos tratados con agomelatina que con los comparadores199,214. |
|
1+
|
La agomelatina, bupropion, mirtazapina, moclobemida y selegilina transdérmica muestran unos porcentajes de disfunción sexual similares al placebo173. |
|
1+
|
En un ECA que evaluó el efecto de la agomelatina sobre la función sexual, no se encontraron diferencias significativas en comparación con la venlafaxina212. |
|
1+
|
La agomelatina fue más eficaz que la venlafaxina, sertralina y el escitalopram en diferentes parámetros relacionados con el sueño211,213,215. |
|
1+
|
En un estudio en el que se evaluó síntomas de discontinuación entre agomelatina y paroxetina, no se encontraron síntomas de discontinuación con la agomelatina ni en la primera ni en la segunda semana tras la interrupción, mientras que sí se presentaron en el grupo que recibió paroxetina en la primera semana219. |
|
1+
|
Existe riesgo de elevación de las transaminasas en pacientes tratados con agomelatina (de un 1,4% con dosis de 50 mg/día; de un 1% con la de 25 mg/día). Las reacciones hepáticas graves (10 veces el límite normal) fueron informadas de forma menos frecuente218. |
|
4
|
La AEMPS recomienda realizar un control de la función hepática al inicio del tratamiento con agomelatina, a las 3, 6, 12 y 24 semanas, y de forma periódica posteriormente. También cuando se aumente la dosis de agomelatina y cuando esté clínicamente indicado220. |
7.3.2.6. Papel de las benzodiacepinas en el tratamiento de la depresión
Las benzodiacepinas son fármacos eficaces como ansiolíticos e hipnóticos y con un inicio de acción rápida. A pesar de no tener un efecto antidepresivo específico, pueden producir mejoría de algunos síntomas de la depresión. Sin embargo, se asocian con tolerancia, dependencia y síndrome de abstinencia que puede ocurrir tras 4 a 6 semanas de uso continuo. Para evitar este problema, se recomienda no ser utilizadas durante más de 2-3 semanas13.
Resumen de la evidencia
|
4
|
Las benzodiacepinas pueden producir mejoría de algunos síntomas de la depresión. Sin embargo, su utilización no debería prolongarse más de 2-3 semanas con el fin de prevenir el desarrollo de dependencia13. |
7.3.3. Duración y dosis del tratamiento para la prevención de recaídas
El riesgo de recaída y de recurrencia en la depresión mayor es elevado, por lo que es importante definir el tiempo que debe mantenerse el tratamiento farmacológico tras la recuperación de un episodio. Diferentes ECA y metanálisis han demostrado que el mantenimiento del tratamiento farmacológico previene eficazmente la recurrencia de los síntomas depresivos, aunque no se han encontrado factores predictores del riesgo de recaída221,222. En general, los pacientes que abandonan el tratamiento antidepresivo tienen mayor riesgo de recurrencia que los que continúan con él221. Sin embargo, cuanto más se prolonga el tratamiento menor es la diferencia en el riesgo de recurrencia entre los pacientes tratados y los controles, es decir, el beneficio de prolongar el tratamiento va disminuyendo con el tiempo. Por este motivo, supone un reto importante ajustar para cada tipo de paciente el tiempo de duración del tratamiento tras la recuperación223,224.
NICE recomienda mantener el tratamiento con fármacos antidepresivos durante al menos 6 meses tras la remisión del episodio13. Otras guías recomiendan un tratamiento de mantenimiento de 12 meses tras alcanzar la remisión de un primer episodio depresivo225.
La dosis de mantenimiento debe ser la misma con la que se obtuvo la mejoría, ya que se ha observado que aquellos pacientes que reducen la dosis presentan mayores tasas de recaída que los que continúan con la misma226.
Es difícil hacer recomendaciones específicas sobre el tratamiento antidepresivo a largo plazo, por lo que es preferible realizar un enfoque personalizado de cada paciente y evaluar cuidadosamente los beneficios (prevención de recaída/recurrencia) y los riesgos de la administración de un fármaco a largo plazo (efectos secundarios, coste económico…).
Para la guía del NICE, la necesidad de un mantenimiento superior a los 6 meses vendría dada por el número de episodios previos de depresión, la presencia de síntomas residuales o la concurrencia de comorbilidades o dificultades psicosociales13.
La guía canadiense227 considera que aquellos pacientes con factores de riesgo (tabla 15) requerirán un tratamiento antidepresivo a largo plazo por un mínimo de 2 años y en ocasiones, de por vida221,222. Aunque sin evidencia empírica, el tratamiento de mantenimiento a largo plazo podría ser también considerado en pacientes con factores de vulnerabilidad a la depresión, como aquella de aparición temprana, cuando existen factores psicosociales adversos o enfermedades crónicas227.

Es importante verificar el cumplimiento de la medicación según el tiempo y las dosis adecuadas. En un estudio llevado a cabo en nuestro país, que realizó un seguimiento del cumplimiento de la medicación durante un periodo de 3 años, se observó que apenas un 22% de los pacientes evaluados consiguió mantener el tratamiento durante el periodo recomendado, esto es, un mínimo de 6 meses, mientras que la mayor parte, el 78%, abandonó el tratamiento antes de cumplir ese plazo, siendo el porcentaje de abandono más alto durante los primeros cuatro meses. Se observó también que los hombres presentaban más riesgo que las mujeres de abandonar el tratamiento farmacológico de manera temprana, ya que el 50% de los hombres manifestó haber dejado la medicación después de dos meses y el 50% de las mujeres después de tres meses228.
Síndrome de discontinuación con antidepresivos
La interrupción del tratamiento antidepresivo puede asociarse con un síndrome de discontinuación, caracterizado por la presencia de algunos de estos síntomas: irritabilidad, náuseas, insomnio, inestabilidad en la marcha, sudoración y parestesias.
Se han descrito casos de este tipo de reacciones con la práctica totalidad de antidepresivos, en respuesta tanto a una interrupción brusca como a una disminución gradual del fármaco, que incluyen: inhibidores selectivos de la recaptación de serotonina (ISRS), antidepresivos tricíclicos, inhibidores de la monoamino oxidasa (IMAO), y otros como la venlafaxina, mirtazapina, trazodona y duloxetina.
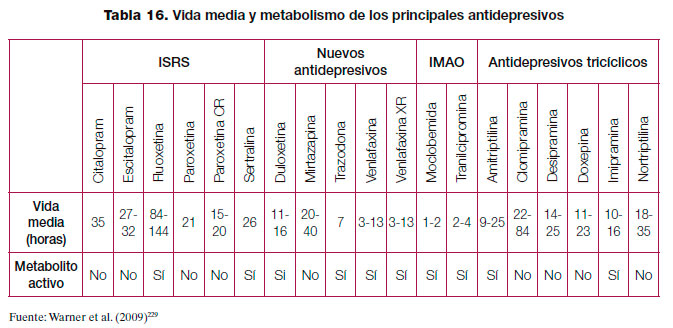
En los ISRS, un grupo de fármacos relativamente homogéneos, las diferencias en las propiedades farmacocinéticas, como la vida media de eliminación o su metabolismo, pueden ser los hechos más clínicamente relevantes (tabla 16). Así, el síndrome de discontinuación es más frecuente en aquellos pacientes que interrumpieron fármacos de una vida media relativamente corta, como la paroxetina, que en aquellos con vidas medias más prolongadas, como la fluoxetina229.
De esta manera el cese de un tratamiento antidepresivo debe realizarse reduciendo la dosis de forma gradual, normalmente en un periodo de 4 semanas, aunque algunas personas necesitarán periodos más prolongados, particularmente con fármacos de vida media corta como la paroxetina o venlafaxina. Debido a su larga vida media, la reducción gradual no sería necesaria con la fluoxetina13.
Resumen de la evidencia
|
3
|
La GPC del NICE recomienda mantener el tratamiento con fármacos antidepresivos durante al menos 6 meses tras la remisión del episodio. La necesidad de un mantenimiento superior a los 6 meses vendría dada por el número de episodios previos de depresión, la presencia de síntomas residuales o la concurrencia de comorbilidades o dificultades psicosociales13. |
|
3
|
Otras GPC recomiendan mantener el tratamiento con fármacos antidepresivos 12 meses tras la remisión del episodio y en aquellos pacientes con factores de riesgo se valorará un tratamiento antidepresivo a largo plazo por un mínimo de 2 años225. |
|
1+
|
La dosis de mantenimiento debe ser la misma con la que se obtuvo la mejoría, ya que se ha observado que aquellos pacientes que reducen la dosis presentan mayores tasas de recaída que los que continúan con la misma226. |
|
3
|
En un estudio llevado a cabo en nuestro país se observó que apenas un 22% de los pacientes consiguió mantener el tratamiento durante el periodo recomendado (un mínimo de 6 meses), mientras que el 78% abandonó el tratamiento antes de cumplir ese plazo, siendo el porcentaje de abandono más alto durante los primeros cuatro meses. Se observó también que los hombres presentaban más riesgo que las mujeres de abandonar el tratamiento farmacológico de manera temprana, ya que el 50% de los hombres manifestó haber dejado la medicación después de dos meses y el 50% de las mujeres después de tres meses228. |
|
4
|
El cese de un tratamiento antidepresivo debe realizarse reduciendo la dosis de forma gradual, normalmente en un periodo de 4 semanas, aunque algunas personas necesitarán periodos más prolongados, particularmente con fármacos de vida media corta como la paroxetina o venlafaxina. Debido a su larga vida media, la reducción gradual no sería necesaria con la fluoxetina13. |
Recomendaciones
La GPC ha sido revisada en junio de 2022. La revisión ha concluido que las recomendaciones continúan siendo vigentes. Aunque existen nuevas alternativas terapéuticas, el grupo de revisión de la guía considera que el abordaje de primera línea no se ve afectado en este momento. Se ha realizado un cambio de redacción en una recomendación sobre tratamiento farmacológico, que se señala en la GPC. El procedimiento para la revisión de la GPC puede consultarse en: Documento de revisión junio 2023
|
√
|
Antes de iniciar el tratamiento antidepresivo, se deberá informar adecuadamente al paciente de los beneficios que se esperan alcanzar, los efectos secundarios y el posible retraso del efecto terapéutico. |
|
A
|
La selección inicial del tratamiento farmacológico deberá basarse principalmente en el perfil de efectos secundarios y su tolerabilidad, la seguridad y las propiedades farmacológicas, así como en otros factores como la respuesta previa al tratamiento, los costes y las preferencias de los pacientes. |
|
A
|
Los ISRS son los antidepresivos con mayor evidencia y con mejor balance riesgo/ beneficio, por lo que deberán considerarse la primera elección de tratamiento. |
|
√
|
Es aconsejable que todos los pacientes con depresión moderada tratados con fármacos sean valorados nuevamente antes de 15 días tras la instauración del tratamiento, y antes de 8 días en el caso de depresión grave. |
|
DGPC
|
Se puede considerar el tratamiento con benzodiacepinas en casos de presencia de ansiedad, insomnio y/o agitación, aunque su uso no debería prolongarse más de 2-3 semanas con el fin de prevenir el desarrollo de dependencia. |
|
√
|
El seguimiento de los pacientes con tratamiento farmacológico ha de ser estrecho, al menos las 4 primeras semanas. |
|
D
|
Se recomienda que el tratamiento antidepresivo se mantenga al menos 6 meses tras la remisión del episodio y valorar aspectos como la existencia de episodios previos, comorbilidad y presencia de otros factores de riesgo antes de decidir su retirada |
|
A
|
Se recomienda que el tratamiento de mantenimiento se realice con la misma dosis con la que se alcanzó la respuesta. |
|
DGPC
|
Para evitar el síndrome de discontinuación, se recomienda que el cese del tratamiento antidepresivo se realice reduciendo la dosis de forma muy gradual, en un periodo de al menos 4 semanas, particularmente con fármacos de vida media corta como la paroxetina o venlafaxina.(modificada en 2023). |
|
DGPC
|
Ante un síndrome de discontinuación, se recomienda llevar a cabo una confirmación diagnóstica y en el caso de síntomas importantes, considerar reintroducir el antidepresivo original en su dosis efectiva (u otro antidepresivo de la misma clase con una vida media larga) y reducir la dosis gradualmente. |
|
Q
|
Cuando se prescriba tratamiento farmacológico se explorará la percepción del paciente y se favorecerá una actitud positiva del mismo. Además, se realizará una adecuada monitorización de los efectos secundarios y de la evolución tanto de los síntomas como de la capacidad funcional. Asimismo, tras haber obtenido la autorización del paciente, se aclararán las dudas de los familiares para poder contar con su apoyo al tratamiento. |
Bibliografía del apartado 07
1. Scottish Intercollegiate Guidelines Network. SIGN 50 A guideline developer’s handbook [Internet]. Edinburgh: Scottish Intercollegiate Guidelines Network; 2008 [actualizado nov 2011; citado 28 mar 2014]. Disponible en: http://www.sign.ac.uk/pdf/sign50.pdf
3. Goldsmith M, Bankhead C, Austoker J. Improving the quality of the written information sent to women about breast screening. Sheffield: NHS Cancer Screening Programmes; 2007.Informe Nº.: 64.
13. National Collaborating Centre for Mental Health. Depression. The treatment and management of depression in adults. London: The British Psychological Society; 2009. Informe No.: 90.
51. Grupo de Trabajo de la Guía de Práctica Clínica de Prevención y Tratamiento de la Conducta Suicida. Guía de Práctica Clínica de Prevención y Tratamiento de la Conducta Suicida. Santiago de Compostela: Agencia de Evaluación de Tecnologías Sanitarias de Galicia (avalia-t); 2012. Guías de Práctica Clínica en el SNS: avalia-t Nº 2010/02.
90. Beck AT, Rush AJ, Shaw BF, Emery G. Cognitive therapy of depression New York: Guilford Press; 1979.
121. Calderón C, Mosquera I, Balagué L, Retolaza A, Bacigalupe A, Belaunzaran J, et al. Modelos e intervenciones de colaboración entre Atención Primaria y Salud Mental en la atención a los pacientes diagnosticados de depresión: resultados de una meta-revisión. Investigación Comisionada. Vitoria-Gasteiz: Departamento de Salud, Gobierno Vasco; 2013. Informe N.º: D-13-13.
122. Bower P, Gilbody S. Stepped care in psychological therapies: access, effectiveness and efficiency: narrative literature review. Br J Psychiatry. 2005;186:11–7.
123. Palao DJ, Pérez-Solà V, Aragonés E, Jódar I. Adaptació al model sanitari català de la guia de pràctica clínica sobre el maneig de la depressió major en l’adult. Barcelona: Departament de Salut. Generalitat de Catalunya, Agència d’Informació, Avaluació i Qualitat en Salut; 2010.
124. Aragonès E, Piñol JL, Caballero A, López-Cortacans G, Casaus P, Hernández JM, et al. Effectiveness of a multi-component programme for managing depression in primary care: a cluster randomized trial. The INDI project. J Affect Disord. 2012;142(1-3):297-305.
125. European Alliance Against Depression [citado 14 ene 2014]. Disponible en: http://www.eaad. net/.
126. Multilevel intervention programme for prevention of depression and suicide. The EAAD experience in Catalonia, Spain [citado 14 ene 2014]. Disponible en: https://webgate.ec.europa. eu/sanco_mental_health/public/GOOD_PRACTICE/402/show.html.
127. Gilbody S, Bower P, Fletcher J, Richards D, Sutton AJ. Collaborative care for depression: a cumulative meta-analysis and review of longer-term outcomes. Arch Intern Med. 2006;166:2314-21.
128. Thota AB, Sipe TA, Byard GJ, Zometa CS, Hahn RA, McKnight-Eily LR, et al. Collaborative care to improve the management of depressive disorders: a community guide systematic review and meta-analysis. Am J Prev Med. 2012;42(5):525-38.
129. Aragonès E, López-Cortacans G, Sánchez-Iriso E, Piñol JL, Caballero A, Salvador-Carulla L, et al. Cost-effectiveness analysis of a collaborative care programme for depression in primary care. J Affect Disord. 2014;159:85-93.
130. European Association for Psychotherapy. Definition of the profession of Psychotherapy [citado 20 sep 2013]. Disponible en: http://www.europsyche.org/contents/13219/definition-ofthe- profession-of-psychotherapy
131. Parikh SV, Segal ZV, Grigoriadis S, Ravindran AV, Kennedy SH, Lam RW, et al. Canadian Network for Mood and Anxiety Treatments (CANMAT) clinical guidelines for the management of major depressive disorder in adults. II. Psychotherapy alone or in combination with antidepressant medication. J Affect Disord. 2009;117(Suppl 1):S15-25.
132. Cuijpers P, Smit F, Bohlmeijer E, Hollon SD, Andersson G. Efficacy of cognitive-behavioural therapy and other psychological treatments for adult depression: meta-analytic study of publication bias. Br J Psychiatry. 2010;196(3):173-8.
133. Barth J, Munder T, Gerger H, Nuesch E, Trelle S, Znoj H, et al. Comparative efficacy of seven psychotherapeutic interventions for patients with depression: a network meta-analysis. PLoS Med. 2013;10(5):e1001454.
134. Butler AC, Chapman JE, Forman EM, Beck AT. The empirical status of cognitivebehavioral therapy: a review of meta-analyses. Clin Psychol Rev. 2006 26(1):17-31.
135. DeRubeis RJ, Hollon SD, Amsterdam JD, Shelton RC, Young PR, Salomon RM, et al. Cognitive therapy vs medications in the treatment of moderate to severe depression. Arch Gen Psychiatry. 2005;62(4):409-16.
136. Dimidjian S, Hollon SD, Dobson KS, Schmaling KB, Kohlenberg RJ, Addis ME, et al. Randomized trial of behavioral activation, cognitive therapy, and antidepressant medication in the acute treatment of adults with major depression. J Consult Clin Psychol. 2006;74(4):658-70.
137. Hautzinger M, Jong-Meyer R, Treiber R, Rudolf GAE, Thien U. Efficacy of cognitive behavior therapy, pharmacotherapy, and the combination of both in non-melancholic, unipolar depression. Z Klin Psychol. 1996;25(2):130-45.
138. Jakobsen JC, Lindschou Hansen J, Storebo OJ, Simonsen E, Gluud C. The effects of cognitive therapy versus ‘treatment as usual’ in patients with major depressive disorder. PLoS One. 2011;6(8):e22890.
139. Jakobsen JC, Hansen JL, Storebo OJ, Simonsen E, Gluud C. The effects of cognitive therapy versus ‘no intervention’ for major depressive disorder. PLoS One. 2011;6(12):e28299.
140. Jakobsen JC, Hansen JL, Simonsen S, Simonsen E, Gluud C. Effects of cognitive therapy versus interpersonal psychotherapy in patients with major depressive disorder: a systematic review of randomized clinical trials with meta-analyses and trial sequential analyses. Psychol Med. 2012;42(7):1343-57.
141. Feng CY, Chu H, Chen CH, Chang YS, Chen TH, Chou YH, et al. The effect of cognitive behavioral group therapy for depression: a meta-analysis 2000-2010. Worldviews Evid Based Nurs. 2012;9(1):2-17.
142. Hegerl U, Hautzinger M, Mergl R, Kohnen R, Schutze M, Scheunemann W, et al. Effects of pharmacotherapy and psychotherapy in depressed primary-care patients: A randomized, controlled trial including a patients’ choice arm. Int J Neuropsychopharmacol. 2010;13(1):31- 44.
143. Bockting CL, Spinhoven P, Wouters LF, Koeter MW, Schene AH. Long-term effects of preventive cognitive therapy in recurrent depression: A 5.5-year follow-up study. J Clin Psychiatry. 2009;70(12):1621-8.
144. Godfrin K, van Heeringen C. The effects of mindfulness-based cognitive therapy on recurrence of depressive episodes, mental health and quality of life: A randomized controlled study. Behav Res Ther. 2010;48(8):738-46.
145. van Aalderen J, Donders A, Giommi F, Spinhoven P, Barendregt H, Speckens A. The efficacy of mindfulness-based cognitive therapy in recurrent depressed patients with and without a current depressive episode: A randomized controlled trial. Psychol Med. 2012;42(5):989-1001.
146. Segal ZV, Bieling P, Young T, MacQueen G, Cooke R, Martin L, et al. Antidepressant monotherapy vs sequential pharmacotherapy and mindfulness-based cognitive therapy, or placebo, for relapse prophylaxis in recurrent depression. Arch Gen Psychiatry. 2010;67(12):1256-64.
147. Britton WB, Shahar B, Szepsenwol O, Jacobs WJ. Mindfulness-based cognitive therapy improves emotional reactivity to social stress: results from a randomized controlled trial. Behav Ther. 2012;43(2):365-80.
148. Martell CR, Addis ME, Jacobson NS. Depression in context: Strategies for guided action. Nueva York: W. W. Nortonn. 2001.
149. Martell CR, Dimidjian S, Herman-Dunn R. Activación conductual para la depresión: Una guía clínica. Bilbao: Desclée de Brouwer. 2013.
150. Ekers D, Richards D, McMillan D, Bland J, Gilbody S. Behavioural activation delivered by the nonspecialist: Phase II randomised controlled trial. Br J Psychiatry. 2011;198(1):66-72.
151. Cohen S, O’Leary K, Foran H. A randomized clinical trial of a brief, problem-focused couple therapy for depression. Behav Ther. 2010;41(4):433-46.
152. Klerman GL, Weissman MM, Rounsaville BJ, Chevron ES. Interpersonal Psychotherapy of Depression. New York: Basic Books; 1984.
153. Raue PJ, Schulberg HC, Heo M, Klimstra S, Bruce ML. Patients’ depression treatment preferences and initiation, adherence, and outcome: a randomized primary care study. Psychiatr Serv. 2009(3):337-43.
154. Rogers CR. The necessary and sufficient conditions of therapeutic personality change. J Consult Psychol. 1957;21:95–103.
155. Shedler J. The efficacy of psychodynamic psychotherapy. Am Psychol. 2010;65(2):98-109.
156. Rodgers M, Asaria M, Walker S, McMillan D, Lucock M, Harden M, et al. The clinical effectiveness and cost-effectiveness of low-intensity psychological interventions for the secondary prevention of relapse after depression: a systematic review. Health Technol Assess. 2012;16(28):1-129.
157. NHS Improving Access to Psychological Therapies. Good practice guidance on the use of selfhelp materials within IAPT services: NHS Improving Access to Psychological Therapies; 2010.
158. Bennett-Levy J, Richards DA, Farrand P. Low intensity CBT interventions: a revolution in mental health care. En: Bennett-Levy J, Richards DA, Farrand P, et al., editors. Oxford guide to low intensity CBT interventions. Oxford: Oxford University Press; 2010.
159. Kessler D, Lewis G, Kaur S, Wiles N, King M, Weich S, et al. Therapist-delivered Internet psychotherapy for depression in primary care: a randomised controlled trial. Lancet. 2009;374(9690):628-34.
160. Vernmark K, Lenndin J, Bjarehed J, Carlsson M, Karlsson J, Oberg J, et al. Internet administered guided self-help versus individualized e-mail therapy: A randomized trial of two versions of CBT for major depression. Behav Res Ther. 2010;48(5):368-76.
161. Warmerdam L, van Straten A, Jongsma J, Twisk J, Cuijpers P. Online cognitive behavioral therapy and problem-solving therapy for depressive symptoms: Exploring mechanisms of change. J Behav Ther Exp Psychiatry. 2010;41(1):64-70.
162. Johansson R, Sjoberg E, Sjogren M, Johnsson E, Carlbring P, Andersson T, et al. Tailored vs. standardized internet-based cognitive behavior therapy for depression and comorbid symptoms: a randomized controlled trial. PLoS One. 2012;7(5):e36905.
163. Titov N, Andrews G, Davies M, McIntyre K, Robinson E, Solley K. Internet treatment for depression: a randomized controlled trial comparing clinician vs. technician assistance. PLoS One. 2010;5(6):e10939.
164. Pittaway S, Cupitt C, Palmer D, Arowobusoye N, Milne R, Holttum S, et al. Comparative, clinical feasibility study of three tools for delivery of cognitive behavioural therapy for mild to moderate depression and anxiety provided on a self-help basis. Ment Health Fam Med. 2010(3):145-54.
165. Johansson R, Ekbladh S, Hebert A, Lindstrom M, Moller S, Petitt E, et al. Psychodynamic guided self-help for adult depression through the internet: a randomised controlled trial. PLoS One. 2012;7(5):e38021.
166. Berger T, Hammerli K, Gubser N, Andersson G, Caspar F. Internet-based treatment of depression: A randomized controlled trial comparing guided with unguided self-help. Cogn Behav Ther. 2011;40(4):251-66.
167. Watkins E, Taylor R, Byng R, Baeyens C, Read R, Pearson K, et al. Guided self-help concreteness training as an intervention for major depression in primary care: A Phase II randomized controlled trial. Psychol Med. 2012;42(7):1359-71.
168. Hollandare F, Johnsson S, Randestad M, Tillfors M, Carlbring P, Andersson G, et al. Randomized trial of Internet-based relapse prevention for partially remitted depression. Acta Psychiatr Scand. 2011;124(4):285-94.
169. Taylor MJ, Freemantle N, Geddes JR, Bhagwagar Z. Early onset of selective serotonin reuptake inhibitor antidepressant action: systematic review and meta-analysis. Arch Gen Psychiatry. 2006;63(11):1217-23.
170. Gartlehner G, Hansen RA, Morgan LC, Thaler K, Lux LJ, Van Noord M, et al. Second- Generation Antidepressants in the Pharmacologic Treatment of Adult Depression. Rockville (MD): Agency for Healthcare Research and Quality (US); 2011. Informe N.º: 12-EHC012-EF Contrato N.º: 2902-2007-10056-I.
171. Taylor D, Paton C, Kapur S. The South London and Maudsley NHS Foundation Trust & Oxleas NHS Foundation Trust. Prescribing guidelines. 10th ed. London: Informa Healthcare; 2009.
172. Anderson IM, Ferrier IN, Baldwin RC, Cowen PJ, Howard L, Lewis G, et al. Evidence-based guidelines for treating depressive disorders with antidepressants: a revision of the 2000 British Association for Psychopharmacology guidelines. J Psychopharmacol. 2008;22(4):343-96.
173. Lam RW, Kennedy SH, Grigoriadis S, McIntyre RS, Milev R, Ramasubbu R, et al. Canadian Network for Mood and Anxiety Treatments (CANMAT) clinical guidelines for the management of major depressive disorder in adults III. Pharmacotherapy. J Affect Disord. 2009;117 Suppl 1:S26-43.
174. Agencia española del medicamento y productos sanitarios. Centro de Información online de Medicamentos de la AEMPS – CIMA [citado 20 nov 2013]. Disponible en: http://www.aemps. gob.es/cima/fichasTecnicas.do?metodo=detalleForm.
175. Angora-Cañego R, Esquinas-Requena JL, Agüera-Ortiz LF. Guía de selección de psicofármacos en el anciano con patología médica concomitante Psicogeriatria. 2012;4(1):1- 19.
176. García-Herrera Pérez Bryan JM, Nogueras Morilla EV, Muñoz Cobos M, Morales Asencio JM. Guía de Práctica Clínica para el tratamiento de la depresión en Atención Primaria. Málaga: Distrito Sanitario Málaga-UGC Salud Mental Hospital Regional Universitario “Carlos Haya”; 2011.
177. Undurraga J, Baldessarini R. Randomized, placebo-controlled trials of antidepressants for acute major depression: Thirty-year meta-analytic review. Neuropsychopharmacology. 2012;37(4):851-64.
178. von Wolff A, Holzel LP, Westphal A, Harter M, Kriston L. Selective serotonin reuptake inhibitors and tricyclic antidepressants in the acute treatment of chronic depression and dysthymia: a systematic review and meta-analysis. J Affect Disord. 2013;144(1-2):7-15.
179. Gartlehner G, Hansen RA, Morgan LC, Thaler K, Lux L, Van Noord M, et al. Comparative benefits and harms of second-generation antidepressants for treating major depressive disorder: an updated meta-analysis. Ann Intern Med. 2011;155(11):772-85.
180. Ou JJ, Xun GL, Wu RR, Li LH, Fang MS, Zhang HG, et al. Efficacy and safety of escitalopram versus citalopram in major depressive disorder: a 6-week, multicenter, randomized, doubleblind, flexible-dose study. Psychopharmacology (Berl). 2011;213(2-3):639-46.
181. Thase ME, Ninan PT, Musgnung JJ, Trivedi MH. Remission with venlafaxine extended release or selective serotonin reuptake inhibitors in depressed patients: A randomized, open-label study. Prim Care Companion J Clin Psychiatry. 2011;13(1):e1-e9.
182. Martinez JM, Katon W, Greist JH, Kroenke K, Thase ME, Meyers AL, et al. A pragmatic 12- week, randomized trial of duloxetine versus generic selective serotonin-reuptake inhibitors in the treatment of adult outpatients in a moderate-to-severe depressive episode. Int Clin Psychopharmacol. 2012;27(1):17-26.
183. Grunebaum MF, Ellis SP, Duan N, Burke AK, Oquendo MA, Mann JJ. Pilot randomized clinical trial of an SSRI vs bupropion: Effects on suicidal behavior, ideation, and mood in major depression. Neuropsychopharmacology. 2012;37(3):697-706.
184. Agencia Española del Medicamento [base de datos en Internet]. Agencia Española del Medicamento.Kastan 100 mg comprimidos de liberación prolongada Ficha técnica o resumen de características del producto. Disponible en: http://www.aemps.gob.es/cima/especialidad.do ?metodo=verPresentaciones&codigo=75554.
185. Tourian KA, Padmanabhan SK, Groark J, Brisard C, Farrington D. Desvenlafaxine 50 and 100 mg/d in the treatment of major depressive disorder: an 8-week, phase III, multicenter, randomized, double-blind, placebo-controlled, parallel-group trial and a post hoc pooled analysis of three studies. Clin Ther. 2009;31 Pt 1:1405-23.
186. Soares CN, Thase ME, Clayton A, Guico-Pabia CJ, Focht K, Jiang Q, et al. Desvenlafaxine and escitalopram for the treatment of postmenopausal women with major depressive disorder. Menopause. 2010;17(4):700-11.
187. Rickels K, Montgomery SA, Tourian KA, Guelfi JD, Pitrosky B, Padmanabhan SK, et al. Desvenlafaxine for the prevention of relapse in major depressive disorder: results of a randomized trial. J Clin Psychopharmacol. 2010;30(1):18-24.
188. Grupo de Trabajo de la Guía de Práctica Clínica sobre la Depresión Mayor en la Infancia y en la Adolescencia. Madrid: Ministerio de Sanidad y Política Social; 2009. Guías de Práctica Clínica en el SNS: avalia-t Nº 2007/09.
189. Bupropion, mirtazapine, and reboxetine in the treatment of depression: Executive summary of final report A05-20C, Version 1.1 (30.05.2011). En: Institute for Quality and Efficiency in Health Care: Executive Summaries. Cologne: IQWiG; 2011.
190. Eyding D, Lelgemann M, Grouven U, Härter M, Kromp M, Kaiser T, et al. Reboxetine for acute treatment of major depression: systematic review and meta-analysis of published and unpublished placebo and selective serotonin reuptake inhibitor controlled trials. BMJ. 2010;341(c4737).
191. Cipriani A, Furukawa TA, Salanti G, Geddes JR, Higgins JP, Churchill R, et al. Comparative efficacy and acceptability of 12 new-generation antidepressants: a multiple-treatments metaanalysis. Lancet. 2009;373(9665):746-58.
192. Wiles NJ, Mulligan J, Peters TJ, Cowen PJ, Mason V, Nutt D, et al. Severity of depression and response to antidepressants: GENPOD randomised controlled trial. Br J Psychiatry. 2012;200(2):130-6.
193. Agencia Española del Medicamento [base de datos en Internet]. Agencia Española del Medicamento.Valdoxan 25 mg comprimidos recubiertos con película – NR: 08499003 Ficha técnica o resumen de características del producto. Disponible en: http://www.ema.europa.eu/ docs/es_ES/document_library/EPAR_-_Product_Information/human/000915/WC500046227. pdf.
194. Kennedy SH, Emsley R. Placebo-controlled trial of agomelatine in the treatment of major depressive disorder. Eur Neuropsychopharmacol. 2006;16(2):93-100.
195. Lôo H, Hale A, D’haenen H. Determination of the dose of agomelatine, a melatoninergic agonist and selective 5-HT(2C) antagonist, in the treatment of major depressive disorder: a placebo-controlled dose range study. Int Clin Psychopharmacol. 2002;17(5):239-47.
196. Olie JP, Kasper S. Efficacy of agomelatine, a MT1/MT2 receptor agonist with 5-HT2C antagonistic properties, in major depressive disorder. Int J Neuropsychopharmacol. 2007;10(5):661-73.
197. Stahl SM, Fava M, Trivedi MH, Caputo A, Shah A, Post A. Agomelatine in the treatment of major depressive disorder: an 8-week, multicenter, randomized, placebo-controlled trial. J Clin Psychiatry. 2010;71(5):616-26.
198. Zajecka J, Schatzberg A, Stahl S, Shah A, Caputo A, Post A. Efficacy and safety of agomelatine in the treatment of major depressive disorder: a multicenter, randomized, double-blind, placebo-controlled trial. J Clin Psychopharmacol. 2010;30(2):135-44.
199. Singh SP, Singh V, Kar N. Efficacy of agomelatine in major depressive disorder: metaanalysis and appraisal. Int J Neuropsychopharmacol. 2012;25(3):417-28.
200. Koesters M, Guaiana G, Cipriani A, Becker T, Barbui C. Agomelatine efficacy and acceptability revisited: systematic review and meta-analysis of published and unpublished randomised trials. Br J Psychiatry. 2013;203:179-87.
201. European Agency for the Evaluation of Medicinal Products. CL3-021. Unpublished study, data from EMA reports. En: CHMP Assessment Report for Valdoxan: European Agency for the Evaluation of Medicinal Products; 2008 [citado 10 dic 2013]. Disponible en: http:// www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/ human/000915/WC500046226.pdf
202. European Agency for the Evaluation of Medicinal Products. CL3-022. Unpublished study, data from EMA reports. En: CHMP Assessment Report for Valdoxan: European Agency for the Evaluation of Medicinal Products; 2008 [citado 10 dic 2013]. Disponible en: http:// www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/ human/000915/WC500046226.pdf
203. European Agency for the Evaluation of Medicinal Products. CL3-024. Unpublished study, data from EMA reports. En: CHMP Assessment Report for Valdoxan: European Agency for the Evaluation of Medicinal Products; 2008 [citado 10 dic 2013]. Disponible en: http:// www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/ human/000915/WC500046226.pdf
204. European Agency for the Evaluation of Medicinal Products. CL3-026. Unpublished study, data from EMA reports. En: CHMP Assessment Report for Valdoxan. European Agency for the Evaluation of Medicinal Products 2008 [citado 10 dic 2013]. Disponible en: http:// www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/ human/000915/WC500046226.pdf
205. European Agency for the Evaluation of Medicinal Products. CL3-023. Unpublished study, data from EMA reports. En: CHMP Assessment Report for Valdoxan: European Agency for the Evaluation of Medicinal Products; 2008 [citado 10 dic 2013]. Disponible en: http:// www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/ human/000915/WC500046226.pdf
206. Novartis. CAGO178A2303. Unpublished Study: Novartis; 2011 [citado 10 dic 2013]. Disponible en: http://www.novctrd.com/ctrdWebApp/clinicaltrialrepository/displayFile. do?trialResult=2659
207. Novartis. CAGO178A2304. Unpublished Study: Novartis; 2011 [citado 10 dic 2013]. Disponible en: http://www.novctrd.com/ctrdWebApp/clinicaltrialrepository/displayFile. do?trialResult=3420
208. Goodwin GM, Emsley R, Rembry S, Rouillon F. Agomelatine prevents relapse in patients with major depressive disorder without evidence of a discontinuation syndrome: a 24-week randomized, double-blind, placebo-controlled trial. J Clin Psychiatry. 2009;70(8):1128-37.
209. Goodwin GM, Boyer P, msley R RF, de Bodinat C. Is it time to shift to better characterization of patients in trials assessing novel antidepressants? An example of two relapse prevention studies with agomelatine. Int Clin Psychopharmacol. 2013;28(1):20-8.
210. Hale A, Corral RM, Mencacci C, Ruiz JS, Severo CA, Gentil V. Superior antidepressant efficacy results of agomelatine versus fluoxetine in severe MDD patients: a randomized, double-blind study. Int Clin Psychopharmacol. 2010;25(6):305-14.
211. Kasper S, Hajak G, Wulff K, Hoogendijk WJ, Montejo AL, Smeraldi E, et al. Efficacy of the novel antidepressant agomelatine on the circadian rest-activity cycle and depressive and anxiety symptoms in patients with major depressive disorder: a randomized, double-blind comparison with sertraline. J Clin Psychiatry. 2010 71(2):109-20.
212. Kennedy SH, Rizvi S, Fulton K, Rasmussen J. A double-blind comparison of sexual functioning, antidepressant efficacy, and tolerability between agomelatine and venlafaxine XR. J Clin Psychopharmacol. 2008;28(3):329-33.
213. Lemoine P, Guilleminault C, Alvarez E. Improvement in subjective sleep in major depressive disorder with a novel antidepressant, agomelatine: randomized, double-blind comparison with venlafaxine. J Clin Psychiatry. 2007;68(11):1723-32.
214. Kasper S, Corruble E, Hale A, Lemoine P, Montgomery SA, Quera-Salva MA. Antidepressant efficacy of agomelatine versus SSRI/SNRI: results from a pooled analysis of head-to-head studies without a placebo control. Int Clin Psychopharmacol. 2013;28(1):12-9.
215. Quera-Salva MA, Hajak G, Philip P, Montplaisir J, Keufer-Le Gall S, Laredo J, et al. Comparison of agomelatine and escitalopram on nighttime sleep and daytime condition and efficacy in major depressive disorder patients. Int Clin Psychopharmacol. 2011;26(5):252-62.
216. Martinotti G, Sepede G, Gambi F, Di Iorio G, De Berardis D, Di Nicola M, et al. Agomelatine versus venlafaxine XR in the treatment of anhedonia in major depressive disorder: a pilot study. J Clin Psychopharmacol. 2012;32(4):487-91.
217. Laux G. The antidepressant agomelatine in daily practice: results of the non-interventional study VIVALDI. Pharmacopsychiatry. 2012;45(7):284-91.
218. Howland RH. A benefit-risk assessment of agomelatine in the treatment of major depression. Drug Saf. 2011;34(9):709-31.
219. Montgomery SA, Kennedy SH, Burrows GD, Lejoyeux M, Hindmarch I. Absence of discontinuation symptoms with agomelatine and occurrence of discontinuation symptoms with paroxetine: a randomized, double-blind, placebo-controlled discontinuation study. Int Clin Psychopharmacol. 2004;19(5):271-80.
220. Informe mensual. Noviembre 2012. Medicamentos de uso humano Madrid: Agencia Española de Medicamentos y Productos Sanitarios; [citado 08 feb 2013]. Disponible en: http://www. aemps.gob.es/informa/informeMensual/2012/noviembre/informe-medicamentos.htm#p3
221. Geddes JR, Carney SM, Davies C, Furukawa TA, Kupfer DJ, Frank E, et al. Relapse prevention with antidepressant drug treatment in depressive disorders: a systematic review. Lancet. 2003;361(9358):653-61.
222. Hansen R, Gaynes B, Thieda P, Gartlehner G, Deveaugh-Geiss A, Krebs E, et al. Meta-analysis of major depressive disorder relapse and recurrence with second-generation antidepressants. Psychiatr Serv. 2008;59(10):1121-30.
223. Reimherr FW, Amsterdam JD, Quitkin FM, Rosenbaum JF, Fava M, Zajecka J, et al. Optimal length of continuation therapy in depression: a prospective assessment during long-term fluoxetine treatment. Am J Psychiatry. 1998;155(9):1247-53.
224. Viguera AC, Baldessarini RJ, Friedberg J. Discontinuing antidepressant treatment in major depression. Harv Rev Psychiatry. 1998;5(6):293-306.
225. Ellis P. Australian and New Zealand clinical practice guidelines for the treatment of depression. Aust N Z J Psychiatry. 2004;38(6):389-407.
226. Papakostas GI, Perlis RH, Seifert C, Fava M. Antidepressant dose reduction and the risk of relapse in major depressive disorder. Psychother Psychosom. 2007;76(5):266-70.
227. Kennedy SH, Lam RW, Parikh SV, Patten SB, Ravindran AV. Canadian Network for Mood and Anxiety Treatments (CANMAT). Clinical guidelines for the management of major depressive disorder in adults. Introduction. J Affect Disord. 2009;117 Suppl 1:S1-2.
228. Serna MC, Cruz I, Real J, Gascó E, Galván L. Duration and adherence of antidepressant treatment (2003 to 2007) based on prescription database. Europe Psychiatry. 2010;25(4): 206– 13.
229. Warner CH, Bobo W, Warner C, Reid S, Rachal J. Antidepressant discontinuation syndrome. Am Fam Physician. 2006;74(3):449-56.






