Guía de Práctica Clínica sobre el Manejo del Ictus en Atención Primaria
Guía de Práctica Clínica sobre el Manejo del Ictus en Atención Primaria
Introducción
Este documento constituye la actualización de la anterior Guía de Práctica Clínica (GPC) para el Manejo de Pacientes con Ictus en Atención Primaria (AP) de 2009 (1). El material donde se presenta de forma detallada la información sobre el proceso metodológico de la GPC (estrategia de búsqueda, criterios de selección, tablas de guías) está disponible tanto en la página web de GuíaSalud como en la del Servicio Vasco de Evaluación de Tecnologías Sanitarias (Osteba) de la Fundación Vasca de Innovación e Investigación Sanitarias (BIOEF).
Epidemiología y carga asociada a las enfermedades cerebrovasculares
El ictus es una enfermedad cerebrovascular que presenta una alta incidencia y prevalencia (2). En España, los datos de 2017 señalaron que la tasa de mortalidad asociada al ictus ajustada por edad era de 25,1 por cada 100.000 habitantes (28,7 en hombres y 21,9 en mujeres) (2). Se trata de la segunda causa de muerte global, aunque por sexos, es la primera causa de mortalidad en mujeres y la tercera en hombres. Además, también se trata de la primera causa de discapacidad adquirida en la persona adulta y la segunda causa de demencia (2), lo que la coloca como una de las prioridades a abordar por nuestro sistema sanitario.
En todo el mundo se producen cerca de 12,2 millones de nuevos ictus al año (un ictus cada tres segundos), y 101 millones de personas viven con secuelas derivadas de éstos (3). Según la Organización Mundial de Ictus, en 2019 el 63 % de los ictus se produjeron en personas menores de 70 años, y el coste total estimado a nivel mundial fue de 861 billones de dólares estadounidenses (1,12 % del Producto Interior Bruto (PIB) mundial). Asimismo, entre 1990 y 2019 el número de casos aumentó de forma substancial (70 % de nuevos casos, 43 % de muertes por ictus, 102 % de ictus prevalentes y 143 % de años de vida ajustados por discapacidad (AVADs)), siendo los países de ingresos bajos o medios los que concentraban la mayor parte de la carga (3). Estos datos constatan que a nivel mundial el ictus sigue siendo la segunda causa de muerte y la tercera causa de la pérdida de AVADs.
En España, desde los años 70 la mortalidad por enfermedad cardiovascular (ECV) experimentó, gracias a los avances en la prevención primaria y en el diagnóstico y tratamiento en fase aguda, un descenso constante (1). Sin embargo, la incidencia de los casos de ictus sigue en aumento. En el estudio IBERICTUS (4) se observó que la tasa cruda de incidencia era de 187 casos por cada 100.000 habitantes, pero al desagregar los datos por grupos de edad, había diferencias, siendo ésta de 66,3 casos por 100.000 habitantes en el grupo de 45 y 54 años, y de 826,7 casos en el de 75 a 85 años (4). Estos datos concuerdan con los resultados obtenidos en un metaanálisis (MA) reciente sobre la pre-valencia e incidencia del ictus en Europa, que encuentra una prevalencia ajustada por sexo del 9,2 % (IC95 %: 4,4-14,0) y una incidencia ajustada por sexo de 191,9 casos por 100.000 personas-año (IC95 %: 156,4-227,3), con una tendencia creciente con el aumento de la edad (5).
Por lo tanto, teniendo en cuenta que la tasa de incidencia aumenta claramente con la edad en ambos sexos, y que nos encontramos en un contexto de un progresivo envejecimiento de la población, se estima que probablemente, la mortalidad por esta enfermedad aumentará en España cerca de un 39 % entre 2015 y 2035 (6).
Como se ha comentado anteriormente, el ictus es la primera causa de discapacidad adquirida en la persona adulta. En consecuencia, estamos ante una enfermedad que no sólo tiene una alta carga sanitaria, sino también una alta carga personal y familiar. Dos de cada tres personas que sobreviven a un ictus presentan algún tipo de discapacidad, ya sea en relación con la movilidad, como con el habla, la visión, el ánimo, la cognición o la personalidad (7). Así, las personas que han sufrido un ictus perciben con mayor frecuencia que su estado de salud y su calidad de vida es peor que la de los pacientes que sufren otras enfermedades crónicas, presentando con mayor frecuencia dificultades en la realización de sus actividades diarias (2). La realidad es que además de la carga personal que conlleva haber sufrido un ictus, el impacto que esto tiene en la familia, también es importante. El impacto en salud no solo se manifiesta en las personas que han sufrido un ictus, sino también implica la pérdida de calidad de vida relacionada con la salud (CVRS) de sus cuidadores (8). Intervenciones dirigidas desde AP para apoyar a las personas cuidadoras, como la atención desde enfermería domiciliaria, pueden ayudar a mejorar la calidad de vida de éstas (9).
Utilización de recursos por las personas con ictus
En relación con la utilización de recursos, la encuesta nacional de salud de 2017 encontró que las personas con ictus acudían con mayor frecuencia al médico de AP y al especialista que las personas que padecían otras enfermedades crónicas. Esta frecuencia era más alta en el grupo de menores de 65 años, que también consultaban más con fisioterapia y psicología o psiquiatría que los mayores de 65 años (2).
En cuanto a la utilización de los servicios de ayuda domiciliaria o del transporte, las personas con ictus los utilizaban con mayor frecuencia, siendo los servicios más demandados por los mayores de 65 años y por las mujeres (2).
También se encontró que los datos que proporcionaban los estudios sobre los costes de la atención a las personas que han sufrido un ictus son muy variables, lo que puede explicarse por la alta heterogeneidad con la fecha del análisis, el origen de los datos (por ejemplo, unidades de ictus o consultas especializadas), la duración del seguimiento (que afecta a los costes directos no sanitarios y a los indirectos) o el tipo de costes contemplados en el análisis (2).
Cabe destacar que la mayor parte de los costes reales no dependen de la hospitalización, sino del seguimiento y de los costes relacionados con la necesidad de cuidados informales.
Según el informe estadístico de enfermedades vasculares de la European Heart Network (10), en 2015 se estimó que el coste total asociado al ictus en España fue de 2908 millones de euros, un 43 % del total del coste sanitario, mientras que los cuidados informales reflejaban un 32 % de los costes y el 25 % restante una pérdida de productividad laboral.
La atención primaria y la variabilidad en la práctica clínica
Uno de los aspectos más importantes de la atención al ictus es que debe ser de carácter multidisciplinar. La integración y coordinación de los servicios de AP, urgencias extra e intrahospitalarias, servicios de neurología, rehabilitación, trabajo social, así como el servicio de geriatría en el caso de personas mayores, es fundamental para minimizar las secuelas del ictus y garantizar una atención eficiente y de calidad (1).
La AP tiene un papel clave en el abordaje de las enfermedades crónicas. En el caso de la ECV, las tareas incluyen desde la prevención primaria y secundaria de la enfermedad (áreas que ya han sido abordadas en otra guía nacional) (11), la atención al ictus agudo y la continuidad de cuidados a las personas que lo han sufrido y sus cuidadores tras el alta hospitalaria (12), siendo el papel de los y las profesionales de enfermería clave para muchas de estas funciones.
Estudios internacionales señalaron que, ante la presencia de sospecha de un ictus agudo, el primer profesional con el que contactaban muchas de estas personas era el médico de AP (1).
En un estudio reciente (13) se observó que el personal médico de AP tenían en general un buen nivel de conocimiento sobre los factores de riesgo y la prevención del ictus. Sin embargo, casi la mitad consideró que su formación no era suficiente y que la atención post-hospitalaria a las personas que han sufrido un ictus no era tan satisfactoria, puesto que solo la mitad de del personal médico encuestados programaban visitas de seguimiento. Además, también se ha descrito un déficit en el acceso de las personas que han sufrido un ictus a las ayudas sociales al año del evento, lo que influye de forma negativa en la calidad de vida percibida por estos pacientes (14).
Se ha descrito que un control eficaz de los factores de riesgo asociados a esta enfermedad puede ayudar a evitar más del 80 % de los casos. Por ello, teniendo en cuenta esto y la previsión del aumento de la prevalencia durante los últimos años, se debería mejorar tanto la prevención, como la atención y el seguimiento de estas personas por parte del equipo de AP, así como los servicios de rehabilitación para las secuelas que puedan presentarse (2).
Sigue habiendo margen de mejora, sobre todo en la atención posterior que recibe la persona que ha sufrido un ictus. Para ello, es necesario facilitar la coordinación entre los profesionales implicados, introduciendo protocolos o planes de acción que lo faciliten y fomentar la formación continuada de los equipos de AP. Por ello, con la actualización de esta guía se pretende actualizar la evidencia y las recomendaciones que se formularon en la versión de 2009 (1), haciendo hincapié en aquellas preguntas que pueden tener un mayor impacto en el manejo desde la AP de las personas que han sufrido un ictus.
Alcance y objetivos
El objetivo de la guía es ayudar a los profesionales sanitarios de AP en la atención y cuida-dos de la persona adulta con sospecha de ictus o ataque isquémico transitorio (AIT) que solicita atención al centro de AP, así como en el seguimiento y manejo posterior de las personas con ictus que han recibido el alta hospitalaria, especialmente si se trata de aspectos que se puedan abordar desde el punto de vista de la AP.
Con las recomendaciones que se han formulado en esta guía se pretende ayudar a reducir la morbimortalidad y mejorar la calidad de vida de estas personas desde la AP.
La guía se dirige principalmente a los profesionales sanitarios de AP implicados, tanto en el manejo de pacientes con sospecha de ictus o AIT, como en el manejo de pacientes con ictus o AIT que están en seguimiento tras el alta hospitalaria. Se trata de una herramienta que pretende identificar las estrategias y posibilidades terapéuticas disponibles para el manejo de esta enfermedad, con el fin de evitar pautas de tratamiento que no estén apoyadas por la evidencia científica.
La guía no incluye recomendaciones sobre la prevención primaria ni secundaria, ni aborda el diagnóstico, tratamiento y rehabilitación en el ámbito de la atención hospitalaria (AH). Tampoco se han incluido aspectos que ya se consideran consolidados en la atención de estas personas desde la AP.
Al tratarse esta guía de un trabajo con un enfoque nacional, no se afrontan temas organizativos, si bien sí trata de establecer unas recomendaciones básicas sobre criterios de derivación a AE, por lo que la guía también se difundirá entre todos los profesionales relacionados con la atención del ictus, aspecto esencial en su implementación.
A la hora de formular las recomendaciones se ha tenido en cuenta los recursos de los que se dispone actualmente en AP.
Recomendaciones
Diagnóstico inicial del ictus
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
¿Son útiles las escalas prehospitalarias en el entorno de la AP (consulta presencial y telefónica)?
Los efectos deseados de la intervención superan a los indeseables. Eso significa que la mayoría de los pacientes deberían recibir la intervención recomendada. LEER MÁS
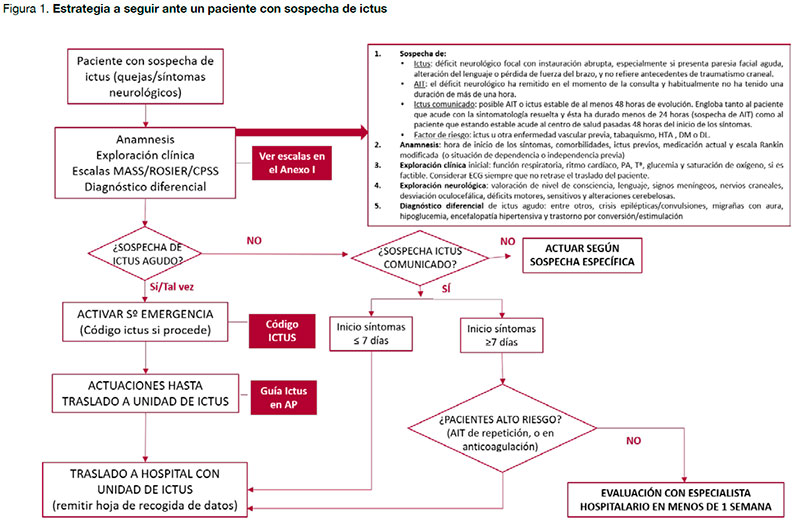
1. Se recomienda utilizar escalas, a ser posible validadas, para ayudar al diagnóstico del ictus en AP, en aquellas personas con síntomas neurológicos de instauración aguda.
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
2. Se sugiere realizar una valoración de los síntomas mediante la escala CPSS a aquellas personas que consultan a través del teléfono por síntomas neurológicos de instauración aguda (ver Anexo 1).
3. En la consulta de AP, se sugiere la utilización de la escala MASS o de la escala ROSIER como ayuda de orientación diagnóstica en personas con sospecha de ictus (ver Anexo 1).
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
4. Ante una persona con sospecha de ictus, no solo hay que tener en cuenta el tiempo y síntomas de inicio, sino también su situación funcional y cognitiva que marcará también la necesidad o no de activar el código ictus.
Justificación
Aunque no se han identificado estudios que comparen el impacto sobre los desenlaces de interés a largo plazo en función del uso o no de herramientas estandarizadas de cribado, se ha realizado una recomendación fuerte a favor del uso de dichas escalas en personas que han sufrido un ictus. Hay estudios que señalan que las herramientas de cribado son suficientemente sensibles y específicas para identificar personas con ictus (aunque sea con evidencia de baja calidad) y que el uso de cualquier herramienta que ayude a sistematizar el proceso de cribado y a registrar de forma sistemática los síntomas en la historia clínica puede ayudar a mejorar la identificación y manejo de estos casos.
En referencia a cuál puede ser la mejor escala para utilizar, se hacen dos sugerencias débiles a favor del uso de la escala Cincinnati Prehospital Stroke Scale (CPSS) si la consulta es telefónica y de la escala Melbourne Ambulance Stroke Scale (MASS) o la escala Recognition of Stroke in the Emergency Room (ROSIER) scale si se trata de la consulta de AP.
Justificación detallada
Calidad de la evidencia: la confianza en la evidencia es baja, porque se incluyen estudios en los que la valoración la hace tanto el personal del ámbito prehospitalario o del servicio de urgencias, incluyendo tanto personal paramédico como personal técnico de emergencias, enfermería, personal médico de urgencias y de AP, y porque muchos de los estudios tenían alto riesgo de sesgos en la selección de las personas con sospecha de ictus y riesgo no claro en el estándar de referencia y en el intervalo de tiempo o en el flujo de seguimiento.
Balance entre beneficios y riesgos: en el caso de la AP, se podrían utilizar las escalas CPSS, MASS o ROSIER. La escala CPSS es consistentemente más sensible, y se necesita más evidencia para determinar la precisión de MASS o ROSIER, que pueden ser más específicas en el diagnóstico.
En el caso de las llamadas telefónicas, se han utilizado las escalas CPSS o Face, arms, speech, time test (FAST), que muestran baja sensibilidad (S) en este contexto, aunque en otros muestran buena S, por lo que se podría sugerir su uso.
Factibilidad: se trata de escalas que ya están siendo utilizadas o, en caso de que no fuera así, que serían fáciles de implementar.
De la evidencia a la recomendación
¿Cómo de válida (exacta) es la prueba?
Varía, en función de la prueba de la que se trate.
Para su uso por personal médico y/o de enfermería de AP (datos de Zhelev et al., 2019 (18)):
– Comparación 1: CPSS vs. MASS: igual de sensible pero menos específica.
– Comparación 2: CPSS vs. ROSIER: igual de sensible pero menos específica.
– Comparación 3: FAST vs. ROSIER: igual de sensible y específica.
– Comparación 4: CPSS vs. Los Angeles Prehospital Stroke Screening (LAPSS): más sensible y quizá menos específica.
– Comparación 5: MASS vs. LAPSS: más sensible e igual de específica.
Para su uso en consulta telefónica (datos de Oostema JA et al., 2016 (19)):
– Medical Priority Dispatch System (MPDS) (cuatro estudios) o FAST (dos estudios): inexacta.
Para su uso por personal médico y/o de enfermería de AP (datos de Zhelev et al., 2019 (18)):
- CPSS es la prueba que presenta la mayor S de forma consistente, y, por lo tanto, se le debería dar preferencia frente a otras escalas existentes. Se necesita más evidencia para determinar la precisión absoluta y si escalas alternativas, como MASS y ROSSIER, que podrían tener una S similar pero mayor especificidad (E), deberían ser utilizadas en su caso para alcanzar mejor precisión.
- En la sala de emergencias, ROSIER debería ser el test de elección, puesto que se encuentra una alta S de forma consistente. En una cohorte de 100 pacientes en los que 62 tenían ictus/AIT, siete (rango de tres a 16) con ictus/AIT no serían diagnosticados. No se pudo obtener un estimador de la E.
Para su uso en consulta telefónica (datos de Oostema JA et al., 2016 (19)):
El personal de atención telefónica de emergencias es el primer punto de contacto que puede activar una respuesta al ictus agudo, y se han propuesto herramientas como la CPSS para mejorar su precisión. Una revisión sistemática (RS) (19) encontró estudios sobre MPDS (cuatro estudios), que se basa en el CPSS, y FAST (dos estudios). La S para el reconocimiento del ictus por el personal de atención telefónica fue subóptima en todos los casos (cinco estudios; rango de 41 a 83%) (valor predictivo positivo (VPP), rango de 42 a 68%, siete estudios).
¿Cuál es la magnitud de los efectos deseados esperados?
Se espera que los efectos deseados sean moderados para su uso por personal médico y/o de enfermería de AP y no se sabe en el caso de los o las teleoperadores/as.Se espera que el hecho de tener una herramienta sensible y específica, que aplicada de forma sistemática y estandarizada pueda tener un impacto moderado en la mejora de la identificación y manejo de estas personas, tanto en el contexto de atención presencial de AP como en la atención telefónica.
¿Cuál es la magnitud de los efectos no deseados esperados?
No se sabe.No hay estudios que comparen la S y E cuando se utilizan o no este tipo de herramientas en la identificación de estas personas. En relación con la S, cuanto peor sea ésta, menos personas serán identificadas.
¿Cuál es la confianza global en la calidad de la evidencia sobre la validez (exactitud) de la prueba?
Baja en general en AP (para todas las comparaciones) y en cuanto a la consulta telefónica, la calidad podría ser hasta muy baja.- Los autores de la revisión Cochrane (18) no han valorado la calidad de la evidencia para cada herramienta, pero debido a la inclusión de estudios en los que no sólo realizan evaluaciones el personal médico de AP y los posibles riegos de sesgos que existen, hacen presuponer que la confianza será baja en todos los casos. Debido al bajo número de estudios por test y por contexto, alto riesgo de sesgo, diferencias substanciales en las características del estudio y alta heterogeneidad entre estudios, estos resultados deberían tomarse como hipótesis provisionales que necesitan ser verificadas en estudios mejor diseñados.
- En el caso del personal de atención telefónica, los estudios tenían un riesgo moderado de sesgos (estándares de referencia variables y exclusión de pacientes del análisis), y ninguno comparó herramientas de cribado. Se señaló la necesidad de más estudios para identificar las causas del bajo nivel de reconocimiento del ictus por parte de los teleoperadores.
¿Cuál es la calidad global de la evidencia para cualquier beneficio directo importante o crítico, efectos adversos o la carga de la prueba?
Estudios no incluidos.No se han incluido estudios sobre el impacto más allá de la S y E.
¿Cuál es la calidad global de la evidencia sobre los efectos del manejo del paciente que es guiado por los resultados de la prueba?
Estudios no incluidos.No se han incluido estudios sobre el impacto más allá de la S y E.
¿Cómo de cierta es la relación entre los resultados de la prueba y las decisiones sobre el manejo del paciente?
Estudios no incluidosNo se han incluido estudios sobre el impacto más allá de la S y E.
¿Cuál es la calidad global de la evidencia sobre los efectos de la prueba?
Estudios no incluidos.Solo contamos con los datos de S y E de las pruebas en general y de algunas comparaciones en particular, pero no conocemos el impacto de utilizar estas pruebas frente a no utilizarlas. Tampoco el impacto que supone su utilización en la mejora del manejo y los resultados en estas personas. Por ello se considera que la evidencia es de baja calidad.
¿Existe incertidumbre o variabilidad importante sobre cómo valoran los pacientes los desenlaces principales?
Posiblemente incertidumbre o variabilidad no importantes.¿El balance entre los efectos deseados y no deseados favorece la intervención o la comparación?
Probablemente favorece la opción, tanto en AP como en consulta telefónica.En AP: se podrían utilizar CPSS, MASS o ROSIER. La escala CPSS es consistentemente más sensible, y se necesita más evidencia para determinar la precisión de MASS o ROSIER, que pueden ser más específicas para el diagnóstico.
En consulta telefónica: los estudios con teleoperadores han utilizado la CPSS o FAST, que en otros contextos muestra también buenos resultados de S, aunque los resultados pueden mejorarse. Se podría utilizar como herramienta para las llamadas telefónicas.
¿Cómo de altos son los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la confianza en la evidencia de los recursos requeridos (costes)?
No se han incluido estudios.No se han identificado estudios.
¿Favorece el coste-efectividad a la intervención o a la comparación?
Estudios no incluidosNo se han identificado estudios.
¿Cuál sería el impacto sobre la equidad en la salud?
Probablemente aumentaríaNo se han identificado estudios.
¿Es la prueba aceptable para los grupos de interés clave?
Probablemente síNo se han identificado estudios.
¿Es la prueba factible de implementar?
Probablemente síNo se han identificado estudios.
Bibliografía
18. Zhelev Z, Walker G, Henschke N, Fridhandler J, Yip S. Prehospital stroke scales as screening tools for early identification of stroke and transient ischemic attack. Cochrane Database Syst Rev. 2019;4(4):Cd011427. DOI: 10.1002/14651858.CD011427.pub2
19. Oostema JA, Carle T, Talia N, Reeves M. Dispatcher Stroke Recognition Using a Stroke Screening Tool: A Systematic Review. Cerebrovasc Dis. 2016;42(5-6):370-7. DOI: 10.1159/000447459
20. Meyran D, Cassan P, Avau B, Singletary E, Zideman DA. Stroke Recognition for First Aid Providers: A Systematic Review and Meta-Analysis. Cureus. 2020;12(11):e11386. DOI: 10.7759/cureus.11386
21. Jones SP, Bray JE, Gibson JM, McClelland G, Miller C, Price CI, et al. Characteris-tics of patients who had a stroke not initially identified during emergency prehospital assessment: a systematic review. Emerg Med J. 2021;38(5):387-93. DOI: 10.1136/emermed-2020-209607
Manejo prehospitalario del ictus agudo: Hipertensión arterial
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Hipertensión arterial
¿Se debe comenzar tratamiento en personas con sospecha de ictus agudo que acuden a AP y presentan presión arterial (PA) elevada?
¿A partir de qué cifras debe tratarse la hipertensión arterial?
En caso de decidir tratar, ¿qué fármacos deben emplearse?
Los efectos no deseables probablemente son mayores que los efectos deseables, pero con una incertidumbre apreciable. Eso significa que la mayoría de los pacientes no deberían recibir la intervención recomendada. Cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. En personas con sospecha de ictus agudo se sugiere no tratar la PA elevada en el ámbito extrahospitalario, siempre que se mantenga una PAS < 220 mmHg o una presión arterial diastólica (PAD) < 120 mmHg, salvo en determinadas situaciones urgentes, como sospecha clínica fundada de insuficiencia cardiaca izquierda, síndrome coronario agudo, disección aórtica o preeclampsia/ eclampsia.
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
2. En el caso en que se decida tratar, evitar descensos bruscos e intensos de la PA (más del 20 % en menos de 24 horas).
3. Evitar los fármacos sublinguales de acción rápida y utilizar preferentemente la vía intravenosa, y si no es posible, la vía oral (tras valoración de disfagia).
4. Cuando exista hipotensión, descartar la presencia de otra enfermedad concomitante grave y tratar según la etiología.
Los efectos no deseables probablemente son mayores que los efectos deseables, pero con una incertidumbre apreciable. Eso significa que la mayoría de los pacientes no deberían recibir la intervención recomendada. Cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
5. Se sugiere no tratar la hipertensión en personas con ictus isquémico agudo cuando su PA es < 220/120 mmHg y no van a recibir trombólisis intravenosa o trombectomía mecánica.
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
6. En personas con ictus isquémico agudo no tratados con trombólisis intravenosa o trombectomía mecánica y con una PA > 220/120 mmHg, es razonable el tratamiento farmacológico (reducción menor al 15 % de la PAS en 24 horas).
7. En personas con hemorragia intracerebral aguda, iniciar el tratamiento antihipertensivo tan pronto como sea posible.
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
8. En personas con hemorragia intracerebral aguda (menos de 6 horas desde el inicio de los síntomas), se sugiere la disminución de la PA hasta 140 mmHg para reducir la expansión del hematoma.
Justificación
Inicio de tratamiento de hipertensión arterial en la AP
La evidencia encontrada, aunque es de baja calidad, no apoya el tratamiento prehospitalario de la hipertensión arterial en personas con ictus agudo, por lo que se realiza una recomendación débil en contra de esta intervención.
Cifras a partir de las cuales iniciar tratamiento
No hay estudios que determinen a partir de qué cifras se ha de tratar la hipertensión arterial, pero sí recomendaciones de buena práctica en determinados contextos en base a estudios de asociación entre el nivel de PA y los desenlaces clínicos de las personas que han sufrido un ictus.
Tratamiento farmacológico para elegir
No se puede recomendar un fármaco en particular, puesto que no hay evidencia que determine cuál de ellos es mejor o más eficaz en reducir la PA o en mejorar los desenlaces de interés de estos pacientes. Por ello no se hacen recomendaciones a favor de uno u otro fármaco.
Justificación detallada
Inicio de tratamiento de hipertensión arterial en la AP
Calidad de la evidencia: la confianza en la evidencia es muy baja, porque se incluyen solo dos estudios pequeños en el ámbito prehospitalario, que tampoco es exactamente el contexto que se está evaluando en este caso (sería en el contexto de AP y no en la ambulancia).
Balance entre beneficios y riesgos: los estudios señalan que no hay beneficios en la reducción de la tasa de mortalidad ni en la recuperación funcional a los tres o seis meses, por lo que el balance no favorece la intervención.
Factibilidad: se considera que no es factible iniciar el tratamiento desde AP por los problemas que podrían surgir, y que es mejor esperar su inicio en el contexto hospitalario.
Cifras a partir de las cuales iniciar tratamiento
Los estudios de asociación entre el nivel de PA y los desenlaces de interés establecen puntos de corte a partir de los cuales los resultados en salud son peores o mejores. De aquí que se puedan establecer estos puntos de corte para iniciar el tratamiento, aunque no se ha demostrado que la disminución de la PA en esos casos se asocie a mejores resultados en los pacientes. Por ello, y teniendo en cuenta las recomendaciones de buena práctica de otras guías, se consideran unos límites de tratamiento para cada tipo de situación particular.
Tratamiento farmacológico para elegir
No hay estudios que comparen cuál de los fármacos tiene mejores resultados en relación con los desenlaces de interés de las personas que han sufrido un ictus, por lo que no se hace recomendación sobre cuál debería ser el fármaco a utilizar para tratar la hipertensión arterial en estos pacientes.
De la evidencia a la recomendación
Inicio de tratamiento de hipertensión arterial en la AP
¿Cuál es la magnitud de los efectos deseados esperados?
Insignificantes.En el estudio RIGHT (22), con 41 personas con sospecha de ictus (FAST 2 de 3) y PAS de más de 140 mmHg en las cuatro primeras horas del inicio de los síntomas, tras la aleatorización de los pacientes, se proporcionó gliceriltrinitrato (GTN) transdermal por personal paramédico entrenado. A los 90 días hubo una recuperación significativa en la escala de Rankin modificada (ERm) a favor del tratamiento, pero no en mortalidad (GTN 4/25 vs. no GTN 6/16, p=0,15). El estudio RIGHT-2 (23) reclutó 1149 personas con sospecha de ictus (FAST con 2 o 3 puntos), y PAS de más de 120 mmHg en las cuatro horas tras el inicio de los síntomas. No encontraron diferencias en las puntuaciones de ERm (GTN 358/568 (66 %) vs. no GTN 373/581 (67 %); p=0,88), ni en la tasa de mortalidad.
En conjunto, se estima una tasa de mortalidad a tres meses similar entre grupos (dos ECA; n=1190; 18,4 % vs. 17,4 %; OR de 0,74 (IC95 % de 0,23 a 2,35). La tasa de buen estado funcional a los tres meses (puntuación ERm de 0 a 2) también fue similar (dos ECA; n=1190; 37,4 % vs. 35,5 %; OR 1,33 (IC95 % de 0,59 a 3,01) (24, 25).
Cabe señalar que la PAS media de ambos estudios oscila entre los 160 y 168 mmHg.
¿Cuál es la magnitud de los efectos no deseados esperados?
No se sabe.No se han recogido datos de efectos adversos en los estudios incluidos.
¿Cuál es la calidad global de la evidencia sobre los efectos?
Muy baja.Son dos ECA, uno es un estudio piloto y los intervalos de confianza son muy amplios para los OR estimados, tanto para la mortalidad a los tres meses como para un buen estado funcional (ERm entre 0-2) a los tres meses post-ictus.
¿Hay incertidumbre o variabilidad importante sobre cómo valoran los pacientes la importancia de los desenlaces principales?
Probablemente la incertidumbre o variabilidad no sean importantes.No se ha identificado evidencia al respecto.
El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
Probablemente favorece la comparación.No se han descrito beneficios de iniciar el tratamiento de forma prehospitalaria, ni en la mortalidad ni en la recuperación funcional a los tres meses del ictus, aunque la evidencia es de muy baja calidad. Por ello, probablemente sea mejor no iniciar el tratamiento en ese contexto.
¿Cuál es la magnitud de los recursos requeridos (costes)?
Costes moderados.¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
Posiblemente favorece la comparación.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
No habría impacto en la equidad.¿Es aceptable la opción para todas las partes interesadas?
Probablemente no.¿Es factible la implementación de la intervención?
Probablemente sí.No se ha identificado estudios.
Cifras a partir de las cuales iniciar tratamiento
¿Cuál es la magnitud de los efectos deseados esperados?
- Personas con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: insignificante.
- Personas con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: moderada.
- Hemorragia intracraneal e hipertensión arterial: moderada.
Los estudios señalan diferencias en las cifras a partir de las cuales habría que iniciar tratamiento en función del tipo de ictus y de si van a recibir o no tratamiento mediante trombólisis endovenosa o trombectomía mecánica.
- Personas con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: en ausencia de revascularización, hay una relación tipo J o U entre la presión sanguínea y los resultados en salud tras un ictus isquémico agudo (26). Tanto una PA alta como baja en las horas iniciales se asocia con desenlaces clínicos no favorables. El nadir difiere entre estudios (de 120 a 185 mmHg), aunque la mayoría lo sitúa entre 150-160 mmHg y es mayor en las primeras 24-48h. A menudo disminuye de forma espontánea, incluso sin medicación (26).
- Personas con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: la relación se vuelve más compleja en estos casos. Personas con menor PAS post-trombólisis tienen resultados más favorables (nadir 148-160 mmHg). Los estudios demuestran de forma consistente que una menor PA se asocia con mejores resultados clínicos. Al ingreso, el límite era de 160-180 mmHg. Post-trombectomía, ésta era 20 mmHg menor, hasta 120 mmHg (26).
- Personas con hemorragia intracraneal e hipertensión arterial: un estudio prospectivo demostró que disminuir la PAS por debajo de 160 mmHg era seguro y factible. En un análisis post-hoc encontraron que el nivel que se asociaba con un menor riesgo de malos resultados clínicos fue 130 mmHg. Los estudios retrospectivos demostraron de forma consistente que una PAS menor de 160 mmHg o 140 mmHg se asociaba con mejores resultados clínicos (26).
En cuanto a los resultados de tratar la hipertensión arterial en personas que han sufrido un ictus:
- Personas con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis intravenosa ni trombectomía mecánica: el tratamiento con cualquier vasodepresor no disminuye la mortalidad a los 3-6 meses (18 ECAs; n=15144; 9,7 % vs. 8,6 %; OR 1 (IC95 % de 0,84 a 1,19)) (calidad moderada), ni la recuperación del estado funcional a los tres o seis meses (12 ECAs; n=9700; 65,8 % vs. 67 %; OR 0,98 (IC95 % de 0,85 a 1,12)) (24).
- Personas con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: no hay ensayos clínicos sobre la seguridad y eficacia de la disminución de la PA en personas con ictus isquémico agudo que excedan las cifras de PA recomendadas y en tratamiento con trombólisis endovenosa.
En cuanto al tratamiento intensivo (cifra objetivo 130-140 mmHg en 1 h) frente al no intensivo (cifra objetivo < 180 mmHg en 72 h), no se observan diferencias tanto en mortalidad como en un buen estado funcional a los tres meses en personas candidatas a trombólisis intravenosa (24). - Personas con hemorragia intracraneal e hipertensión arterial: en personas con ictus hemorrágico agudo (primeras 6 h), no hay diferencias en mortalidad a los tres y seis meses (cinco ECAs; n=3314; 11,7 % vs. 11,9 %; OR 0,95 (IC95 % de 0,64 a 1,43)), aunque sí en la expansión del hematoma (tres ECAs; n=2186; 21,4 % vs. 25,1 %; OR 0,81 (IC95 % de 0,67 a 0,99)), que reduce de forma significativa para el grupo tratado (24).
¿Cuál es la magnitud de los efectos no deseados esperados?
- Personas con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: no se sabe.
- Personas con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: moderada.
- Personas con hemorragia intracraneal e hipertensión arterial: no se sabe.
- Personas con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: no se han identificado datos, aunque utilizar fármacos que no son eficaces podría aumentar la probabilidad de aparición de efectos adversos.
- Personas con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: la evidencia sugiere que la presión sanguínea elevada antes o durante la trombólisis endovenosa puede relacionarse con desenlaces clínicos y resultados de imagen adversos (24), por lo que la infusión de alteplasa en aquellos con niveles de PAS y PAD elevados (> 185/110 mmHg) está contraindicada.
La probabilidad de hemorragia intracraneal sintomática es mayor en personas con ictus isquémico agudo con PA previa > 185/110 mmHg tratados con trombólisis endovenosa (OR de 1,39 a 2,59) (27, 28). En el estudio de Tsivgoulis G et al. (27), las violaciones del protocolo de PA pretratamiento con trombólisis endovenosa (> 185/110 mmHg) ocurrieron en el 12 % de los ictus isquémicos agudos, siendo la hemorragia intracraneal sintomática más probable en las personas en las que se había violado el protocolo de PA (OR 2,59; IC95 % de 1,07 a 6,25; p=0,034).
En un análisis retrospectivo del estudio Safe Implemenetation of Treatments in Stroke thrombolysis registry (SITS) (28), se encontró que una PA elevada pretratamiento era el único criterio off-label asociado de forma independiente a un mayor OR para sICH (OR 1,39; IC95 % de 1,08 a 1,80). - Personas con hemorragia intracraneal e hipertensión arterial: no se han identificado efectos adversos no deseados.
¿Cuál es la calidad global de la evidencia sobre los efectos?
- Personas con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: moderada.
- Personas con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: muy baja.
- Personas con hemorragia intracraneal e hipertensión arterial: muy baja.
- Personas con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: la calidad de la evidencia para los desenlaces considerados fue moderada en todos los casos.
- Personas con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: no hay estudios aleatorizados o prospectivos sobre la eficacia y seguridad de reducir la hipertensión arterial en personas con ictus isquémico agudo candidatos a trombólisis intravenosa, la evidencia proviene de estudios observacionales que señalan un aumento de riesgo de hemorragia intracraneal sintomática con niveles de PA superiror a 185 mmHg.
- Personas con hemorragia intracraneal e hipertensión arterial: la calidad de la evidencia para el desenlace de mortalidad es muy baja, lo que condiciona la calidad global de la evidencia.
¿Hay incertidumbre o variabilidad importante sobre cómo valoran los pacientes la importancia de los desenlaces principales?
Probablemente la incertidumbre o variabilidad no sean importantes.No se ha identificado evidencia al respecto.
El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
- Personas con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: favorece la comparación.
- Personas con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: probablemente favorece la intervención.
- Personas con hemorragia intracraneal e hipertensión arterial: probablemente favorece la intervención.
- Personas con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: se considera que al no encontrar evidencia sobre la eficacia del tratamiento antihipertensivo en los desenlaces de interés de personas con ictus agudo e hipertensión arterial no candidatos a trombólisis, no se justifica el tratamiento antihipertensivo en estas personas.
- Personas con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: aunque no existe evidencia directa, la relación entre el riesgo de hemorragia intracraneal sintomática en pacientes con ictus agudo e hipertensión arterial previa al tratamiento con trombólisis intravenosa, inclina la balanza a favor del tratamiento de la hipertensión arterial en aquellas personas que son susceptibles al tratamiento mediante trombólisis intravenosa.
- Personas con hemorragia intracraneal e hipertensión arterial: aunque no se hayan encontrado diferencias significativas en mortalidad, sí se ha señalado un impacto en la extensión del hematoma intracraneal, con lo que la balanza favorecería al tratamiento antihipertensivo en personas que han sufrido un ictus hemorrágicos.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.
No se han incluido estudios para ninguno de los casos.
¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.¿Cuál sería el impacto en la equidad en salud?
- Pacientes con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: no se sabe.
- Pacientes con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: no se sabe.
- Pacientes con hemorragia intracraneal e hipertensión arterial: no se sabe.
¿Es aceptable la opción para todas las partes interesadas?
- Pacientes con ictus isquémico agudo e hipertensión arterial no candidatos a trombólisis endovenosa ni trombectomía mecánica: probablemente sí.
- Pacientes con ictus isquémico agudo e hipertensión arterial candidatos a trombólisis: probablemente sí.
- Pacientes con hemorragia intracraneal e hipertensión arterial: probablemente sí.
¿Es factible la implementación de la intervención?
Probablemente síTratamiento farmacológico a elegir
¿Cuál es la magnitud de los efectos deseados esperados?
No se sabe.En la revisión de Bath et al. (29) se señala que en el subgrupo de personas con ictus isquémico agudo (n=11015) no se observa un beneficio sobre la muerte o la dependencia de recibir tratamiento frente al control (OR 1; IC95 % de 0,92 a 1,08).
Y en cuanto al tipo de fármaco, no se encontraron diferencias sobre la combinación de muerte o dependencia (OR 0,98; IC95 % de 0,92 a 1,05), siendo la heterogeneidad muy baja. Ninguna de las comparaciones individuales entre clases de fármacos o estrategias de bajada de PA fue significativa. Todos los fármacos (CCBs, ACEi, ARB, betabloqueantes y donantes de óxido nítrico) disminuían la PA (29).
¿Cuál es la magnitud de los efectos no deseados esperados?
No se sabe.No se han descrito los efectos adversos en la revisión.
¿Cuál es la calidad global de la evidencia sobre los efectos?
Muy baja.Aunque no se presenta la evaluación de la calidad de la evidencia de cada comparación, en general son pocos estudios (los antagonistas de los receptores de la angiotensina II (ARA-II) son los que más estudios y número de pacientes tienen), y se trata de comparaciones frente a placebo, no entre diferentes tipos de fármacos antihipertensivos.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantes.No se ha identificado evidencia al respecto.
El balance entre los efectos deseados y los no deseados esperados, ¿favorece a la intervención o a la comparación?
No se sabe.Se señala que todos los fármacos disminuyen la PA pero no cuál es mejor. En cuanto al efecto sobre mortalidad o dependencia, tampoco se señalan diferencias.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la confianza en la evidencia sobre los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
No se sabe.¿Es aceptable la opción para todas las partes interesadas?
No se sabe.¿Es factible la implementación de la intervención?
No se sabe.Tablas GRADE
Resumen de la evidencia
Bibliografía
22. Ankolekar S, Fuller M, Cross I, Renton C, Cox P, Sprigg N, et al. Feasibility of an ambulance-based stroke trial, and safety of glyceryl trinitrate in ultra-acute stroke: the rapid intervention with glyceryl trinitrate in Hypertensive Stroke Trial (RIGHT, ISRCTN66434824). Stroke. 2013;44(11):3120-8. DOI: 10.1161/STROKEAHA.113.001301
23. Bath PMS, P.; Anderson, C.S.; Appleton, J.P.; Berge, E.; Cala, l.; and the RIGHT-2 In-vestigators. Prehospital transdermal glyceryl trinitrate in patients with ultra-acute pre-sumed stroke (RIGHT-2): an ambulance-based, randomised, sham-controlled, blinded, phase 3 trial. Lancet. 2019;393(10175):1009-20. DOI: 10.1016/S0140-6736(19)30194-1
24. Sandset EC, Anderson CS, Bath PM, Christensen H, Fischer U, Gąsecki D, Lal A, Manning LS, Sacco S, Steiner T, Tsivgoulis G. European Stroke Organisa-tion (ESO) guidelines on blood pressure management in acute ischaemic stroke and intracerebral haemorrhage. Eur Stroke J. 2021 Jun;6(2):XLVIII-LXXXIX. DOI: 10.1177/23969873211012133
25. Lim BL, Lee WF, Ng WM, Situ W, Loo KV, Man Goh CJ, et al. Benefits and safety of transdermal glyceryl trinitrate in acute stroke: A systematic review and meta-analysis of randomized trials. Acad Emerg Med. 2022;29(6):772-88. DOI: 10.1111/acem.14408
26. Guo QH, Liu CH, Wang JG. Blood Pressure Goals in Acute Stroke. Am J Hypertens. 2022;35(6):483-99. DOI: 10.1093/ajh/hpac039
27. Tsivgoulis G, Frey JL, Flaster M, Sharma VK, Lao AY, Hoover SL, et al. Pre-tissue plasminogen activator blood pressure levels and risk of symptomatic intracerebral hem-orrhage. Stroke. 2009;40(11):3631-4. DOI: 10.1161/STROKEAHA.109.564096
28. Mundiyanapurath S, Hees K, Ahmed N, Wahlgren N, Uhlmann L, Kieser M, et al. Pre-dictors of symptomatic intracranial haemorrhage in off-label thrombolysis: an analysis of the Safe Implementation of Treatments in Stroke registry. Eur J Neurol. 2018;25(2):340-e11. DOI: 10.1111/ene.13507
29. Bath PM, Krishnan K. Interventions for deliberately altering blood pressure in acute stroke. Cochrane Database Syst Rev. 2014;2014(10):Cd000039. DOI: 10.1002/14651858. CD000039.pub3
Manejo prehospitalario del ictus agudo: Hiperglucemia
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Hiperglucemia
En personas con sospecha de ictus agudo, ¿se debe iniciar tratamiento de la hiperglucemia desde la AP/prehospitalaria?
¿A partir de qué cifras debe tratarse la hiperglucemia?
Los efectos no deseables probablemente son mayores que los efectos deseables, pero con una incertidumbre apreciable. Eso significa que la mayoría de los pacientes no deberían recibir la intervención recomendada. Cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere no tratar de forma prehospitalaria la hiperglucemia en personas con sospecha de ictus agudo.
Los efectos indeseados de la intervención superan los deseados. Eso significa que la intervención no debería ser usada o recomendada. LEER MÁS
2. Se recomienda no tratar de forma intensiva la hiperglucemia en personas con ictus agudo.
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
3. Tratar la hiperglucemia en aquellos casos que se superen los 155 mg/mL, manteniendo el nivel entre los 140-180 mg/dL.
4. Descartar la hipoglucemia como causa de los síntomas y corregir el nivel de glucemia si ésta estuviese presente.
Justificación
No existe evidencia sobre el beneficio de tratar de forma prehospitalaria a personas que han sufrido un ictus agudo y presentan hiperglucemia, solo se ha identificado un estudio que evalúa el efecto del tratamiento en los niveles de glucemia y los episodios de hipoglucemia que podían darse, por lo que se ha formulado una recomendación débil en contra de dicha intervención.
En cuanto a las cifras de glucemia a partir de las cuales habría que iniciar tratamiento, no se hace una recomendación en base a evidencia, pero sí una recomendación de buena práctica.
Justificación detallada
Inicio de tratamiento de hiperglucemia en AP
- Calidad de la evidencia: la calidad de la evidencia es muy baja, porque el único estudio que se ha identificado valora el efecto del tratamiento en el valor de la glucemia y no en los desenlaces de interés para las personas que acaban de sufrir un ictus.
- Balance entre beneficios y riesgos: la insulina intravenosa disminuye la glucosa en plasma de forma significativa y la subcutánea no, pero no hay más datos relevantes para el paciente.
- Aceptabilidad e implementación: probablemente estarían de acuerdo en no iniciar el tratamiento.
Cifras a partir de las cuales iniciar tratamiento
No se hace una recomendación en base a evidencia, pero sí una recomendación de buena práctica en base a un estudio español y las cifras objetivo que se marcaron en los grupos control de los ensayos clínicos incluidos en la comparación con el tratamiento intensivo. También se tiene en cuenta de forma indirecta que el tratamiento intensivo no tiene beneficios sobre los desenlaces de interés para las personas con ictus, además de aumentar los episodios de hipoglucemia. No se toma el valor de 11 mmol/L, porque se considera que se trata de un valor demasiado elevado y porque formaba parte de otro paquete de medidas que hace difícil evaluar el efecto directo de la medida.
No se realiza distinción entre personas con o sin diabetes, porque se considera que el 25 % de las personas con ictus que acuden al hospital tienen diabetes no conocida. Por eso, se considera tratar a todos por igual.
De la evidencia a la recomendación
Inicio de tratamiento de hiperglucemia en AP
¿Cuál es la magnitud de los efectos deseados esperados?
Insignificantes.La guía de la European Academy of Neurology (EAN) y European Stroke Organization (ESO) 2017 (30) identifica un único estudio en el ámbito prehospitalario (31) sobre la administración de insulina intravenosa o subcutánea y de su efecto en personas con ictus agudo e hiperglucemia. Se observa que la concentración de glucosa del grupo con tratamiento intravenoso disminuye de forma significativa (–1,9 mmol/ L, IC95 % de –3,5 a –0,27, o lo que es lo mismo: -34,23 mg/dL, IC95% de -63,06 a -4,86 mg/dL) en comparación con el del grupo control. La insulina subcutánea no disminuyó la glucosa en plasma de forma significativa frente al grupo control (–0,9 mmol/L, IC95 % de –2,4 a 0,6; o lo que es lo mismo -16,4mg/dL, IC95% de -43,24 a 10,81 mg/dL).
En la búsqueda realizada para actualizar la evidencia desde la publicación de esta guía, no se identificaron nuevos estudios en el ámbito prehospitalario, y tampoco referidos a la AP, que proporcionaran más datos al respecto, por lo que no hay evidencia que establezca si el tratamiento de forma prehospitalaria tiene efecto en los desenlaces de interés.
¿Cuál es la magnitud de los efectos no deseados esperados?
Pequeños.El estudio de Nurmi et al. (31), no registró eventos adversos serios, aunque sí una hipoglucemia sintomática en el grupo intravenoso y una hipoglucemia asintomática retardada en una persona que recibió por error una dosis subcutánea más alta que la del protocolo.
¿Cuál es la calidad global de la evidencia sobre los efectos?
Muy baja.No hay estudios que valoren el efecto de tratar la hiperglucemia en personas que han sufrido un ictus agudo en los desenlaces del paciente, solo se mide si se desciende o no el nivel de glucemia en éstos.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantes.No se ha identificado evidencia al respecto.
El balance entre los efectos deseables e indeseables esperados, ¿favorece a la intervención o a la comparación?
No favorece ni la intervención ni la comparación.No se han descrito los beneficios de iniciar tratamiento de forma prehospitalaria en la mortalidad ni en la recuperación funcional a los tres meses del ictus, aunque la evidencia es de muy baja calidad. Por ello, probablemente sea mejor no iniciar el tratamiento en ese contexto.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad global de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
No se sabe.¿Es aceptable la opción para las partes interesadas?
No se sabe.¿Es factible la implementación de la opción?
Probablemente sí.Cifras a partir de las cuales iniciar tratamiento
¿Cuál es la magnitud de los efectos deseados esperados?
No se sabe.La guía australiana (32) incluye el ensayo Quality in Acute Stroke Care (QASC) (33) en el que cuando se utiliza el tratamiento de la hiperglucemia > 11 mmol/L (o lo que es lo mismo, > 200 mg/dL) en las primeras 72 h (como parte de un paquete de medidas), se obtiene una mejora en los resultados a 90 días (157 pacientes menos con mortalidad o dependencia por 1000 pacientes tratados), aunque no se puede atribuir el efecto solo a dicha intervención.
Los estudios que evalúan la eficacia del tratamiento intensivo frente al grupo control demuestran que no se obtienen beneficios al marcarse niveles objetivos estrictos, además de aumentar los eventos adversos asociados al tratamiento.
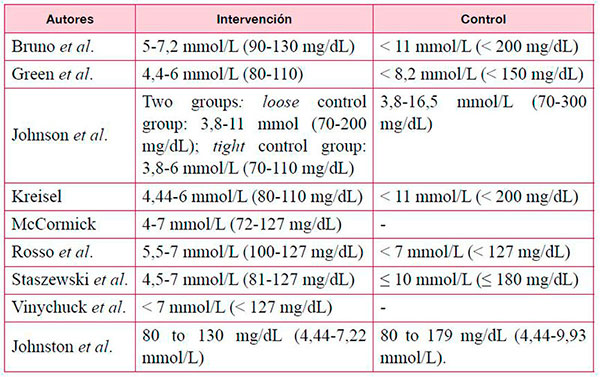
Los niveles objetivo que se marcan en los diferentes estudios son los siguientes:
En España, el estudio GLycemia in Acute Stroke study (GLIAS) (34) señaló que el valor de glucosa con mayor valor predictivo de un mal desenlace a los tres meses era de 155 mg/mL (S del 53 %; E del 73 %), que se asociaba con un aumento del riesgo de 2,7 veces de presentar muerte o dependencia (IC95 % del 1,42 a 5,24) tras ajustar por edad, diabetes, glucosa capilar al ingreso, volumen de infarto y gravedad basal del ictus, siendo el HR de muerte a los tres meses de 3,80 (IC95 % de 1,79 a 8,10).
En cuanto al efecto del tratamiento intensivo frente al convencional o no tratamiento, la quía de la ESO de 2018 (35), señala que, en personas con ictus isquémico, no se encuentran diferencias significativas en presentar un buen desenlace al final del seguimiento (ocho estudios; n=560; RR 1,09; IC95 % de 0,87 a 1,37) o mayor supervivencia (RR 0,99; IC95 % de 0,94 a 1,05) (35). Lo mismo ocurre con las personas con ictus hemorrágico, aunque solo se incluyó un único estudio (36), sin encontrar diferencias significativas en obtener un buen resultado al final del seguimiento (RR de 0,72; IC95 % de 0,14 a 3,61), mayor supervivencia (RR 0,81; IC9 5% de 0,4 a 1,65).
¿Cuál es la magnitud de los efectos no deseados esperados?
No se sabe.Los estudios que evalúan la eficacia del tratamiento intensivo frente al grupo control demuestran que no se obtienen beneficios al marcarse niveles objetivos estrictos, además de aumentar los eventos adversos asociados al tratamiento.
En cuanto al efecto del tratamiento intensivo frente al convencional o no tratamiento, la guía de la ESO de 2018 (35), señala que, en personas con ictus isquémico, aumenta el riesgo de hipoglucemia (ocho estudios; n=458; RR 4,75; IC95 % de 1,52 a 14,85) y de hipoglucemia sintomática (nueve estudios; n=491; RR 2,99; IC95 % de 0,95 a 9,40) (35), aunque no de forma significativa. Lo mismo ocurre con las personas con ictus hemorrágico, aunque solo se incluyó un único estudio (36), sin encontrar diferencias significativas en el riesgo de hipoglucemia (RR 3,2; IC95 % de 0,39 a 27,15).
¿Cuál es la calidad global de la evidencia sobre los efectos?
Muy baja.No hay estudios que comparen el efecto sobre los desenlaces clínicos del tratamiento de la hiperglucemia en función del nivel glucémico de partida, aunque existen estudios sobre el efecto del nivel de glucemia en los desenlaces de interés y estudios que demuestran que el tratamiento intensivo frente al convencional no obtiene beneficios.
Por ello, se considera que la calidad es muy baja.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantesNo se ha identificado evidencia al respecto.
El balance entre los efectos deseados y los no deseados esperados, ¿favorece la intervención o la comparación?
No se sabe.Se espera que, aunque no haya evidencia directa, la disminución de la hiperglucemia a partir del valor determinado tendrá más beneficios que riesgos, pero no se sabe con certeza.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad global de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
No se sabe.¿Es aceptable la opción para las partes interesadas?
No se sabe.¿Es factible la implementación de la opción?
No se sabe.Tablas GRADE
Resumen de la evidencia
Bibliografía
30. Kobayashi A, Czlonkowska A, Ford GA, Fonseca AC, Luijckx GJ, Korv J, et al. Euro-pean Academy of Neurology and European Stroke Organization consensus statement and practical guidance for pre-hospital management of stroke. Eur J Neurol. 2018;25(3):425-33. DOI: 10.1111/ene.13539
31. Nurmi J, Lindsberg PJ, Häppölä O, Klemetti E, Westerbacka J, Castrén M. Strict glucose control after acute stroke can be provided in the prehospital setting. Acad Emerg Med. 2011;18(4):436-9. DOI: 10.1111/j.1553-2712.2011.01020.x
32. Stroke Foundation. Clinical Guidelines for Stroke Management. Available at https://informme.org.au/guidelines/living-clinical-guidelines-for-stroke-management.
33. Middleton S, McElduff P, Ward J, Grimshaw JM, Dale S, D’Este C, et al. Implementation of evidence-based treatment protocols to manage fever, hyperglycaemia, and swallowing dysfunction in acute stroke (QASC): a cluster randomised controlled trial. Lancet. 2011;378(9804):1699-706. DOI: 10.1016/S0140-6736(11)61485-2
34. Fuentes B, Castillo J, San José B, Leira R, Serena J, Vivancos J, et al. The prognostic value of capillary glucose levels in acute stroke: the GLycemia in Acute Stroke (GLIAS) study. Stroke. 2009;40(2):562-8. DOI: 10.1161/STROKEAHA.108.519926
35. Fuentes B, Ntaios G, Putaala J, Thomas B, Turc G, Díez-Tejedor E. European Stroke Organisation (ESO) guidelines on glycaemia management in acute stroke. Eur Stroke J. 2018;3(1):5-21. DOI: 10.1177/2396987317742065
36. Green DM, O’Phelan KH, Bassin SL, Chang CW, Stern TS, Asai SM. Intensive versus conventional insulin therapy in critically ill neurologic patients. Neurocrit Care. 2010;13(3):299-306. DOI: 10.1007/s12028-010-9417-3
Manejo prehospitalario del ictus agudo: Antiagregantes
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Tratamiento antiagregante
¿Se debe iniciar tratamiento antiagregante de forma inmediata desde AP en personas con sospecha de ictus agudo?
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
1. No iniciar tratamiento antiagregante en personas con ictus antes de descartar hemorragia mediante una tomografía computarizada (TC) o resonancia magnética (RM).
Los efectos deseados de la intervención superan a los indeseables. Eso significa que la mayoría de los pacientes deberían recibir la intervención recomendada. LEER MÁS
2. Se recomienda iniciar tratamiento antiagregante en personas con ictus isquémico agudo tan pronto se descarte hemorragia intracraneal por técnicas de imagen.
Justificación
Se ha considerado seguir siendo prudentes y mantener la idea de no iniciar tratamiento antiagregante desde AP hasta no haber descartado mediante prueba de imagen la presencia de hemorragia intracraneal. De lo que sí hay evidencia es de que, una vez descartada la presencia de hemorragia intracraneal, el inicio de tratamiento antiagregante en personas con ictus isquémico agudo sí tiene beneficios en el paciente.
Justificación detallada
Calidad de la evidencia: la confianza en la evidencia es muy baja, puesto que se incluyó un subanálisis de los pacientes de los estudios International Stroke Trial (IST) y Chinese Acute Stroke Trial (CAST) en los que no se descartó hemorragia intracerebral antes de la aleatorización (37).
Balance entre beneficios y riesgos: el ácido acetilsalicílico (AAS) parecía reducir la incidencia de otros ictus (uno (0,3 %) vs. ocho (2,2 %)) (37) y no aumentaba el riesgo de sufrir otra hemorragia craneal sintomática, pero debido a la baja calidad de los datos y al principio de prudencia, se considera que no hay suficientes datos para señalar si el balance favorece o no la intervención.
Aceptabilidad: se cree que los profesionales no aceptarían iniciar tratamiento antiagregante sin haber descartado antes la presencia de hemorragia intracraneal.
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseados esperados?
Pequeños.En la versión anterior de la guía se incluyó un MA de datos individuales de los estudios IST y CAST que indicaba que el 22 % de los pacientes (n=773) de estos estudios fueron aleatorizados a recibir o no tratamiento antes de haberse realizado la TC, observando resultados similares a los de pacientes aleatorizados después de la prueba de imagen.
El riesgo general de presentar otro ictus o muerte fue alto (17 %). Sin embargo, el tratamiento con AAS parecía reducir la incidencia de otros ictus (uno (0,3 %) vs. ocho (2,2 %)) (37).
¿Cuál es la magnitud de los efectos no deseados esperados?
Pequeños.El AAS no aumentaba de forma significativa la incidencia de presentar otra hemorragia cerebral sintomática (29 (7,3 %) vs. 26 (6,9 %)) (37) en los pacientes que habían sido clasificados posteriormente como ictus hemorrágico.
Además, en personas con ictus isquémico en los que se ha descartado hemorragia intracerebral, el riesgo absoluto de hemorragia extracraneal importante era algo mayor con tratamiento antiagregante (cuatro casos más por 1000 (IC95 % de dos a seis más) (siete estudios; n=41042 pacientes; Peto OR de 1,69; IC95 % de 1,35 a 2,11), así como el riesgo de hemorragia intracraneal importante que fue de dos más por 1000 (de cero menos a cuatro más) (nueve estudios; n=41652; Peto OR de 1,18 (de 0,97 a 1,44).
¿Cuál es la calidad global en la evidencia sobre los efectos?
Muy baja.Los resultados se obtuvieron en un análisis de subgrupos de dos estudios de forma posterior. Asimismo, en cuanto a la evidencia del tratamiento antiagregante en personas con ictus isquémico en los que se ha descartado hemorragia intracraneal, la calidad de la evidencia es moderada.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran los desenlaces principales?
La incertidumbre o la variabilidad probablemente no sean importantes.No se ha identificado evidencia al respecto.
El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
No favorece ni la intervención ni la comparación.A pesar de que los estudios no demostraron un efecto negativo del AAS en personas con ictus hemorrágico, los datos se obtienen de un análisis posterior, y se señala que conviene ser prudentes al hablar de tratar con AAS a personas que pueden tener una hemorragia intracerebral. El balance en el caso de las personas en las que se ha descartado ictus hemorrágico sí es favorable al tratamiento antiagregante.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.¿Cuál es la calidad de la evidencia sobre la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
Probablemente no.No se han identificado estudios al respecto.
¿Es aceptable la opción para todas las partes interesadas?
Probablemente sí.No se han identificado estudios al respecto.
¿Es factible la implementación de la opción?
Probablemente sí.No se han incluido estudios al respecto.
Tablas GRADE
Bibliografía
37. Chen ZM, Sandercock P, Pan HC, Counsell C, Collins R, Liu LS, et al. Indications for early aspirin use in acute ischemic stroke : A combined analysis of 40 000 randomized patients from the chinese acute stroke trial and the international stroke trial. On behalf of the CAST and IST collaborative groups. Stroke. 2000;31(6):1240-9. DOI: 10.1161/01. str.31.6.1240
38. Minhas JS, Chithiramohan T, Wang X, Barnes SC, Clough RH, Kadicheeni M, et al. Oral antiplatelet therapy for acute ischaemic stroke. Cochrane Database Syst Rev. 2022;1(1):Cd000029. DOI: 10.1002/14651858.CD000029.pub4
39. Stroke Foundation. Clinical guidelines for stroke management. Chapter 3 of 8: acute medical and surgical management. Available at https://app.magicapp.org/#/guideline/QnoKGn.
¿Debe ser derivado de manera urgente a Atención Hospitalaria una persona con sospecha de AIT o ictus estable que refiere el inicio de los síntomas hace más de 48 horas?
Los efectos deseados de la intervención superan a los indeseables. Eso significa que la mayoría de los pacientes deberían recibir la intervención recomendada. LEER MÁS
1. Se recomienda la derivación urgente de la persona con sospecha de ictus o de AIT que acude al centro de AP en la ventana temporal entre las 48 horas hasta los primeros siete días desde el inicio de los síntomas.
Justificación
Los factores determinantes para esta recomendación han sido, por un lado, la evidencia de calidad moderada que señala el beneficio en la salud de las personas a las que va dirigida, y por otro, la reducción de los costes del manejo posterior del paciente. Por ello, queda justificado realizar una recomendación fuerte a favor.
Sin embargo, no se hace una recomendación de qué características tienen mayor o menor prioridad para dicha atención urgente, puesto que en general no se recomienda utilizar herramientas de cálculo de riesgo de recurrencia de estos pacientes.
Justificación detallada
Balance de beneficios y riesgos: la tasa de recurrencia a los siete días era de un 5,7 %, y a los 30 días, de un 6,3 %. A los 90 días, la tasa de recurrencia se situaba en un 7,4 % (40). En el estudio Effect of urgent treatment of transient ischaemic attack and minor stroke on early recurrent stroke (EXPRESS) entre el 74 % y el 82 % de los casos de recurrencia a los 90 días se dieron en la primera semana tras el inicio de los síntomas (41). Por otro lado, se sugiere que la atención y derivación urgente de las personas que han sufrido un AIT o un ictus leve tiene un alto impacto en evitar que se produzca un ictus recurrente, que se mantiene a largo plazo, pudiendo reducir el riesgo hasta en un 80 % (41).
Costes: se trata de una práctica coste-efectiva, puesto que se reducen las recurrencias y los ingresos hospitalarios, además del riesgo de presentar ictus fatal o discapacitante. Aun teniendo en cuenta los costes de implementación de un servicio que permita esta atención urgente, éste sería coste-efectivo (42, 43).
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseados esperados?
Moderado para el riesgo de sufrir un ictus recurrente en la primera semana tras el evento inicial, y grande para el impacto de la derivación e inicio urgente del tratamiento sobre los desenlaces de salud de las personas con sospecha de haber sufrido un AIT o con síntomas leves de ictus.
Incidencia de ictus recurrente en primera semana
Se han publicado varias RS y MA sobre el riesgo de recurrencia temprana de ictus en personas que consultan con sospecha de AIT. El último MA (40) compara los datos de recurrencia de estudios publicados en las últimas cinco décadas, observando que antes de 1999, la tasa de recurrencia a los dos días del inicio de los síntomas era del 3,4 %. A los siete días, la tasa era de un 5,7 %, y a los 30 días, de un 6,3 %. A los 90 días, la tasa de recurrencia se situaba en un 7,4 %. Entre el 74 % y el 82 % de los casos de recurrencia registrados a los 90 días se dieron en la primera semana tras el inicio de los síntomas, por lo que cualquier persona que acuda transcurridas las 48 horas desde el inicio de los síntomas, pero menos de una semana, debería ser tratado de forma urgente y ser visto por un especialista en ictus tan rápido como fuera posible.
Impacto de la derivación e inicio urgente de tratamiento
El único estudio que se ha identificado que compara la tasa de recurrencia de ictus antes y después de implementar un servicio de atención y tratamiento urgente de personas con sospecha de AIT o ictus leve (clínica de AIT), demuestra que dicho servicio disminuye hasta en un 80 % el riesgo de sufrir una recurrencia de ictus en los 90 días de seguimiento (41). Publicaciones posteriores han demostrado también que el efecto se mantiene en el tiempo, con un seguimiento realizado hasta diez años posteriores al inicio de los síntomas. Si se comparan los resultados obtenidos en la fase 2 del estudio (cuando se implementa el servicio de derivación y tratamiento urgente) frente a los obtenidos en la fase 1 (antes de implementar dicho servicio), se observa un menor riesgo de sufrir un ictus recurrente (HR 0,20; IC95 % de 0,08 a 0,49) y también un menor riesgo de sufrir un ictus fatal o discapacitante (OR 0,07; IC95 % de 0,01 a 0,50) o un ingreso por ictus recurrente (OR 0,21; IC95 % de 0,08 a 0,56) (42). Tras 10 años de seguimiento, el riesgo de recurrencia de ictus seguía siendo menor (HR 0,68; IC95 % de 0,48 a 0,95). Asimismo, los pacientes de la fase 2 presentaron una esperanza de vida ajustada a 10 años con descuento por discapacidad de 0,53 años más (IC95 % de 0,03 a 1,04) que los de la fase 1, y una esperanza de vida ajustada por calidad a los 10 años de 0,41 años de vida ajustados por calidad (AVAC) más en la fase 2 que en la fase 1 (43).
¿Cuál es la magnitud de los efectos no deseados esperados?
InsignificanteEn el estudio EXPRESS no se registra un aumento del riesgo de sangrado intestinal o intracerebral a los 90 días del inicio de los síntomas, por lo que la derivación e inicio urgente de tratamiento no parece tener efectos indeseables en los pacientes.
¿Cuál es la calidad global en la evidencia sobre los efectos?
Moderada.Las múltiples RS publicadas (40, 41, 45, 46) señalan que el riesgo de que se produzca un nuevo episodio de ictus en la primera semana tras el inicio de los síntomas de un AIT es alta, y se ha observado que la derivación e inicio urgente del tratamiento de personas que han sufrido un AIT o un ictus leve tiene un alto impacto en los desenlaces de interés, por lo que aunque se trata de un estudio observacional, se considera que la calidad de la evidencia global es moderada (41-43).
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran los desenlaces principales?
La incertidumbre o la variabilidad probablemente no sean importantes.No se han identificado estudios.
El balance entre los efectos deseables e indeseables esperados, ¿favorece a la intervención o a la comparación?
Favorece la intervención.Las diferencias en el riesgo de sufrir un ictus recurrente, e incluso letal o discapacitante, es muy grande tanto a los 90 días como a largo plazo. No se registran desenlaces indeseados por implementar un proceso de derivación y tratamiento urgente de personas con estos síntomas, por lo tanto, se cree que el balance favorece claramente la opción, incluso para aquellas que se encuentran entre las 48 horas y la semana de inicio de los síntomas.
¿Cuál es la magnitud de los recursos requeridos (costes)?
Costes y ahorros insignificantes.El estudio EXPRESS señala que en la fase 2 (fase en la que se implementa la derivación e inicio urgente de tratamiento) se redujeron los días de hospitalización, tanto por ictus recurrente (menor número de días de ingreso hospitalario (672 vs. 1957 días; p=0,017)), como por causas vasculares (427 vs. 1365 días; p=0,016). Así, se calculó un ahorro de 624 libras por persona (p=0,028) (42) en la fase 2 frente a la fase 1. A los 10 años, para la fase 2 el número de AVAC ganados fue de 5,06 y para la fase 1 de 4,65, diferencia igual a 0,41, estadísticamente significativa, P=0,034. (43). A los 10 años, se obtuvo un coste total para la fase 2 de 20399 $ y para la fase 1 de 19846 $, diferencia igual a 553 $, no estadísticamente significativa, P=0,80 (43).
En el estudio realizado por Luengo-Fernández et al. (43) se observó que para los pacientes de la fase 2 (en la que se implementa la derivación e inicio urgente de tratamiento), tanto la esperanza de vida, como la esperanza libre de discapacidad fueron superiores a la de los pacientes de la fase 1. Las diferencias encontradas para la esperanza de vida (5,87 vs. 5,58 años, diferencia de 0,29) no fueron estadísticamente significativas (P=0,082), mientras que las halladas para la esperanza de vida libre de discapacidad en años (4,02 vs. 3,49, diferencia de 0,53) sí lo fueron (P=0,043).
Con respecto a los costes, el de la clínica y el de las hospitalizaciones por causa no vascular fue superior para la fase 2 en comparación al de la fase 1 (755 vs. 582 $ y 15025 vs. 13786, respectivamente), siendo la diferencia encontrada para el coste de hospitalizaciones por causa no vascular (1239 $) no estadísticamente significativo (P=0,49), Por otro lado, el coste de las hospitalizaciones por causa vascular fue inferior para la fase 2 frente a la fase 1 (4619 vs. 5478 $), diferencia -860 $ no estadísticamente significativa (P=0,49).
¿Cuál es la certeza en torno a la evidencia sobre los recursos requeridos?
Moderada.La confianza en la evidencia se considera que es moderada-baja. Presenta problemas metodológicos importantes al no señalar la perspectiva del análisis y no reflejar específicamente ni justificar el horizonte temporal del análisis. Además, se observa que la validez externa del estudio es escasa debido a que se realiza con base en un estudio de comparación secuencial de base poblacional anidado y en un entorno clínico no existente en el SNS (43).
El coste-efectividad de la intervención, ¿favorece a la intervención o a la comparación?
Favorece la intervención.El coste adicional por AVAC ganado de la fase 2 frente a la fase 1 fue de 2103 $, por debajo de disponibilidad a pagar por año de vida ganado establecido en el estudio 29000 $ (43). El análisis de sensibilidad señaló una probabilidad del 93 % de que la fase 2 fuese coste-efectiva para un umbral de disponibilidad a pagar por AVAC ganado de 29000 $ (43).
¿Cuál sería el impacto en la equidad en salud?
Probablemente disminuiría.¿Es aceptable la opción para los grupos de interés implicados?
Probablemente sí.En la guía australiana se señala que las personas que han vivido la experiencia de haber sufrido un AIT o un ictus leve y sus familias han expresado la importancia de un acceso temprano a la valoración y el diagnóstico para prevenir un nuevo evento. Se enfatiza la necesidad de recibir educación a tiempo de los signos y síntomas de ictus, y explicaciones claras del riesgo de sufrir un nuevo ictus y la relevancia del tiempo en aquellos que presentan diferentes niveles de riesgo. El tiempo de espera puede ser estresante para estas personas y debería tenerse en cuenta (47).
¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
1. Grupo de Trabajo de la Guía de Práctica Clínica para el manejo de pacientes con Ictus en Atención Primaria. Guía de Práctica Clínica para el manejo de pacientes con Ictus en Atención Primaria. Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad y Política Social. Unidad de Evaluación de Tecnologías Sanitarias de la Agencia Laín Entralgo de la Comunidad de Madrid; 2009. Guías de Práctica Clínica en el SNS: UETS Nº 2007/5-2.
40. Shahjouei S, Sadighi A, Chaudhary D, Li J, Abedi V, Holland N, et al. A 5-Decade Analysis of Incidence Trends of Ischemic Stroke After Transient Ischemic Attack: A Systematic Review and Meta-analysis. JAMA Neurol. 2021;78(1):77-87. DOI: 10.1001/jamaneurol.2020.3627
41. Rothwell PM, Giles MF, Chandratheva A, Marquardt L, Geraghty O, Redgrave JN, et al. Effect of urgent treatment of transient ischaemic attack and minor stroke on early recurrent stroke (EXPRESS study): a prospective population-based sequential comparison. Lancet. 2007;370(9596):1432-42. DOI: 10.1016/S0140-6736(07)61448-2
42. Luengo-Fernandez R, Gray AM, Rothwell PM. Effect of urgent treatment for transient ischaemic attack and minor stroke on disability and hospital costs (EXPRESS study): a prospective population-based sequential comparison. Lancet Neurol. 2009;8(3):235-43. DOI: 10.1016/S1474-4422(09)70019-5
43. Luengo-Fernandez R, Li L, Silver L, Gutnikov S, Beddows NC, Rothwell PM. Long-Term Impact of Urgent Secondary Prevention After Transient Ischemic Attack and Minor Stroke: Ten-Year Follow-Up of the EXPRESS Study. Stroke. 2022;53(2):488-96. DOI: 10.1161/STROKEAHA.121.034279
44. Johnston SC, Rothwell PM, Nguyen-Huynh MN, Giles MF, Elkins JS, Bernstein AL, et al. Validation and refinement of scores to predict very early stroke risk after transient ischaemic attack. Lancet. 2007;369(9558):283-92. DOI: 10.1016/S0140-6736(07)60150-0
45. Giles MF, Rothwell PM. Risk of stroke early after transient ischaemic attack: a systematic review and meta-analysis. Lancet Neurol. 2007;6(12):1063-72. DOI: 10.1016/S1474-4422(07)70274-0
46. Mohan KM, Wolfe CD, Rudd AG, Heuschmann PU, Kolominsky-Rabas PL, Grieve AP. Risk and cumulative risk of stroke recurrence: a systematic review and meta-analysis. Stroke. 2011;42(5):1489-94. DOI: 10.1161/STROKEAHA.110.602615
47. Canadian Stroke Best Practices. Secondary Prevention Of Stroke. Triage and Initial Diagnostic Evaluation of Transient Ischemic Attack and Non-Disabling Stroke. 2020. Available at https://www.strokebestpractices.ca/recommendations/secondary-prevention-of-stroke/triage-and-initial-diagnostic-evaluation-of-transient-ischemic-attack-and-non-disabling-stroke.
Manejo del ictus tras el alta hospitalaria: Espasticidad
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Espasticidad
¿Los fármacos orales han demostrado ser eficaces en el tratamiento de la espasticidad post-ictus?
Los efectos no deseables probablemente son mayores que los efectos deseables, pero con una incertidumbre apreciable. Eso significa que la mayoría de los pacientes no deberían recibir la intervención recomendada. Cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere no utilizar fármacos orales como el baclofeno o la tizanidina para tratar la espasticidad focal post-ictus
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
2. Aquellas personas que presenten espasticidad que interfiera con su vida diaria deben ser enviados a consulta de neurología, rehabilitación y/o fisioterapia para que se valore el tratamiento más apropiado.
Justificación
Los factores determinantes para realizar esta recomendación han sido la muy baja confianza en la evidencia que existe sobre la eficacia y seguridad de estos fármacos en el tratamiento de la espasticidad post-ictus, así como la falta de un balance favorable entre los beneficios y los riesgos. De hecho, en ninguna de las comparaciones se observa una diferencia significativa en la mejora de la espasticidad.
Justificación detallada
Calidad de la evidencia: la confianza en la evidencia es muy baja. Solo se ha identificado un nuevo estudio en la actualización que compara el uso de la tolperisona frente a baclofeno, pero como se trata de un fármaco no financiado por el SNS, no se ha tenido en cuenta.
Balance entre beneficios y riesgos: los estudios incluidos tienen un tamaño muestral muy pequeño y no encuentran diferencias significativas de los fármacos frente a placebo ni entre ellos.
Costes: el coste de introducir tratamientos no efectivos supondrá siempre un gasto innecesario para la persona que ha sufrido un ictus y para el sistema sanitario.
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseables esperados?
- Comparación 1: Tizanidina vs. placebo: insignificante.
- Comparación 2: Tizanidina vs. Diazepam: insignificante.
- Comparación 3: Tizanidina vs. Baclofeno: insignificante.
- Comparación 1: Tizanidina vs. placebo: la tizanidina no mejora la puntuación de la escala de discapacidad (un estudio; DM -0,20; IC95 % de -0,90 a 0,50), ni la espasticidad (un estudio; n=40; OR 0,54; IC95 % de 0,14 a 2,11) (48).
- Comparación 2: Tizanidina vs. Diazepam: la distancia (en metros) que los pacientes pueden andar después de ocho semanas de tratamiento en una superficie lisa es menor en los tratados con tizanidina que en los que reciben diazepam (un estudio; n=79 pacientes; DM -183,30; IC95 % de -330,40 a -36,20), sin encontrar diferencias significativas en el porcentaje de pacientes en los que la espasticidad mejora (un estudio; n=78; OR 0,90; IC95 % de 0,37 a 2,20) (49).
- Comparación 3: Tizanidina vs. Baclofeno: no se han observado diferencias en el porcentaje de pacientes en los que la espasticidad mejora (un estudio; n=30; OR 2,36; IC95 % de 0,36 a 15,45) (50).
¿Cuál es la magnitud de los efectos indeseables esperados?
- Comparación 1: Tizanidina vs. placebo: moderada.
- Comparación 2: Tizanidina vs. Diazepam: pequeña.
- Comparación 3: Tizanidina vs. Baclofeno: insignificante.
- Comparación 1: Tizanidina vs. placebo: los efectos adversos son más frecuentes en el grupo tratado con tizanidina frente a placebo (un estudio; n=40; RR 1,72; IC95 % de 1,10 a 2,69) (48).
- Comparación 2: Tizanidina vs. Diazepam: se observa que en el grupo tratado con tizanidina el porcentaje de pacientes que abandona el estudio por efectos adversos es menor que en el grupo tratado con diazepam, aunque el intervalo de confianza al 95 % es impreciso e incluye al 1 (un estudio; n= 105; RR 0,42 (IC95 % de 0,18 a 1,01) (49).
- Comparación 3: Tizanidina vs. Baclofeno: no se observan diferencias en el número de pacientes con algún efecto adverso (un estudio; n=29 pacientes; RR 2,10; IC95 % de 0,36 a 15,45). Tampoco se observan diferencias en el porcentaje de pacientes que abandonan por efectos adversos (un estudio; n=29; RR 0,13; IC95 % de 0,01 a 2,38) (50).
¿Cuál es la certeza global de la evidencia sobre los efectos?
- Comparación 1: Tizanidina vs. placebo: baja.
- Comparación 2: Tizanidina vs. Diazepam: baja.
- Comparación 3: Tizanidina vs. Baclofeno: baja.
Se ha identificado un estudio para cada comparación y de pequeño tamaño, con posible riesgo de sesgos.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran los desenlaces principales?
Probablemente la incertidumbre o variabilidad no sean importantes.No se ha identificado evidencia al respecto.
El balance entre los efectos deseables e indeseables esperados, ¿favorece a la intervención o a la comparación?
- Comparación 1: Tizanidina vs. placebo: probablemente favorece la comparación.
- Comparación 2: Tizanidina vs. Diazepam: no favorece ni la intervención ni la comparación.
- Comparación 3: Tizanidina vs. Baclofeno: no favorece ni la intervención ni la comparación.
- Comparación 1: Tizanidina vs. placebo: probablemente no hay beneficio sobre la espasticidad y sí mayor probabilidad de sufrir efectos adversos frente a placebo.
- Comparación 2: Tizanidina vs. Diazepam: no hay diferencias en la eficacia entre los diferentes fármacos y aunque el porcentaje de personas que abandona el tratamiento por efectos adversos es mayor entre los tratados con diazepam frente a los tratados con tizanidina, la diferencia no parece ser estadísticamente significativa.
- Comparación 3: Tizanidina vs. Baclofeno: no parece haber diferencias en cuanto a la eficacia y la seguridad entre ambos tratamientos.
¿Cuál es la magnitud de los recursos requeridos (costes)?
Costes moderados.No se ha identificado evidencia sobre el uso de recursos y costes para el tratamiento con fármacos orales de la espasticidad focal post-ictus.
¿Cuál es la certeza en torno a la evidencia sobre los recursos requeridos?
No se han incluido estudios.No se ha identificado evidencia sobre al uso de recursos y costes para el tratamiento con fármacos orales de la espasticidad focal post-ictus.
El coste-efectividad de la intervención, ¿favorece a la intervención o a la comparación?
No se sabe.No se han identificado estudios de coste-efectividad sobre el tratamiento con fármacos orales de la espasticidad focal post-ictus.
¿Cuál sería el impacto en la equidad en salud?
No se sabe.¿Es aceptable la opción para los agentes implicados?
- Comparación 1: Tizanidina vs. placebo: probablemente no.
- Comparación 2: Tizanidina vs. Diazepam: probablemente no.
- Comparación 3: Tizanidina vs. Baclofeno: probablemente no.
¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
48. Simpson DM, Gracies JM, Yablon SA, Barbano R, Brashear A. Botulinum neurotoxin versus tizanidine in upper limb spasticity: a placebo-controlled study. J Neurol Neurosurg Psychiatry. 2009;80(4):380-5. DOI: 10.1136/jnnp.2008.159657
49. Bes A, Eyssette M, Pierrot-Deseilligny E, Rohmer F, Warter JM. A multi-centre, double-blind trial of tizanidine, a new antispastic agent, in spasticity associated with hemiplegia. Curr Med Res Opin. 1988;10(10):709-18. DOI: 10.1185/03007998809111122
50. Medici M, Pebet M, Ciblis D. A double-blind, long-term study of tizanidine (‘Sirdalud’) in spasticity due to cerebrovascular lesions. Curr Med Res Opin. 1989;11(6):398-407. DOI: 10.1185/03007998909110141
Manejo del ictus tras el alta hospitalaria: Dolor central-post-ictus
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Dolor central post-ictus
¿Qué fármacos son eficaces en el tratamiento del dolor central post-ictus?
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. En el tratamiento del dolor centrar post-ictus se sugiere la utilización de amitriptilina como fármaco de primera línea, teniendo siempre en cuenta los efectos secundarios asociados a su uso y estableciendo el balance riesgo/ beneficio en cada caso.
2. Como alternativa a amitriptilina en el tratamiento del dolor central post-ictus se sugiere el uso de lamotrigina, si bien se debe tener en cuenta la posible aparición de efectos secundarios.
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
3. Se recomienda derivar a la persona con dolor central post-ictus no controlado en AP a unidades especializadas en el manejo del dolor.
Justificación
Aunque la evidencia es de baja o muy baja calidad, tanto amitriptilina como lamotrigina tienen efectos sobre la reducción del dolor, aunque no están exentos de efectos adversos, que hacen abandonar el tratamiento con mayor frecuencia en el caso de la lamotrigina.
Además, la amitriptilina tiene menor coste por DDD que la lamotrigina y los demás medicamentos.
Justificación detallada
Calidad de la evidencia: la calidad global es baja o muy baja para todas las comparaciones, debido a riesgo de sesgo de los estudios incluidos, al pequeño tamaño de los estudios y a la imprecisión de los resultados.
Balance entre beneficios y riesgos: los únicos fármacos en los que el balance podría favorecer a la intervención son la amitriptilina y en segundo lugar la lamotrigina, puesto que el dolor se reduce de forma significativa en estos casos, aunque hay un mayor número de efectos adversos, sobre todo en el caso de la lamotrigina, donde aumenta el número de abandonos por los mismos.
Costes: el coste de DDD es menor para la amitriptilina.
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseados esperados?
- Amitriptilina vs. placebo: moderados.
- Pregabalina vs. placebo: pequeños.
- Carbamazepina vs. placebo: insignificantes.
- Lamotrigina vs. placebo: moderados.
- Levetiracetam vs. placebo: insignificantes.
- Amitriptilina vs. Carbamazepina: insignificantes.
- Amitriptilina vs. placebo: aumenta el porcentaje de pacientes con una mejora en la reducción del dolor a las cuatro semanas de tratamiento (un estudio; n=30 pacientes; RR 10, IC95 % de 1,46 a 68,69) (51).
- Pregabalina vs. placebo: el efecto del tratamiento con pregabalina frente a placebo sobre el dolor es controvertido, puesto que en un estudio éste disminuye de forma significativa (DM 2,18; IC95 % de 0,57 a 3,80) (52) y en otro no (DM de LS -02; IC95 % de -0,7 a 0,4) (53). En cuanto a la calidad de vida medida por EQ 5D-VAS, en un estudio no se observan diferencias entre grupos y en el segundo, parece que es mejor en el grupo tratado con pregabalina.
- Carbamazepina vs. placebo: no se encontraron diferencias significativas en la reducción del dolor en el grupo tratado con carbamazepina frente al placebo (un estudio; n=29; RR 5,36, IC95 % de 0,71 a 40,37 (51).
- Lamotrigina vs. placebo: aumenta el porcentaje de pacientes con una mejora en la reducción del dolor a las ocho semanas (un estudio; n=30; RR 4, IC95 % de 1,27 a 12,60) (54).
- Levetiracetam vs. placebo: el tratamiento con levetiracetam no se asoció con una mejora significativa del dolor espontáneo o evocado (ni con cualquier otro desenlace secundario de interés) (55).
- Amitriptilina vs. Carbamazepina: no encuentran diferencias significativas en la reducción del dolor al final del tratamiento (un estudio; n=29; RR 1,87, IC95 % de 0,85 a 4,11) (51).
¿Cuál es la magnitud de los efectos no deseados esperados?
- Amitriptilina vs. placebo: pequeños.
- Pregabalina vs. placebo: insignificantes.
- Carbamazepina vs. placebo: pequeños.
- Lamotrigina vs. placebo: insignificantes.
- Levetiracetam vs. placebo: insignificantes.
- Amitriptilina vs. Carbamazepina: insignificantes.
- Amitriptilina vs. placebo: el riesgo de presentar algún efecto adverso es mayor en los pacientes que reciben amitriptilina frente a placebo (un estudio; n=30; RR 2, IC95 % de 1,15 a 3,49), aunque no efectos adversos moderados o graves (un estudio; n=30; RR 2, IC95 % de 0,20 a 19,78) (51).
- Pregabalina vs. placebo: no hay diferencias significativas en los pacientes que abandonan el tratamiento por efectos adversos en el grupo que recibe pregabalina (dos estudios; n=259; RR 1,65; IC9 5% de 0,67 a 4,08), ni en el número de pacientes que presenta algún efecto adverso (52, 53).
- Carbamazepina vs. placebo: no hubo diferencias en el porcentaje de pacientes con efectos adversos de moderados a graves (un estudio; n=29; RR 5,36, IC95 % de 0,71 a 40,37), aunque sí más pacientes con algún efecto adverso en el grupo tratado con carbamazepina (un estudio; n=29; RR 1,99, IC95 % de 1,14 a 3,48) (51).
- Lamotrigina vs. placebo: un mayor número de pacientes abandona el tratamiento por efectos adversos, aunque no de forma significativa (un estudio; n=30; RR 7, IC95 % de 0,38 a 129,35) y sin diferencias en el porcentaje de pacientes que presenta efectos adversos (54).
- Levetiracetam vs. placebo: hubo un aumento en la frecuencia de los efectos adversos reportados (un estudio; n=33; RR 5, IC95 % de 0,62 a 40,51), aunque no de forma significativa (55).
- Amitriptilina vs. Carbamazepina: no hay diferencias en el porcentaje de pacientes que presenta algún efecto adverso (un estudio; n=29; RR 1,01, IC95 % de 0,82 a 1,23) y tampoco en el porcentaje de pacientes con efectos adversos moderados a graves (un estudio; n=29; RR 0,37, IC95 % de 0,09 a 1,62) (51).
¿Cuál es la calidad global de la evidencia sobre los efectos?
- Amitriptilina vs. placebo: muy baja.
- Pregabalina vs. placebo: muy baja.
- Carbamazepina vs. placebo: muy baja.
- Lamotrigina vs. placebo: baja.
- Levetiracetam vs. placebo: muy baja.
- Amitriptilina vs. Carbamazepina: muy baja.
En casi todas las comparaciones se cuenta con un único estudio y con muy pocas personas, lo que hace que la evidencia que existe sea de muy baja calidad. En algunos casos, aunque los RR sean altos, los intervalos de confianza incluyen el no efecto y los bordes del intervalo son extremadamente amplios, lo que impide establecer diferencias significativas, sobre todo en el caso de los efectos adversos. Por ello, la certeza global en la evidencia es muy baja en todos los casos.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran la importancia de los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantes.No se ha identificado evidencia al respecto.
El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
- Amitriptilina vs. placebo: probablemente favorece la opción.
- Pregabalina vs. placebo: no se sabe.
- Carbamazepina vs. placebo: probablemente favorece la opción.
- Lamotrigina vs. placebo: probablemente favorece la opción.
- Levetiracetam vs. placebo: no se sabe.
- Amitriptilina vs. Carbamazepina: no se sabe.
Aunque la evidencia es de baja o muy baja calidad, tanto amitriptilina como lamotrigina tienen efectos sobre la reducción del dolor, aunque no están exentos de efectos adversos, que hacen abandonar el tratamiento con mayor frecuencia en el caso de la lamotrigina. El resto de los tratamientos no parecen tener efectos significativos sobre el dolor.
¿Cuál es la magnitud de los recursos requeridos (costes)?
Costes moderados.No se ha identificado evidencia sobre el uso de recursos y costes para el tratamiento con fármacos orales de la espasticidad focal post-ictus.
¿Cuál es la calidad global de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.No se ha identificado evidencia sobre el uso de recursos y costes para el tratamiento con fármacos del dolor central post-ictus.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad sobre el tratamiento con fármacos del dolor central post-ictus.
¿Cuál sería el impacto en la equidad en salud?
No se sabe.¿Es la intervención aceptable para todas las partes interesadas?
Probablemente no.¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
51. Leijon G, Boivie J. Central post-stroke pain–a controlled trial of amitriptyline and carbamazepine. Pain. 1989;36(1):27-36. DOI: 10.1016/0304-3959(89)90108-5
52. Vranken JH, Dijkgraaf MG, Kruis MR, van der Vegt MH, Hollmann MW, Heesen M. Pregabalin in patients with central neuropathic pain: a randomized, double-blind, placebo-controlled trial of a flexible-dose regimen. Pain. 2008;136(1-2):150-7. DOI: 10.1016/j.pain.2007.06.033
53. Kim JS, Bashford G, Murphy KT, Martin A, Dror V, Cheung R. Safety and efficacy of pregabalin in patients with central post-stroke pain. Pain. 2011;152(5):1018-23. DOI: 10.1016/j.pain.2010.12.023
54. Vestergaard K, Andersen G, Gottrup H, Kristensen BT, Jensen TS. Lamotrigine for central poststroke pain: a randomized controlled trial. Neurology. 2001;56(2):184-90. DOI: 10.1212/wnl.56.2.184
55. Jungehulsing GJ, Israel H, Safar N, Taskin B, Nolte CH, Brunecker P, et al. Levetiracetam in patients with central neuropathic post-stroke pain–a randomized, double-blind, placebo-controlled trial. Eur J Neurol. 2013;20(2):331-7.DOI: 10.1111/j.1468-1331.2012.03857.x
Manejo del ictus tras el alta hospitalaria: Disfagia
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Evaluación de la disfagia en AP
¿Cómo debe realizarse la evaluación de la disfagia desde AP?
Los efectos deseados de la intervención superan a los indeseables. Eso significa que la mayoría de los pacientes deberían recibir la intervención recomendada. LEER MÁS
1. Se recomienda descartar la presencia de disfagia lo antes posible y detectar si existen problemas nutricionales asociados.
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
2. Se sugiere la prueba de deglución de agua para el cribado de aspiración en AP, teniendo en cuenta ante todo las características de la persona que ha sufrido el ictus y su disponibilidad.
La realización de esta prueba debería acompañarse de una valoración clínica previa observando la calidad de la voz, si la persona puede sacar la lengua y moverla de un lado al otro o si siente la parte posterior de la pared de la garganta si se le toca. Esta valoración puede mejorar la capacidad de detección de los casos.
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
3. Reevaluar la presencia de disfagia tras el alta hospitalaria y realizar un seguimiento periódico por el equipo de AP.
4. Aquellas personas con ictus en las que se detecten por primera vez dificultades en la deglución (generales, durante o tras la deglución) deben ser evaluadas por el especialista correspondiente.
5. Entrenar a las personas en las que persistan las dificultades al tragar y a sus cuidadores en la identificación y manejo de los problemas en la deglución.
6. Las personas con disfagia persistente tras un ictus deben ser monitorizadas una vez dadas de alta, de manera regular, pesándolas regularmente, asegurando que no estén desnutridas, para valorar la necesidad de cambios en la dieta y/o en la vía de alimentación.
Justificación
Se ha realizado una recomendación débil a favor del uso del test de deglución de agua, puesto que se trata de una prueba fácil de realizar en AP, y aunque no sea muy específica, puede ser suficientemente sensible para detectar la mayoría de los casos de disfagia en aquellas personas que han sufrido un ictus. Además, aunque no se cuente con evidencia directa del impacto que puede tener la implementación del cribado de disfagia en AP, sí contamos con evidencia del contexto del ámbito hospitalario agudo, donde éste sí tiene efectos positivos en los desenlaces de las personas que han sufrido un ictus.
No se ha realizado una recomendación sobre el uso de la herramienta EAT-10, puesto que, aunque se ha descrito que puede ser utilizada para el cribado de la disfagia, no presenta buenos resultados en pacientes con ictus, por lo que, a pesar de su facilidad de uso, no se ha formulado una recomendación al respecto.
Justificación detallada
Calidad de la evidencia: son pocos los estudios que existen, y se puede decir que la calidad de la evidencia es baja para las pruebas de cribado de disfagia mediante la prueba de deglución de agua. En cuanto a la herramienta EAT-10, existe incertidumbre en la fiabilidad de la herramienta cuando se trata de detectar disfagia en personas que han sufrido un ictus.
Balance entre beneficios y riesgos: el cribado de la disfagia en el hospital, aunque no sea el contexto que se está evaluando, reduce el riesgo de desenlaces negativos en personas que han sufrido un ictus y pueden presentar disfagia. El uso de la prueba de deglución de agua, junto con la clínica, son los que mejores resultados de S y E tienen. En el caso de la EAT-10, aunque los resultados para el cribado de disfagia en población de riesgo son buenos, cuando se trata de personas que han sufrido un ictus, los resultados que se obtienen no lo son tanto.
Aceptabilidad: la prueba puede no ser aceptada por todas las personas. Un cuestionario auto cumplimentado podría tener mayor aceptabilidad.
De la evidencia a la recomendación
Para el cribado de disfagia por la prueba de deglución de agua
¿Cómo de válida es la prueba?
Válida.Son pocos los estudios identificados fuera del contexto hospitalario agudo que hacen referencia a las pruebas de deglución de agua, acompañadas o no de una valoración clínica previa.
La S y E de detectar aspiración al utilizar volúmenes de agua inferiores a 60 ml es baja, siendo la S y E al utilizar un volumen de 60 ml de 55,7 %, y de 85,4 %, respectivamente (56), La presencia de una velocidad de deglución anormal o de asfixia tras la ingesta de 100 ml de agua tuvo una S y E del 85,5 % y del 50 %, respectivamente en el primer caso, y del 47,8 % y 91,7 % en el segundo (57).
Cuando se suma una valoración clínica previa a la prueba de deglución de agua para valorar la presencia de tos o de cambios en la vocalización o respiración (58) o de aspiración (59), se obtienen mejores resultados, con una S del 93,3 % o 89,1 % respectivamente, y una E del 87,7 % u 80,8 %. En personas que han sufrido un ictus y se encuentran en rehabilitación, la utilización del Toronto Bedside Swallowing Screening Test (TOR-BSST) (que incluye una serie de preguntas clínicas y un test de deglución con 10 cucharadas de 5 ml de agua), tiene una S del 89,5 % y una E del 68 % (60).
¿Cuál es la magnitud de los efectos deseados esperados?
No se sabe.No se han identificado estudios.
¿Cuál es la magnitud de los efectos no deseados esperados?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad global de la evidencia sobre la validez de la prueba?
Baja.Hay mucha heterogeneidad en las características de la prueba, y los datos de S y E son variables.
¿Cuál es la calidad global de la evidencia para cualquier beneficio directo importante o crítico, de efectos adversos o la carga de la prueba?
Estudios no incluidos.No se han identificado estudios.
¿Cuál es la calidad global de la evidencia sobre el efecto que tienen los resultados de la prueba en el manejo del paciente?
Estudios no incluidos.No hay evidencia directa, pero sí indirecta en referencia a realizar cribado y su impacto en resultados de salud.
¿Cómo de cierta es la relación entre los resultados de la prueba y las decisiones sobre el manejo del paciente?
Estudios no incluidos.No se han identificado estudios.
¿Cuál es la calidad global de la evidencia sobre los efectos de la prueba?
Baja.Aunque no haya evidencia directa del efecto del cribado de la disfagia en los desenlaces de la persona que ha sufrido un ictus en el ámbito de la AP, se tiene evidencia de la S del cribado en este contexto y evidencia indirecta sobre los efectos beneficiosos de la realización del cribado de disfagia en las personas con ictus agudo en el contexto hospitalario.
¿Hay incertidumbre o variabilidad importante en cómo valoran los pacientes la importancia de los desenlaces de interés?
Probablemente incertidumbre o variabilidad no importantes.No se han identificado estudios.
¿El balance entre los efectos deseados y no deseados favorece la intervención o la comparación?
Probablemente favorece la intervención.Como se ha señalado anteriormente, el cribado de la disfagia en el contexto agudo hospitalario tiene efectos beneficiosos en los desenlaces de interés de las personas que han sufrido un ictus y en nuestro contexto, la aplicación de la prueba de deglución de agua puede ayudar a detectar casos de disfagia en las personas que han sido dados de alta y acuden a AP para su seguimiento, lo que probablemente también tenga un beneficio en los desenlaces de interés para el paciente.
¿Cómo de altos son los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.No se han identificado estudios al respecto.
¿El coste-efectividad favorece la intervención o la comparación?
No se sabe.No se han identificado estudios.
¿Cuál sería el impacto sobre la equidad en la salud?
Probablemente aumentaría.No se han identificado estudios al respecto.
¿Es la intervención aceptable para todas las partes interesadas?
Probablemente síNo se han identificado estudios al respecto.
¿Es factible la implementación de la intervención?
Probablemente sí.No se han identificado estudios al respecto.
Para la herramienta de autocumplementación EAT-10
¿Cómo de válida es la prueba?
No válida.Bartlett R et al. (63) observan una correlación moderada entre las puntuaciones de la EAT-10 y PAS en pacientes con cáncer de cabeza y cuello (con déficit estructurales), pero una correlación débil en el caso de personas con Parkinson o ictus (con deficiencias neurológicas), señalando que los déficits neurosensoriales pueden jugar un papel en la percepción de la disfagia por parte de estas personas. En la muestra total, la correlación fue moderada (r=0,50), siendo el resultado similar al obtenido en la validación de la versión española de EAT-10 por Giraldo-Cadavid et al. (r=0,59) (64). En esa validación (64), solo el 37 % de las personas incluidas presentaba enfermedad vascular y no se realizó un análisis de subgrupos por tipo de paciente. En la revisión de Zhang et al. (65) se señala que, a pesar de que un análisis Rasch revela que los ítems 2, 7 y 10 no contribuyen al constructo general de la EAT-10 (66), existe una correlación lineal entre la EAT-10 y las puntuaciones PAS. Los estudios que incluyen señalan que, utilizando un punto de corte de 3, la precisión diagnóstica es mejor (65). Sin embargo, solo uno de los estudios incluidos en esta revisión es en personas con ictus agudo (67), y se trata además del estudio que peores datos de S presenta para detectar disfagia.
Speyer et al. (68) realizan un análisis de las propiedades del EAT-10 que obtiene una puntuación baja en cada ítem frente al análisis que hicieron los autores de la herramienta (69) donde señalaban que el instrumento presentaba una excelente consistencia interna, una reproducibilidad test-retest y criterion-based validity, y donde se sugería un valor de tres como punto de corte.
¿Cuál es la magnitud de los efectos deseados esperados?
No se sabe.No se han identificado estudios en personas con ictus que proporcionen resultados de S y E, aunque los datos de correlación que se proporcionan señalan que la prueba tiene peores resultados cuando se aplica en personas que han sufrido un ictus.
¿Cuál es la magnitud de los efectos no deseados esperados?
No se sabe.No se han identificado estudios que proporcionen resultados de FP y FN en personas con ictus, aunque los datos de correlación que se proporcionan señalan que la prueba tiene peores resultados cuando ésta se aplica en personas que han sufrido un ictus.
¿Cuál es la calidad global de la evidencia sobre la validez de la prueba?
Baja.Los estudios incluyen todo tipo de pacientes, y cuando se hace un estudio de correlación se observa que precisamente las personas con ictus eran las que peores resultados obtienen para la prueba (63).
¿Cuál es la calidad global de la evidencia para cualquier beneficio directo importante o crítico, efectos adversos o carga de la prueba?
Estudios no incluidos.No se ha identificado evidencia directa sobre el beneficio directo importante de la prueba.
¿Cuál es la calidad global de la evidencia sobre el efecto que tienen los resultados de la prueba en el manejo del paciente?
Estudios no incluidos.No se han identificado estudios que indiquen cuál es el procedimiento a seguir una vez se conozcan los resultados de la prueba y el impacto que esto tiene en los desenlaces del paciente.
¿Cómo de cierta es la relación entre los resultados de la prueba y las decisiones sobre el manejo del paciente?
Estudios no incluidosNo se han identificado estudios que analicen la relación directa.
¿Cuál es la calidad global de la evidencia sobre los efectos de la prueba?
Baja.No hay evidencia directa sobre el efecto del cribado de disfagia en AP mediante herramientas de autocumplimentación en los desenlaces del paciente, aunque sí se tiene evidencia indirecta en el contexto hospitalario agudo sobre el cribado de disfagia en personas que han sufrido un ictus y el efecto sobre los desenlaces clínicos de interés.
¿Hay incertidumbre o variabilidad en cómo valoran los pacientes la importancia de los desenlaces principales?
Probablemente incertidumbre o variabilidad no importantes.¿El balance entre los efectos deseados y no deseados favorece la intervención o la comparación?
No favorece la intervención ni la comparación.La utilización de la herramienta de auto cumplimentación EAT-10 en personas con ictus obtiene peores resultados (peor correlación con el diagnóstico de disfagia) que en otro tipo de pacientes en los que se sospecha de disfagia. Esto significa que probablemente al aplicar esta herramienta en personas con ictus se escapen casos de disfagia y puede que se diagnostique con disfagia a personas que no la presentan en realidad.
¿Cómo de altos son los recursos requeridos (costes)?
No se sabe.No se han identificado estudios al respecto.
¿Cuál es la calidad global de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.No se han identificado estudios al respecto.
¿Favorece el coste-efectividad la intervención o la comparación?
No se sabe.No se han identificado estudios al respecto.
¿Cuál sería el impacto sobre la equidad en salud?
Probablemente reduciría.¿Es la intervención aceptable para las partes interesadas?
Probablemente sí.No se han identificado estudios al respecto.
¿Es factible la implementación de la intervención?
Probablemente sí.No se han identificado estudios al respecto.
Bibliografía
56. Osawa A, Maeshima S, Tanahashi N. Water-swallowing test: screening for aspiration in stroke patients. Cerebrovasc Dis. 2013;35(3):276-81. DOI: 10.1159/000348683
57. Wu MC, Chang YC, Wang TG, Lin LC. Evaluating swallowing dysfunction using a 100- ml water swallowing test. Dysphagia. 2004;19(1):43-7. DOI: 10.1007/s00455-003-0030-x
58. Momosaki R, Abo M, Kakuda W, Kobayashi K. Applicability of the two-step thickened water test in patients with poststroke dysphagia: a novel assessment tool for paste food aspiration. J Stroke Cerebrovasc Dis. 2013;22(6):817-21. DOI: 10.1016/j.jstrokecerebrovasdis.2012.05.011
59. Zhou Z, Salle J, Daviet J, Stuit A, Nguyen C. Combined approach in bedside assessment of aspiration risk post stroke: PASS. Eur J Phys Rehabil Med. 2011;47(3):441-6.
60. Martino R, Silver F, Teasell R, Bayley M, Nicholson G, Streiner DL, et al. The Toronto Bedside Swallowing Screening Test (TOR-BSST): development and validation of a dysphagia screening tool for patients with stroke. Stroke. 2009;40(2):555-61. DOI: 10.1161/STROKEAHA.107.510370
61. Brodsky MB, Suiter DM, González-Fernández M, Michtalik HJ, Frymark TB, Venediktov R, et al. Screening Accuracy for Aspiration Using Bedside Water Swallow Tests: A Systematic Review and Meta-Analysis. Chest. 2016;150(1):148-63. DOI: 10.1016/j. chest.2016.03.059
62. Osawa A, Maeshima S, Matsuda H, Tanahashi N. Functional lesions in dysphagia due to acute stroke: discordance between abnormal findings of bedside swallowing assessment and aspiration on videofluorography. Neuroradiology. 2013;55(4):413-21. DOI: 10.1007/s00234-012-1117-6
63. Bartlett RS, Kenz MK, Wayment HA, Thibeault SL. Correlation Between EAT-10 and Aspiration Risk Differs by Dysphagia Etiology. Dysphagia. 2022;37(1):11-20. DOI: 10.1007/s00455-021-10244-0
64. Giraldo-Cadavid LF, Gutiérrez-Achury AM, Ruales-Suárez K, Rengifo-Varona ML, Barros C, Posada A, et al. Validation of the Spanish Version of the Eating Assessment Tool-10 (EAT-10spa) in Colombia. A Blinded Prospective Cohort Study. Dysphagia. 2016;31(3):398-406. DOI: 10.1007/s00455-016-9690-1
65. Zhang PP, Yuan Y, Lu DZ, Li TT, Zhang H, Wang HY, et al. Diagnostic Accuracy of the Eating Assessment Tool-10 (EAT-10) in Screening Dysphagia: A Systematic Review and Meta-Analysis. Dysphagia. 2023;38(1):145-58. DOI: 10.1007/s00455-022-10486-6
66. Cordier R, Joosten A, Clavé P, Schindler A, Bülow M, Demir N, et al. Evaluating the Psychometric Properties of the Eating Assessment Tool (EAT-10) Using Rasch Analysis. Dysphagia. 2017;32(2):250-60. DOI: 10.1007/s00455-016-9754-2
67. Wang R, Xiong X, Zhang C, Fan Y. [Reliability and validity of the Chinese Eating Assessment Tool (EAT-10) in evaluation of acute stroke patients with dysphagia]. Zhong Nan Da Xue Xue Bao Yi Xue Ban. 2015;40(12):1391-9. DOI: 10.11817/j.issn.1672-7347.2015.12.017
68. Speyer R, Cordier R, Kertscher B, Heijnen BJ. Psychometric properties of questionnaires on functional health status in oropharyngeal dysphagia: a systematic literature review. Biomed Res Int. 2014;2014:458678. DOI: 10.1155/2014/458678
69. Belafsky PC, Mouadeb DA, Rees CJ, Pryor JC, Postma GN, Allen J, et al. Validity and reliability of the Eating Assessment Tool (EAT-10). Ann Otol Rhinol Laryngol. 2008;117(12):919-24. DOI: 10.1177/000348940811701210
Plan terapéutico en el domicilio
¿Qué plan terapéutico puede realizarse en el domicilio? (Dietas (espesantes), ejercicios…)
Dieta
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere proporcionar una dieta adecuada a aquellas personas con ictus que presentan disfagia y son alimentadas por vía oral.
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
2. Revisar periódicamente su situación para ir adaptando la dieta al estado de la persona en las visitas regulares de seguimiento (tres, seis, 12 meses) o siempre que haya un cambio funcional en el mismo.
Justificación
Se ha realizado una recomendación débil a favor de adecuar la dieta de las personas con ictus que presentan disfagia, pero no se mencionan las texturas ni el uso de los espesantes, debido a la falta de evidencia al respecto y a los efectos negativos que estas restricciones pueden tener en la calidad de vida de estas personas. Se señala la importancia de revisar periódicamente su situación para realizar modificaciones siempre que se detecten cambios en la misma (disminución o aumento de las restricciones de la dieta en función al estado del paciente).
Justificación detallada
Calidad de la evidencia: la calidad de la evidencia es muy baja.
Balance riesgos beneficios: no hay diferencias significativas en las variables de interés, salvo el número de días en el hospital, que es mayor para aquellos que no llevan una dieta modificada.
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseados esperados?
Pequeña.En la guía de la ESO y la European Society for Swallowing Disorders (ESSD) (70), se recoge que en pacientes con una dieta modificada, no hubo diferencias significativas en la aparición de neumonía post-ictus (cuatro estudios; n=100 pacientes; RR 0,19, IC95 % de 0,03 a 1,4), ni en el riesgo de penetración (un estudio, n=122 pacientes; RR 0,06; IC95 % de 0,00 a 1,00); calidad baja), aspiración (tres estudios; n=188; RR 0,51 IC95 % de 0,14 a 1,77; calidad muy baja) frente al grupo control. El único desenlace significativo fue la diferencia en el número de días de ingreso hospitalario, que fue de 9,58 días menos (IC95 % de 15 a 3,76 menos; calidad baja) que en el grupo control.
¿Cuál es la magnitud de los efectos no deseados esperados?
Insignificante.En la guía de la ESO y la ESSD (70), se recoge que, en pacientes con una dieta modificada, no hubo diferencias significativas en la ingesta de líquidos (tres estudios; n=77 pacientes; DM de -133,22 ml; IC95 % de -541,9 a 275,46; calidad baja) frente al grupo control.
¿Cuál es la calidad global de la evidencia sobre los efectos?
Muy baja.Aunque para algunos desenlaces la calidad es baja, para la aspiración es muy baja, por lo que la calidad global se define como muy baja.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran los desenlaces principales?
La incertidumbre o la variabilidad probablemente no sean importantes.El balance entre los efectos deseables e indeseables esperados, ¿favorece a la intervención o a la comparación?
No se sabe.No hay diferencias significativas en las variables de interés, salvo el número de días en el hospital, que es mayor para aquellos que no llevan una dieta modificada.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad de la evidencia sobre sobre los recursos requeridos?
No se han incluido estudios.No se han identificado estudios.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
Probablemente sí.Una RS (71) encuentra dos estudios: el primero un análisis de ahorro de costes realizado en EE. UU. (72) y el otro un modelo basado en el análisis de coste-utilidad en Polonia (73). El uso de un espesante a base de goma para modificar la textura de la dieta era coste-efectiva desde el punto de vista del pagador público en Polonia (ratio incremental de coste-utilidad de 21387 PLN a 20977 PLN por QALY ganado, o sobre 4750–4660 €, por debajo del límite establecido en Polonia de 147,024 PLN por AVAC) (73). El otro estudio encuentra que los líquidos espesados preparados comercialmente son más consistentes y menos caros que los que se preparaban in situ (de 44 a 59 %) desde la perspectiva hospitalaria en los EE. UU. (72).
¿Cuál sería el impacto en la equidad en salud?
No se sabe.¿Es aceptable la opción para todas las partes interesadas?
Varía.La RS de estudios cualitativos sobre el impacto de la textura de la dieta en la calidad de vida de la persona que ha sufrido un ictus (74), se observa que aunque la gravedad de la disfagia puede ser un factor de confusión, la modificación del bolo alimenticio tiene un impacto negativo sobre la calidad de vida relacionada con la salud, encontrando que cuanto más se modifica la textura de los alimentos y líquidos, menor es la calidad de vida de la persona que ha sufrido el ictus (74).
¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
70. Dziewas R, Michou E, Trapl-Grundschober M, Lal A, Arsava EM, Bath PM, et al. Euro-pean Stroke Organisation and European Society for Swallowing Disorders guideline for the diagnosis and treatment of post-stroke dysphagia. Eur Stroke J. 2021;6(3):Lxxxixcxv. DOI: 10.1177/23969873211039721
71. Marin S, Ortega O, Serra-Prat M, Valls E, Pérez-Cordón L, Clavé P. Economic Evaluation of Clinical, Nutritional and Rehabilitation Interventions on Oropharyngeal Dysphagia after Stroke: A Systematic Review. Nutrients. 2023;15(7). DOI: 10.3390/nu15071714
72. Kotecki S, Schmidt R. Cost and effectiveness analysis using nursing staff-prepared thickened liquids vs. commercially thickened liquids in stroke patients with dysphagia. Nurs Econ. 2010;28(2):106-9, 13.
73. Pelczarska A, Jakubczyk M, Niewada M. The cost-effectiveness of food consistency modification with xanthan gum-based Nutilis Clear® in patients with post-stroke dysphagia in Poland. BMC Health Serv Res. 2020;20(1):552. DOI: 10.1186/s12913-020-05411-2
74. Swan K, Speyer R, Heijnen BJ, Wagg B, Cordier R. Living with oropharyngeal dysphagia: effects of bolus modification on health-related quality of life–a systematic review. Qual Life Res. 2015;24(10):2447-56.DOI: 10.1007/s11136-015-0990-y
Ejercicios para la disfagia (ver Anexo 2)
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere la realización de ejercicios de deglución para rehabilitar la función deglutoria en personas que han sufrido un ictus y presentan disfagia.
2. Se sugiere ofrecer los ejercicios Shaker o Chin tuck en vez de los ejercicios de resistencia además de la terapia convencional de disfagia.
3. Se sugiere ofrecer el ejercicio de entrenamiento de la fuerza muscular espiratoria (EMST) para el tratamiento de la disfagia en personas que han sufrido un ictus y sin traqueostomía.
Justificación
Se realizan recomendaciones débiles a favor de los ejercicios Shaker, Chin tuck y para el entrenamiento de la fuerza muscular espiratoria, puesto que existe evidencia que señala que con estos ejercicios mejora la disfagia de estos pacientes, e incluso disminuye el riesgo de neumonía si se consideran todas las intervenciones a la vez, aunque la evidencia es de baja calidad. Además, puede haber diferencias entre los valores y preferencias de los pacientes. Sin embargo, la evidencia es insuficiente para recomendar a favor o en contra de los ejercicios con entrenamiento de la resistencia de lengua al paladar (tongue to palate resitance training) para el tratamiento de la disfagia.
Justificación detallada
Ejercicios de Shaker y/o Chin Tuck against resistance (CTAR)
- Calidad de la evidencia: la calidad es baja. Son estudios de pequeño tamaño, sin ocultamiento de la secuencia, alto sesgo por pérdida de datos (attrition bias) y cegamiento no claro de los evaluadores.
- Balance beneficios y riesgos: estos ejercicios mejoran la disfagia en los pacientes y no se han descrito efectos adversos.
- Aceptabilidad por parte de los pacientes: ésta puede variar. Los pacientes pueden no tolerar este tratamiento por fatiga, dolor en el cuello o musculatura abdominal, aunque se considera que los posibles beneficios superan los riesgos potenciales que serían relativamente leves.
Entrenamiento de la fuerza muscular espiratoria (EMST)
- Calidad de la evidencia: la confianza es baja.
- Balance beneficios y riesgos: Fom et al. (75) no encontraron diferencias entre la tasa de abandono entre los grupos. Otras consideraciones sobre los beneficios de realizar los ejercicios con estos dispositivos, como la obtención de una mayor ingesta oral y la disminución del riesgo de aspiración, superan el pequeño riesgo que existe de efectos adversos.
- Aceptabilidad por parte de los pacientes: el ejercicio supone un aumento de la presión respiratoria requerida para la intervención.
- Recursos requeridos: Aunque se necesitan recursos para financiar los dispositivos de entrenamiento, es una herramienta que está disponible, relativamente barata, portátil y fácil de implementar.
Tongue to palate resistance training (TPRT)
- Calidad de la evidencia: la confianza es baja.
- Balance beneficios y riesgos: el beneficio potencial no está probado.
- Los valores y preferencias de los pacientes: estos son variables, existiendo aversión por parte de algunos pacientes al bulbo de la lengua debido a un reflejo de nausea hipersensible.
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseables esperados?
- Comparación 1: ejercicios Shaker o CTAR vs. tratamiento habitual: moderada.
- Comparación 2: ejercicios EMST vs. no tratamiento: pequeña.
- Comparación 3: ejercicios fortalecimiento lengua: insignificante.
Se observa una gran mejora en la escala de disfagia en el grupo que recibe cualquier tipo de intervención conductual (36 estudios; g de Hedges 1,139; EE 0,142; IC95 % de 0,862 a 1,416) (76) y una reducción del riesgo de neumonía en el grupo que recibe la intervención (seis estudios; RR 0,57; IC95 % de 0,43 a 0,75), aunque no se encuentran diferencias significativas en mortalidad (tres estudios; RR de 1,47; IC95 % de 0,32 a 6,78) (70).
- Comparación 1. Ejercicios Shaker o CTAR: se observa una gran mejoría en la escala de disfagia en el grupo que realiza ejercicios Shaker frente a los que reciben tratamiento habitual (dos estudios; g de Hedges de 1,038; IC95 % de 0,300 a 1,776) (76). También se observa una gran mejoría en la escala de disfagia en el grupo que realiza CTAR (tres estudios; g de Hedges de 1,045; IC95 % de 0,427 a 1,663) (76).
- Comparación 2. EMST frente a no tratamiento: se observa una gran mejoría en la escala de disfagia en el grupo que realiza EMST (dos estudios; g de Hedges de 0,819; IC95 % de 0,389 a 1,250) (76), aunque el riesgo de neumonía no disminuye de forma significativa en el grupo con la intervención (tres estudios; RR 0,58; IC95 % de 0,24 a 1,41) (70).
- Comparación 3. Ejercicios fortalecimiento lengua: Kim et al. (77) no encontraron diferencias significativas en las puntuaciones PAS entre el grupo control e intervención un mes después de los ejercicios.
¿Cuál es la magnitud de los efectos no deseados esperados?
- Comparación 1: ejercicios Shaker o CTAR: no se sabe.
- Comparación 2: ejercicios EMST: no se sabe.
- Comparación 3: ejercicios fortalecimiento lengua: no se sabe.
- Comparación 1: ejercicios Shaker o CTAR: estudios no incluidos.
- Comparación 2: ejercicios EMST: estudios no incluidos.
- Comparación 3: ejercicios fortalecimiento lengua: estudios no incluidos.
¿Cuál es la calidad global en la evidencia sobre los efectos?
- Comparación 1: ejercicios Shaker o CTAR: baja.
- Comparación 2: ejercicios EMST: baja.
- Comparación 3: ejercicios fortalecimiento lengua: baja.
- Comparación 1: ejercicios Shaker o CTAR: posible riesgo de sesgos en los estudios incluidos y pocos pacientes, lo que reduce la confianza en la calidad de la evidencia.
- Comparación 2: ejercicios EMST: posible riesgo de sesgos en los estudios incluidos y pocos pacientes, lo que reduce la confianza en la calidad de la evidencia.
- Comparación 3: ejercicios fortalecimiento lengua: un único estudio con posible riesgo de sesgos y pocos pacientes.
¿Existe incertidumbre o variabilidad importante sobre cómo valoran los pacientes la importancia de los desenlaces principales?
Probablemente la incertidumbre o variabilidad no sean importantes.El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
- Comparación 1: ejercicios Shaker o CTAR: probablemente favorece la intervención.
- Comparación 2: ejercicios EMST: probablemente favorece la intervención.
- Comparación 3: ejercicios fortalecimiento lengua: no se sabe.
- Comparación 1: ejercicios Shaker o CTAR: ambos tipos de ejercicios producen una mejora en la disfagia, aunque puede que no todas las personas que han sufrido un ictus toleren realizarlos.
- Comparación 2: ejercicios EMST: este ejercicio produce también una mejora en la disfagia, pero puede resultar pesado de realizar para las personas que han sufrido un ictus.
- Comparación 3: ejercicios fortalecimiento lengua: no se ha demostrado que haya efecto beneficioso en las personas con ictus que presentan disfagia.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.No se han identificado estudios.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
Probablemente aumentaría¿Es aceptable la opción para todas las partes interesadas?
Varía.En referencia a los ejercicios de Shaker, se ha descrito que hay pacientes que rechazan continuar con la realización de los mismos (78). En personas que presentan dolor crónico de cuello o historia de cirugía en el cuello o traqueotomía, no está indicada su realización.
¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
75. Eom MJ, Chang MY, Oh DH, Kim HD, Han NM, Park JS. Effects of resistance expiratory muscle strength training in elderly patients with dysphagic stroke. NeuroRehabilitation. 2017;41(4):747-52. DOI: 10.3233/NRE-172192
76. Speyer R, Cordier R, Sutt AL, Remijn L, Heijnen BJ, Balaguer M, et al. Behavioural Interventions in People with Oropharyngeal Dysphagia: A Systematic Review and Meta-Analysis of Randomised Clinical Trials. J Clin Med. 2022;11(3). DOI: 10.3390/jcm11030685
77. Kim HD, Choi JB, Yoo SJ, Chang MY, Lee SW, Park JS. Tongue-to-palate resistance training improves tongue strength and oropharyngeal swallowing function in subacute stroke survivors with dysphagia. J Oral Rehabil. 2017;44(1):59-64. DOI: 10.1111/joor.12461
78. Choi JB, Shim SH, Yang JE, Kim HD, Lee DH, Park JS. Effects of Shaker exercise in stroke survivors with oropharyngeal dysphagia. NeuroRehabilitation. 2017;41(4):753-7. DOI: 10.3233/NRE-172145
Manejo del ictus tras el alta hospitalaria: Depresión, ansiedad y labilidad emocional
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
¿Deben tratarse farmacológicamente la depresión, ansiedad y labilidad emocional tras un ictus?
¿Cuáles son los antidepresivos eficaces en el tratamiento de la depresión, ansiedad y labilidad emocional en las personas que han sufrido un ictus?
¿Es eficaz la psicoterapia como tratamiento adicional al tratamiento farmacológico de la depresión y ansiedad post-ictus?
Es frecuente que las personas que han sufrido un ictus presenten alguna alteración del humor, especialmente depresión. Además, pueden presentar ansiedad o labilidad emocional, en solitario o acompañando a la depresión y aunque puede aparecer en cualquier momento, los primeros meses tras la vuelta a casa son los más críticos.
Tratamiento farmacológico de la depresión post-ictus
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere el uso de fármacos antidepresivos para el tratamiento de la depresión post-ictus, valorando individualmente el riesgo de efectos adversos.
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
2. Monitorizar la persona que ha sufrido un ictus y que toma antidepresivos para valorar la aparición de efectos adversos, la adherencia al tratamiento, etc.
Justificación
Se ha realizado una recomendación débil a favor porque evidencia de muy baja calidad sugiere que los antidepresivos tienen un efecto beneficioso frente a placebo en la mejoría de los síntomas, aunque también producen efectos adversos que hay que tener en cuenta y habría que valorar en cada paciente.
En relación con si un fármaco es mejor que otro, no se ha realizado una recomendación al respecto porque la clasificación de fármacos que presentan los metaanálisis identificados difiere, y aunque los inhibidores de la serotonina parecen ser más eficaces, también presentan sus efectos adversos. Por ello, no se hace una recomendación a favor de ninguno en particular.
Justificación detallada
Para tratamiento farmacológico frente a placebo
Calidad de la evidencia: la calidad es muy baja. Los estudios tienen riesgo de sesgo, hay heterogeneidad importante en los resultados de los desenlaces e imprecisión en las estimaciones.
Balance entre beneficios y riesgos: aunque el tratamiento farmacológico tiene efecto sobre la depresión, tienen también efectos adversos a tener en cuenta sobre todo a nivel individual.
Aceptabilidad por parte de los pacientes: puede variar, en función de los riesgos que éste pueda o quiera asumir.
Para comparaciones entre fármacos
Calidad de la evidencia: se han identificado cuatro MA en red, pero hay una gran diferencia en el número de ECAs incluidos y el número y tipo de antidepresivos, y la evidencia para cada comparación por partes no se proporciona por separado para la evidencia directa, indirecta y la del MA en red.
Balance beneficios y riesgos: parece que los inhibidores selectivos de la recaptación de serotonina (ISRS) son mejores que los tricíclicos, aunque hay datos discordantes en la clasificación presentada por los MA.
Aceptabilidad por parte de los pacientes: puede variar, en función de los riesgos o efectos adversos que éste pueda o quiera asumir.
De la evidencia a la recomendación
Tratamiento con antidepresivos frente a no tratamiento
¿Cuál es la magnitud de los efectos deseados esperados?
Moderada.En la RS Cochrane (79) se obtiene que en el grupo no tratado tiene más riesgo de que la depresión no remita (ocho ECAs, n=1025; RR 0,70; IC95 % de 0,55 a 0,88) que en el grupo tratado con fármacos antidepresivos. El tratamiento antidepresivo también tiene un efecto beneficioso en la reducción del 50 % de la puntuación de la escala de depresión (seis ECAs; n=511; RR 0,47; IC95 % de 0,32 a 0,69).
Para la remisión de la depresión, el grupo control tiene más riesgo de que ésta no remita (ocho ECAs; n=1025; RR 0.70; IC95 % de 0,55 a 0,88). En cuanto a la reducción de un 50 % de la puntuación de la escala de depresión, el tratamiento farmacológico tiene un efecto beneficioso frente a placebo (seis ECAs; n=511; RR 0,47; IC95 % de 0,32 a 0,69).
¿Cuál es la magnitud de los efectos no deseados esperados?
Moderada.Aunque no se observan diferencias en los efectos adversos que provocan el abandono del tratamiento (incluyendo la muerte), sí aumentan los efectos adversos sobre el sistema nervioso central (SNC) (RR 1,55; IC95 % de 1,12 a 2,15) y gastrointestinales (RR 1,62; IC95 % de 1,19 a 2,19).
Teniendo en cuenta los estudios en las personas con ictus que son tratadas con SSRI para la recuperación funcional, se observa que el riesgo de fracturas óseas (RR 2,35; IC95 % de 1,62 a 3,41; calidad alta) (80) y de convulsiones (RR 1,40; IC95 % de 1,00 a 1,98) (80) es mayor en pacientes tratados con SSRI. En cambio, el riesgo de caídas no aumenta de forma significativa (RR 1,71; IC95 % de 0,80 a 3,64) (81).
¿Cuál es la calidad global en la evidencia sobre los efectos?
Muy baja.En general, los estudios tienen un alto riesgo de sesgos o riesgo no claro en múltiples de los dominios analizados, se observa alta heterogeneidad o los intervalos de confianza son muy amplios, lo que disminuyen la calidad de la evidencia para todos los desenlaces, que es muy baja para todos ellos.
¿Existe incertidumbre o variabilidad importante sobre cómo valoran los pacientes la importancia de los desenlaces principales?
Probablemente incertidumbre o variabilidad importante.El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o a la comparación?
Probablemente favorece la intervención.El riesgo de que la depresión no remita es mayor en el grupo no tratado con fármacos antidepresivos, aunque hay que tener en cuenta los efectos adversos que pueden tener lugar, por lo que el tratamiento dependerá de las características de la persona de la que se trate.
¿Cuál es la magnitud de los recursos requeridos (costes)?
Costes moderados.No se ha identificado evidencia sobre el uso de recursos y costes para el tratamiento con fármacos de la depresión, ansiedad y labilidad emocional en las personas que han sufrido un ictus.
¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.No se ha identificado evidencia sobre el uso de recursos y costes para el tratamiento con fármacos de la depresión, ansiedad y labilidad emocional en las personas que han sufrido un ictus.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad para el tratamiento con fármacos de la depresión, ansiedad y labilidad emocional en las personas que han sufrido un ictus.
¿Cuál sería el impacto en la equidad en salud?
No se sabe.¿Es aceptable la opción para los grupos de interés implicados?
Varía.No se han identificado estudios.
¿Es factible la implementación de la opción?
Probablemente sí.Comparaciones entre fármacos antidepresivos
Los cuatro MA en red identificados que pretenden establecer una clasificación de los fármacos más eficaces para el tratamiento de la depresión post-ictus se han realizado en China (82-85). El primero fue publicado en 2017 (85); otros dos fueron publicados en 2018 (82, 84), y el último en 2020 (83). Hay una gran diferencia en el número de ECAs incluidos entre el más reciente y los otros tres MA, en parte debido probablemente a la inclusión de bases de datos de estudios chinos en el MA actual. De hecho, el más reciente incluye 51 ECAs (83) y los otros tres entre 12 y 15 ECAs. Por otro lado, hay diferencias en los ECAs incluidos entre los MA (incluso en los que incluyen un número parecido de ECAs) (ver Tabla 1 en el anexo).
El número y tipo de antidepresivos incluidos también varía entre los MA, lo que puede explicar en parte los datos discordantes obtenidos con relación a la clasificación que presentan éstos.
Por otro lado, para poder evaluar la evidencia de un MA en red mediante GRADE, la evidencia para cada comparación por pares debe proporcionarse por separado (la evidencia directa, la indirecta y la del MA en red), y en este caso, ninguno de los autores lo hace, por lo que se dificulta dicha valoración.
Por todo ello, y por las recomendaciones que realizan las guías más recientes que se han identificado al respecto, no se concluye cuáles son las mejores opciones de tratamiento farmacológico de las personas con depresión post-ictus.
Tablas GRADE
Bibliografía
79. Allida S, Cox KL, Hsieh CF, Lang H, House A, Hackett ML. Pharmacological, psychological, and non-invasive brain stimulation interventions for treating depression after stroke. Cochrane Database Syst Rev. 2020;1(1):Cd003437. DOI: 10.1002/14651858. CD003437.pub5
80. Legg LA, Rudberg AS, Hua X, Wu S, Hackett ML, Tilney R, et al. Selective serotonin reuptake inhibitors (SSRIs) for stroke recovery. Cochrane Database Syst Rev. 2021;11(11):Cd009286. DOI: 10.1002/14651858.CD009286.pub4
81. Jones JS, Kimata R, Almeida OP, Hankey GJ. Risk of Fractures in Stroke Patients Treated With a Selective Serotonin Reuptake Inhibitor: A Systematic Review and Meta-Analysis. Stroke. 2021;52(9):2802-8.DOI: 10.1161/STROKEAHA.120.032973
82. Deng L, Qiu S, Yang Y, Wang L, Li Y, Lin J, et al. Efficacy and tolerability of pharmacotherapy for post-stroke depression: a network meta-analysis. Oncotarget. 2018;9(34):23718-28. DOI: 10.18632/oncotarget.23891
83. Li X, Zhang C. Comparative efficacy of nine antidepressants in treating Chinese patients with post-stroke depression: A network meta-analysis. J Affect Disord. 2020;266:540-8. DOI: 10.1016/j.jad.2020.09.078
84. Qin B, Chen H, Gao W, Zhao LB, Zhao MJ, Qin HX, Chen W, Chen L, Yang MX. Efficacy, acceptability, and tolerability of antidepressant treatments for patients with post-stroke depression: a network meta-analysis. Braz J Med Biol Res. 2018;51(7):e7218. DOI: 10.1590/1414-431×20187218
85. Sun Y, Liang Y, Jiao Y, Lin J, Qu H, Xu J, et al. Comparative efficacy and acceptability of antidepressant treatment in poststroke depression: a multiple-treatments meta-analysis. BMJ Open. 2017;7(8):e016499.DOI: 10.1136/bmjopen-2017-016499
Tratamiento farmacológico de la ansiedad
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere el uso de farmacoterapia para el tratamiento de la ansiedad en personas que han sufrido un ictus.
Justificación
Se ha realizado una recomendación débil a favor de su uso, puesto que, aunque la evidencia es de baja calidad, hay un efecto beneficioso del tratamiento farmacológico sobre la ansiedad en personas que han sufrido un ictus.
Justificación detallada
Calidad de la evidencia: la confianza en la evidencia es baja.
Balance riesgos beneficios: solo se señala el efecto sobre la puntuación en la escala de la ansiedad antes y después del tratamiento, pero no se informa de más efectos, ni de eficacia ni de seguridad.
Aceptabilidad por parte de los pacientes: se cree que será un tratamiento aceptado por los pacientes.
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseados esperados?
Moderada.De las dos RS identificadas (86, 87), solo la de Chun et al. (86) presentan datos metaanalizados. En esta revisión (86) se incluyen personas con infarto cerebral, hemorragia parenquimatosa, hemorragia subaracnoidea o lesión cerebral traumática. Se incluyen cuatro estudios que analizan cinco comparaciones de farmacoterapia frente a control, observando que la farmacoterapia tiene efecto sobre la disminución de la ansiedad (cuatro ECAs; DEM de -2,12; IC95 % de -3,05 a -1,18).
¿Cuál es la magnitud de los efectos no deseados esperados?
Moderada.La mitad de las personas tratadas con paroxetina presentaron efectos adversos como náusea, vómitos o mareos, pero solo el 14 % de los pacientes tratados con buspirona sufrieron náuseas o palpitaciones (86).
¿Cuál es la calidad global de la evidencia sobre los efectos?
Muy baja.La heterogeneidad es alta (I2=89 %). Los estudios evalúan la paroxetina frente a otro SSRI o tratamiento habitual; otro evalúa el uso de imipramina (antidepresivo tricíclico) frente al tratamiento habitual; y el último, un ansiolítico azapirona (buspirona) frente al tratamiento habitual. Las cuatro comparaciones provenían de tres estudios con alto riesgo de sesgos. El estudio que no disponía de datos para el análisis reportó un aumento del trastorno de ansiedad generalizado cuatro veces mayor en el grupo placebo que el grupo tratado con escitalopram (HR ajustado de 4,95; IC95 % de 1,54 a 15,93).
¿Existe incertidumbre o variabilidad importante sobre cómo valoran los pacientes los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantes.
El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
Probablemente favorece la intervención.El tratamiento tiene efectos beneficiosos sobre la ansiedad, aunque también produce efectos adversos como vómitos o mareos en algunas personas.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se ha identificado evidencia sobre el uso de recursos y costes para el tratamiento con fármacos de la ansiedad en personas que han sufrido un ictus.
¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.No se han identificado estudios.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se ha identificado estudios coste-efectividad para el tratamiento con fármacos de la depresión, ansiedad y labilidad emocional en personas que han sufrido un ictus.
¿Cuál sería el impacto en la equidad en salud?
No se sabe.¿Es aceptable la opción para los grupos de interés implicados?
Varía.No se han identificado estudios.
¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
86. Chun HY, Newman R, Whiteley WN, Dennis M, Mead GE, Carson AJ. A systematic review of anxiety interventions in stroke and acquired brain injury: Efficacy and trial design. J Psychosom Res. 2018;104:65-75. DOI: 10.1016/j.jpsychores.2017.11.010
87. Knapp P, Campbell Burton CA, Holmes J, Murray J, Gillespie D, Lightbody CE, et al. Interventions for treating anxiety after stroke. Cochrane Database Syst Rev. 2017;5(5):Cd008860. DOI: 10.1002/14651858.CD008860.pub3
Tratamiento farmacológico de la labilidad emocional
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere considerar el tratamiento con antidepresivos en aquellas personas que, tras un ictus, presentan labilidad emocional persistente, con episodios frecuentes y graves, valorando los efectos adversos de estos fármacos, sobre todo en personas de edad avanzada.
Justificación
Se ha realizado una recomendación débil a favor porque existe evidencia de baja calidad del efecto del tratamiento farmacológico en la labilidad emocional de las personas que han sufrido un ictus. Se trata de fármacos cuya prescripción es factible y probablemente aceptable por los pacientes.
Justificación detallada
Calidad de la evidencia: la confianza en la evidencia es baja o muy baja.
Balance beneficios y riesgos: se miden los resultados de diferente manera, pero todos indican que hay una mejora en la labilidad emocional de las personas que han sufrido un ictus. Como en otros casos, tener en cuenta los efectos adversos de cada tipo de fármaco y la situación individual del paciente, que puede hacer inclinar el balance.
Aceptabilidad por parte de los pacientes: se cree que es un tratamiento que es aceptado por los pacientes.
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseados esperados?
Moderada.En la revisión Cochrane (88), se incluyen siete ECAs (n=239). Dos eran estudios cruzados y sus datos no se encontraban disponibles, por lo que los resultados se basan en cinco ECAs con 213 pacientes.
Los antidepresivos aumentan el número de pacientes que reducen en un 50 % la labilidad emocional (un ECA; n=19; RR 16,50; IC95 % de 1,07 a 253,40) y mejoran la puntuación de la Escala de labilidad del centro de estudios neurológicos (CNS-LS) y de la Clinician Interview Based Impression of Change (CIBIC) (un ECA; n=28; RR 1,44, IC9 5% de 0,95 a 2,19). Los antidepresivos (ISRS y antidepresivos tricíclicos (ATC)) aumentan el porcentaje de pacientes en los que se reduce la labilidad emocional (tres ECAs; n=164; RR 2,18, IC95 % de 1,29 a 3,71) y mejora de la escala PLSC (un ECA; n=28; DM 8,40, IC95 % de 11,56 a 5,24).
¿Cuál es la magnitud de los efectos no deseados esperados?
Pequeña.No se encuentran diferencias en mortalidad (seis ECAs; n=172; RR 0,59, IC95 % de 0,08 a 4,50).
¿Cuál es la calidad global en la evidencia sobre los efectos?
Muy baja.Aunque la calidad de la evidencia no es muy baja para todos los desenlaces, sí lo es para el porcentaje de pacientes en el que se reduce en un 50 % la labilidad emocional, por ello se clasifica la evidencia global como muy baja calidad.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran la importancia de los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantes.El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
Probablemente favorece la intervenciónLa evidencia indica que hay una mejora en la labilidad emocional y que no aumenta la mortalidad, aunque habría que tener en cuenta los otros efectos adversos descritos para estos fármacos y hacer un balance con la situación basal del paciente.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se ha identificado evidencia sobre el uso de recursos y costes para el tratamiento con fármacos de la labilidad emocional en personas que han sufrido un ictus.
¿Cuál es la calidad de la evidencia sobre los recursos requeridos?
No se han incluido estudios.No se han identificado estudios.
El coste-efectividad de la intervención, ¿favorece a la intervención o a la comparación?
No se sabe.¿Cuál sería el impacto en la equidad en salud?
No se sabe.¿Es aceptable la opción para todos los grupos de interés implicados?
Probablemente sí.¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
88. Allida S, Patel K, House A, Hackett ML. Pharmaceutical interventions for emotionalism after stroke. Cochrane Database Syst Rev. 2019;3(3):Cd003690. DOI: 10.1002/14651858.CD003690.pub5
Adición de la psicoterapia al tratamiento farmacológico de la depresión y la ansiedad
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere la adición de psicoterapia al tratamiento farmacológico de las personas que han sufrido un ictus, tanto las que sufren depresión como ansiedad.
Justificación
Se hace una recomendación débil a favor de la adición de la psicoterapia al tratamiento farmacológico del paciente, puesto que, aunque la evidencia es de baja calidad en ambos casos, se describe un efecto positivo tanto en la depresión como en la ansiedad. Además, se trata de intervenciones que tienen efectos positivos en otro tipo de pacientes, lo que apoya la realización de una recomendación débil a favor.
Sin embargo, no se detalla qué tipo de psicoterapia debe utilizarse ni si debe ser el personal médico de AP el que realice la intervención o si se debe derivar a consulta especializada. Dependerá de las capacidades y de la organización de cada Comunidad y organización sanitaria.
Justificación detallada
Para la depresión
Calidad de la evidencia: la confianza en la evidencia es muy baja.
Balance entre beneficios y riesgos: existe un beneficio de la adición de la psicoterapia sin efectos adversos descritos.
Aceptabilidad y factibilidad: variables, en función de la organización y recursos disponibles.
Para la ansiedad
Calidad de la evidencia: la confianza en la evidencia es baja.
Balance entre beneficios y riesgos: existe un beneficio de la adición de la psicoterapia sin efectos adversos descritos.
Aceptabilidad y factibilidad: variables, en función de la organización y recursos disponibles.
De la evidencia a la recomendación
Para la depresión
¿Cuál es la magnitud de los efectos deseados esperados?
Moderado.En la revisión Cochrane de Allida (79) se incluyen dos ensayos al respecto, uno con fluoxetina (89) y psicoterapia y otro con paroxetina y psicoterapia (90). La diferencia media de la puntuación para la depresión al final del tratamiento fue de 1,53 puntos menos (de 2,10 a 0,96 puntos menos) (dos ECAs; n=198), y la puntuación de las actividades de la vida diaria (AVD) algo mayor (DM 11,83 puntos más; de 0,27 a 23,4 más) (dos ECAs; n=198).
¿Cuál es la magnitud de los efectos no deseados esperados?
No se sabe.No se han identificado estudios que describan efectos adversos de la adición de la psicoterapia.
¿Cuál es la calidad global de la evidencia sobre los efectos?
Muy baja.Los datos se obtienen de dos estudios, con posible riesgo de sesgo, con heterogeneidad substancial e imprecisión en las estimaciones.
¿Existe incertidumbre o variabilidad importante sobre cómo valoran los pacientes la importancia de los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantes.El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
Probablemente favorece la intervención.La evidencia indica que hay una mejora en la depresión y en la puntuación de las actividades diarias, y no se detallan efectos adversos de añadir la psicoterapia al tratamiento farmacológico del paciente.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.No se han identificado estudios.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se han identificado estudios de coste-efectividad.¿Cuál sería el impacto en la equidad en salud?
Probablemente aumentaría.¿Es aceptable la opción para todas las partes interesadas?
Probablemente sí.¿Es factible la implementación de la opción?
Probablemente sí.Para la ansiedad
¿Cuál es la magnitud de los efectos deseados esperados?
Moderada.Chun et al. (86) incluye los datos de un estudio que demuestra un mayor efecto sobre la puntuación de la ansiedad con la escala Hamilton Anxiety Rating Scale (HAMA), al combinar el tratamiento con paroxetina con la psicoterapia frente al tratamiento con paroxetina (DEM −4,79; IC95 % de −5,87 a −3,71) (90).
¿Cuál es la magnitud de los efectos no deseados esperados?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad global en la evidencia sobre los efectos?
Muy baja.Solo hay un estudio que evalúa la adición de la psicoterapia al tratamiento farmacológico de la ansiedad post-ictus, con pocos pacientes y posible riesgo de sesgos.
¿Existe incertidumbre o variabilidad importante sobre cómo valoran los pacientes la importancia de los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantes.El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
Probablemente favorece la intervenciónLa adición de la psicoterapia disminuye de forma significativa la puntuación de la ansiedad, sin describirse efectos adversos al respecto, aunque se trata de un único estudio pequeño.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.No se han identificado estudios.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
Probablemente aumentaría.¿Es aceptable la opción para todas las partes interesadas?
Probablemente sí.¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
79. Allida S, Cox KL, Hsieh CF, Lang H, House A, Hackett ML. Pharmacological, psychological, and non-invasive brain stimulation interventions for treating depression after stroke. Cochrane Database Syst Rev. 2020;1(1):Cd003437. DOI: 10.1002/14651858. CD003437.pub5
86. Chun HY, Newman R, Whiteley WN, Dennis M, Mead GE, Carson AJ. A systematic review of anxiety interventions in stroke and acquired brain injury: Efficacy and trial design. J Psychosom Res. 2018;104:65-75. DOI: 10.1016/j.jpsychores.2017.11.010
89. Cao WW YJ, Sun SY, Sun YB, Luan L, Cai XJ, et al. Group psychotherapy in treatment of post stroke depression [团体心理治疗在脑卒中后抑郁治疗中的应用]. Chinese Mental Health Journal 2009;23(2):100-4. Available from: https://www.cochranelibrary. com/central/doi/10.1002/central/CN-00744478/full.
90. Wang X, He Y, Xiao C-L. A clinical trial of paroxetine and psychotherapy in pa-tients with poststroke depression and anxiety. Chinese mental health journal [Internet]. 2005; 19(8):[564-6 pp.]. Available from: https://www.cochranelibrary.com/central/doi/10.1002/central/CN-00712949/full.
Manejo del ictus tras el alta hospitalaria: Intervenciones multidisciplinares
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
¿Son eficaces las intervenciones multidisciplinares (fisioterapia junto con terapia ocupacional, logopedia, etc.) en la mejoría de la independencia para las actividades de la vida diaria (AVD) en personas que han sufrido un ictus?
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere la implementación de intervenciones multidisciplinares que permitan la evaluación conjunta de la persona que ha sufrido un ictus y de sus necesidades, para que la atención que se le brinda sea lo más integral y coordinada posible.
2. Se sugiere contar con profesionales de la enfermería, rehabilitadores, fisioterapeutas, logopedas, terapeutas ocupacionales, etc. que puedan ayudar a mejorar las diferentes secuelas y necesidades de las personas que han sufrido un ictus, hasta que no se identifiquen objetivos funcionales que mejorar.
Los efectos deseados de la intervención superan a los indeseables. Eso significa que la mayoría de los pacientes deberían recibir la intervención recomendada. LEER MÁS
3. La persona que ha sufrido un ictus y su cuidador/a y/o familiares deberían participar de forma activa en la definición de los objetivos de rehabilitación y familiarizarse con los ejercicios y cuidados que deberían realizarse.
4. Tras el alta hospitalaria, el equipo de AP debe comprobar que la persona que ha sufrido un ictus está cumpliendo o ha cumplido con el tratamiento rehabilitador indicado en cada caso.
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
5. El equipo de AP debería instruir a las personas cuidadoras o familiares de personas que han sufrido un ictus y con gran deterioro funcional que no son candidatas a rehabilitación en los cuidados necesarios para estas personas.
6. Cuando la persona que ha sufrido un ictus experimente un deterioro funcional por depresión, fracturas, caídas, espasticidad, dolor o cualquier otra causa, se recomienda derivar de nuevo a rehabilitación con el fin de intentar recuperar el nivel funcional previo además de tratar las posibles causas desencadenantes.
Justificación
Se ha realizado una recomendación débil a favor de las intervenciones multidisciplinares, puesto que aquellas intervenciones que mejores resultados han obtenido son las que han contado con reuniones multidisciplinares para la valoración conjunta de la persona que ha sufrido un ictus y de sus necesidades, así como aquellas que coordinan de forma estrecha la AP y AE. Sin embargo, para implementar estas intervenciones habría que analizar las necesidades organizativas y los recursos disponibles, para poder ofrecer este servicio de la forma más eficiente posible.
Justificación detallada
Calidad de la evidencia: la confianza en la evidencia es moderada.
Balance entre beneficios y riesgos: existe un beneficio cuanto se implementan intervenciones multidisciplinares, sin que se reporten efectos adversos por haber implementado este tipo de intervenciones.
Factibilidad: la fuerza de la recomendación es débil porque se entiende que la implementación de este tipo de intervenciones necesita de una organización y recursos que quizá no estén disponibles en todos los casos. Por ello, se realiza una recomendación débil a favor.
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseados esperados?
Moderado.En cuanto a las AVD, no observan una mejoría ni la revisión de Fens et al. (91) ni el ensayo de Vluggen et al. (92) en personas mayores frágiles (Frenchay Activity Index (FAI): DM -1,69; IC95 % de -5,39 a 2). Sin embargo, sí se observa una mejora en la subescala de autonomía fuera del hogar de Impact on Participation and Activity (IPA) (máximo 20 puntos, siendo menos mejor) (DM −2,15, p=0,047) y la carga percibida del cuidador (DM 1,23, P=0,048).
En otro ensayo posterior (93) se observa una mejoría en el autocuidado (índice de Barthel modificado a los 3 meses del grupo HCISM vs. control: 72,28 ± 10,52 vs. 60,02 ± 10,11) y la autoeficacia (General Self Efficacy Scale (GSES): grupo observación vs. control: 26,61 ± 5,01 vs. 21,55 ± 4,18).
En el estudio STROKE-CARD (94), el 81,4 % del grupo intervención alcanzaba la independencia funcional a los 12 meses (escala de Rankin modificada) frente al 76,1 % del grupo control (RR de 1,07; IC95 % de 1,02 a 1,12).
En cuanto a los eventos de enfermedad vascular importante (desenlace compuesto por ictus isquémico no fatal, ictus hemorrágico no fatal, infarto de miocardio no fatal o muerte vascular), se observa una reducción significativa del riesgo en el grupo intervención (HR de 0,63; IC95 % de 0,45 a 0,88; p=0,007), aunque sin diferencias significativas en la recurrencia de ictus o AIT y mortalidad por todas las causas (HR de 0,81; IC95 % de 0,54 a 1,21; HR de 0,72; IC95 % de 0,47 a 1,10, respectivamente). Sí hubo diferencias significativas para infarto de miocardio (HR de 0,32; IC95 % de 0,13 a 0,80; p=0,014) y mortalidad vascular (HR 0,32; IC95 % de 0,16 a 0,66) (94).
En cuanto a la calidad de vida, en la revisión de Fens et al. (91) solo dos de los ocho estudios reportaron efectos favorables, aunque en el STROKE CARD (94) se observó una mejor calidad a los 12 meses, siendo el valor mediano del índice de salud (EQ-5D-3L) de 0,783 (IQR 0,687-1,000) en el grupo intervención y de 0,779 (IQR 0,573-1,000) en el control (P <0,001). Asimismo, el 43 % del grupo intervención obtuvo una puntuación de 1 (ausencia de problemas) en todas las dimensiones, frente al 32 % del grupo control (RR 1,36; IC95 % de 1,20 a 1,54; P <0,001).
¿Cuál es la magnitud de los efectos no deseados esperados?
Insignificantes.No se observan efectos adversos en ningún caso. Willeit et al. (94) señalan que no encontraron diferencias en el riesgo de efectos adversos potenciales de una prevención secundaria intensificada en el grupo STROKE-CARD frente al control.
¿Cuál es la calidad global de la evidencia sobre los efectos?
Moderada.Aunque no se ha realizado un MA, se considera que el estudio de STROKE-CARD (94) proporciona evidencia de alta calidad sobre el efecto de la intervención multidisciplinar, así como el estudio de Feng et al. (93). Sin embargo, como los estudios anteriores más pequeños y con intervenciones más simples no encontraron diferencias con el grupo control, se ha disminuido la calidad de la evidencia a moderada.
¿Existe incertidumbre o variabilidad importante sobre cómo valoran los pacientes la importancia de los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantes.El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
Probablemente favorece la intervención.El estudio de mejor calidad y mayor tamaño indica que la intervención multidisciplinar ayuda a disminuir los eventos vasculares y mejora tanto las actividades diarias como la calidad de vida de los pacientes, sin presentar al parecer efectos adversos.
¿Cuál es la magnitud de los recursos requeridos (costes)?
Costes y ahorros insignificantes.Se ha identificado un estudio de coste-efectividad sobre una intervención que no respondía exactamente a la pregunta planteada, pero en la que se generó una vía de atención post-ictus integrada en AP (iCaPPS©) en comparación con la atención convencional tras un ictus desde la perspectiva de la sociedad, utilizando el EuroQol EQ-5D-5 L (95). En este estudio se demostró que la implementación de una ruta clínica de este tipo mejoraba la calidad de vida de los pacientes. A los seis meses, se ganaron 0,55 AVACs, mientras que con la vía de atención tradicional se ganaron 0,32 AVACs (efectividad incremental 0,23 AVAC) (95). A los seis meses, el coste total de la terapia fue de 790,32 Ringgit Malayo (MYR) de 2012 (376,1€ de 2023), mientras que con la vía de atención tradicional fue de 527,22 MYR de 2012 (250,9€ de 2023) (coste incremental de 263,12 MYR de 2012 (125,2 € de 2023)) (95).
¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
Moderada.La validez externa del estudio es moderada, puesto que el estudio se realiza en Malasia, y tanto los resultados del estudio como los precios son los de dicho país (95), y puede que no se correspondan con los de nuestro sistema.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
Probablemente favorece la intervención.El coste adicional por AVAC ganado de la intervención iCaPPS frente a los cuidados habituales fue de 1144 MYR (544,4€ de 2023), equivalente al 3,7 % del PIB per cápita para el 2012 en Malasia (95). El análisis de S señaló que, para el mejor escenario, la ratio coste-efectividad incremental (RCEI) fue de 1379,91 MYR de 2012 (656,6€ de 2023) y para el peor de 3310,78 MYR de 2012 (1575,5€ de 2023) al comparar iCaPPS frente al cuidado habitual (95).
¿Cuál sería el impacto en la equidad en salud?
Probablemente disminuiría¿Es aceptable la opción para todas las partes interesadas?
Probablemente sí¿Es factible la implementación de la opción?
Varía.Tablas GRADE
Bibliografía
91. Fens M, Vluggen T, van Haastregt JC, Verbunt JA, Beusmans GH, van Heugten CM. Multidisciplinary care for stroke patients living in the community: a systematic review. J Rehabil Med. 2013;45(4):321-30. DOI: 10.2340/16501977-1128
92. Vluggen T, van Haastregt JCM, Tan FE, Verbunt JA, van Heugten CM, Schols J. Ef-fectiveness of an integrated multidisciplinary geriatric rehabilitation programme for older persons with stroke: a multicentre randomised controlled trial. BMC Geriatr. 2021;21(1):134. DOI: 10.1186/s12877-021-02082-4
93. Feng W, Yu H, Wang J, Xia J. Application effect of the hospital-community integrated service model in home rehabilitation of stroke in disabled elderly: a randomised trial. Ann Palliat Med. 2021;10(4):4670-7. DOI: 10.21037/apm-21-602
94. Willeit P, Toell T, Boehme C, Krebs S, Mayer L, Lang C, et al. STROKE-CARD care to prevent cardiovascular events and improve quality of life after acute ischaemic stroke or TIA: A randomised clinical trial. EClinicalMedicine. 2020;25:100476. DOI: 10.1016/j.eclinm.2020.100476
95. Abdul Aziz AF, Mohd Nordin NA, Muhd Nur A, Sulong S, Aljunid SM. The integrated care pathway for managing post stroke patients (iCaPPS(©)) in public primary care Healthcentres in Malaysia: impact on quality adjusted life years (QALYs) and cost effec-tiveness analysis. BMC Geriatr. 2020;20(1):70. DOI: 10.1186/s12877-020-1453-z
Manejo del ictus tras el alta hospitalaria: terapia ocupacional
Actualizado a fecha: 05/02/2025
¿Es eficaz la terapia ocupacional en la mejoría de la independencia para las actividades de la vida diaria (AVD) en personas que han sufrido un ictus?
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
1. Se sugiere que, si la persona que ha sufrido un ictus tiene dificultades para realizar las actividades diarias, ésta sea tratada por un/una terapeuta ocupacional.
Justificación
La evidencia señala que la terapia ocupacional tiene un efecto positivo en la reducción de la mortalidad o de presentar un desenlace negativo para la persona que ha sufrido un ictus, y un efecto algo menor, pero significativo, en la mejora de las AVD, sobre todo de las actividades instrumentales. Además, se trata de un tema de suma importancia para las personas que han sufrido un ictus, por lo que se recomienda de forma fuerte a favor del mismo.
Justificación detallada
Calidad de la evidencia: la confianza en la evidencia es baja.
Balance entre beneficios y riesgos: existe un beneficio moderado, puesto que se reduce de forma importante la probabilidad de la mortalidad y de presentar un desenlace negativo al final del seguimiento, y mejoran las AVD, sin que se reporten efectos adversos por haber implementado este tipo de intervenciones.
Factibilidad: se entiende que puede haber variabilidad en la disponibilidad de terapeutas ocupacionales en los servicios sanitarios de las diferentes comunidades, pero debería ser algo que se tendría que ofertar a estas personas. Por eso, a pesar de las dificultades que puedan encontrarse, se realiza una recomendación fuerte a favor.
De la evidencia a la recomendación
¿Cuál es la magnitud de los efectos deseados esperados?
Moderada.Según los resultados de la revisión sistemática de Legg et al. (96) sobre la terapia ocupacional en personas que han sufrido un ictus y presentan problemas con las actividades diarias, la probabilidad de muerte o para un desenlace negativo al final del seguimiento (muerte, deterioro o dependencia para realizar actividades personales diarias) fue de 0,71 (IC95 % de 0,52 a 0,96) a favor de la terapia ocupacional. La media de la puntuación de las actividades diarias fue 0,17 DE mayor (diferencia significativamente pequeña) en el grupo que recibió terapia ocupacional frente al que recibió atención habitual (DEM 0,17 mayor; IC95 % de 0,03 a 0,31). La puntuación para las actividades instrumentales de la vida diaria al final del seguimiento fue de 0,22 DE mayor (IC95 % de 0,07 a 0,37) para el grupo con terapia ocupacional que para el grupo control.
En cuanto a la puntuación media del estado de ánimo o la angustia, esta fue 0,08 DE mayor (de 0,09 menos a 0,26 veces más), siendo la diferencia no significativa.
¿Cuál es la magnitud de los efectos no deseados esperados?
No se sabe.No se encuentra un aumento de efectos adversos con la implementación de la terapia ocupacional.
¿Cuál es la calidad global de la evidencia sobre los efectos?
Baja.Se baja la calidad de la evidencia por riesgo de sesgo de los estudios y por imprecisión en todos los desenlaces.
¿Existe incertidumbre o variabilidad importante sobre cómo valoran los pacientes la importancia de los desenlaces principales?
Probablemente la incertidumbre o la variabilidad no sean importantes.El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
Probablemente favorece la intervención.La evidencia indica que hay una mejora tanto en la reducción de mortalidad y desenlaces negativos como una mejoría en las actividades diarias de estas personas, sin que se describan además efectos adversos relacionados, por lo que el balance favorece la intervención frente a la comparación.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la certeza en torno a la evidencia sobre los recursos requeridos?
No se han incluido estudios.No se han identificado estudios.
El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
Probablemente disminuiría.¿Es aceptable la opción para los grupos de interés implicados?
Probablemente sí.En una revisión integradora (97) que explora la evidencia existente sobre barreras y facilitadores para aumentar la implicación de las personas con ictus en la rehabilitación hospitalaria, se identifican cuatro temas principales: 1) el impacto del ictus; 2) la autoeficacia; 3) therapeutic relationship; y, 4) factores motivadores. Se señala que la definición de los objetivos con la persona que ha sufrido un ictus podría aumentar su participación y la eficacia de cualquier intervención rehabilitadora.
En otra metasíntesis cualitativa sobre la experiencia en ejercer una ocupación tras el ictus (98) se identificaron cinco temas conceptuales: 1) respuesta emocional tras el ictus; 2) impacto del ictus en la identidad; 3) el papel significativo de otras personas; 4) el acceso a la comunidad; y, 5) el proceso de la adaptación ocupacional.
Se señala que la implicación ocupacional tras un ictus está ligada a la propia identidad y a la respuesta emocional, siendo dos aspectos que tienen un impacto en la capacidad de la adaptación ocupacional.
¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
96. Legg LA, Lewis SR, Schofield-Robinson OJ, Drummond A, Langhorne P. Occupational therapy for adults with problems in activities of daily living after stroke. Cochrane Data-base Syst Rev. 2017;7(7):Cd003585.DOI: 10.1002/14651858.CD003585.pub3
97. Forgea MC, Lyons AG, Lorenz RA. Barriers and Facilitators to Engagement in Rehabili-tation Among Stroke Survivors: An Integrative Review. Rehabil Nurs. 2021;46(6):340-7. DOI: 10.1097/RNJ.0000000000000340
98. Williams S, Murray C. The Experience of Engaging in Occupation following Stroke: A Qualitative Meta-Synthesis. British Journal of Occupational Therapy. 2013;76(8):370-378. DOI:10.4276/030802213X13757040168351
Manejo del ictus tras el alta hospitalaria: Tratamiento dual antiagregante
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Actualizado a fecha: 05/02/2025
Aquellas personas que han sufrido un ictus isquémico leve o un AIT no cardioembólico, que no son candidatos a trombólisis y que reciben tratamiento dual antiagregante, ¿cuánto tiempo deberían estar recibiendo dicho tratamiento?
Los efectos deseados de la intervención superan a los indeseables. Eso significa que la mayoría de los pacientes deberían recibir la intervención recomendada. LEER MÁS
1. Se recomienda que en aquellas personas con ictus isquémico no cardioembólico leve o AIT de alto riesgo en las que se inició tratamiento dual antiagregante con AAS y clopidogrel, éste se mantenga durante las primeras tres semanas para prevenir la recurrencia de ictus.
Los efectos deseables probablemente superan los efectos no deseables, pero con una incertidumbre apreciable. Eso implica que cada paciente debería ser ayudado a llegar a la decisión más adecuada a sus valores y preferencias. LEER MÁS
3. Se sugiere que en aquellas personas con ictus isquémico leve o AIT de alto riesgo no cardioembólico que iniciaron tratamiento con AAS y ticagrelor, éste se mantenga durante un máximo de 30 días para prevenir la recurrencia del ictus.
Práctica recomendada basada en la experiencia clínica y el consenso del equipo elaborador. LEER MÁS
3. Una vez finalizada la doble antiagregación, el tratamiento antiagregante con AAS o clopidogrel debería continuar de forma indefinida.
Justificación
Con relación al tratamiento dual antiagregante y su duración en personas con ictus leve o AIT de alto riesgo no cardioembólico, en la versión anterior de la guía no se hacía hincapié en el seguimiento posterior desde AP. La evidencia a este respecto señala que el tratamiento dual antiagregante con clopidogrel y AAS durante 21 días es beneficioso para estas personas y que el tratamiento dual con ticagrelor y AAS también lo es, aunque con mayor riesgo de hemorragia.
Justificación detallada
Calidad de la evidencia: la confianza en la evidencia es moderada para el tratamiento dual antiagregante de clopidogrel y AAS, y más baja para el tratamiento dual con ticagrelor y AAS.
Balance entre beneficios y riesgos: el balance en ambos casos sería favorable, aunque en mayor medida para el tratamiento con clopidogrel y AAS de no más de 21 días de duración.
De la evidencia a la recomendación
Clopidogrel y AAS
¿Cuál es la magnitud de los efectos deseados esperados?
Moderado.El riesgo de ictus recurrente no fatal a los 90 días disminuye con el tratamiento dual (RR de 0,70; IC95 % de 0,61 a 0,80; 19 menos por 1000 (de 25 menos a 13 menos)). El riesgo de discapacidad funcional grave también es menor en el grupo tratado (RR 0,90; IC95 % de 0,81 a 1,01; 14 menos por 1000 (de 27 menos a uno más)), así como el de presentar una baja calidad de vida a los 90 días (EQ-5D de 0,5 o menos) (RR 0,81; IC95 % de 0,66 a 1,01; 13 menos por 1000 (de 23 menos a uno más)). El riesgo de mortalidad a los 90 días no es estadísticamente mayor (OR 1,27; IC95 % de 0,73 a 2,23; uno más por 1000 (de dos menos a cuatro más)). En el análisis de subgrupo en función de la duración del tratamiento (< 21 días o más), el riesgo de ictus isquémico a los 90 días era similar (cuatro más por 1000 (de dos menos a 11 más)) (39, 99).
¿Cuál es la magnitud de los efectos no deseados esperados?
Pequeños.Entre las 36 RS publicadas desde 2019, en ninguna de ellas se añaden nuevos estudios a los ya incluidos por la guía australiana escogida como base. Por ello se utilizan sus datos para responder a esta pregunta.
El riesgo de sangrado importante extracraneal a los 90 días es mayor en el grupo tratado con clopidogrel y AAS (OR 1,71; IC95 % de 0,92 a 3,20; cuatro más por 1000 (de dos a seis más)).
El análisis de subgrupos según la duración del tratamiento (< 21 días o más) mostró que había diferencias en el porcentaje de pacientes con sangrado moderado o grave a los 90 días, que era mayor en el grupo con una duración mayor de 21 días (OR 2,20; IC95 % de 0,83 a 5,78; tres más por 1000 (de uno menos a siete más)) (39, 99).
¿Cuál es la calidad global de la evidencia sobre los efectos?
Moderada.La calidad de la evidencia ha sido considerada alta o moderada para todos los desenlaces. Por eso se considera calidad global moderada.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran los desenlaces principales?
La incertidumbre o la variabilidad probablemente no sean importantes.No se ha identificado evidencia al respecto.
El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
Favorece la intervención.Se considera que el balance es favorable, sobre todo teniendo en cuenta que, con una duración de 21 días, el riesgo de sangrado en estos pacientes es menor en comparación con alargarlo 90 días, sin reducir el efecto sobre el riesgo de recurrencia de ictus.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.No se han identificado estudios.
¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.El coste-efectividad de la intervención, ¿favorece la intervención o la comparación?
No se sabe.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
No se sabe.No se han identificado estudios al respecto.
¿Es aceptable la opción para todas las partes interesadas?
Probablemente sí.No se han incluido estudios al respecto.
¿Es factible la implementación de la opción?
Probablemente sí.Ticagrelor y AAS
¿Cuál es la magnitud de los efectos deseados esperados?
Moderado.El riesgo de sufrir un ictus o mortalidad a los 30 días es menor con el tratamiento de ticagrelor y AAS (HR 0,83; IC9 5% de 0,71 a 0,96), lo que supone una diferencia de 10 menos por 1000 (de 18 menos a dos menos). El riesgo de ictus recurrente a los 30 días también es menor (HR 0,79; IC95 % de 0,68 a 0,93), lo que supone una diferencia de 13 menos por 1000 (de 20 a cuatro menos). No había cambios en el riesgo de discapacidad (ERm > 1) a los 30 días (39, 100).
¿Cuál es la magnitud de los efectos no deseados esperados?
Moderado.El riesgo de sangrado grave fue mayor para este grupo (HR 3,99; IC95 % de 1,74 a 9,14), lo que supone una diferencia de cuatro casos más por 1000 (IC95 % de uno a ocho más) (39, 99).
¿Cuál es la calidad global de la evidencia sobre los efectos?
Baja.Se ha considerado la calidad de la evidencia para los desenlaces como moderada, salvo para el riesgo de sangrado grave, que era baja. Por ello, se considera la calidad global de la evidencia como baja.
¿Existe incertidumbre o variabilidad importante sobre cómo los pacientes valoran los desenlaces principales?
La incertidumbre o la variabilidad probablemente no sean importantes.No se ha identificado evidencia al respecto.
El balance entre los efectos deseados y no deseados esperados, ¿favorece la intervención o la comparación?
Probablemente favorece la intervención.En este caso el balance probablemente favorezca la opción, aunque con menos fuerza que en el caso de clopidogrel y AAS.
¿Cuál es la magnitud de los recursos requeridos (costes)?
No se sabe.¿Cuál es la calidad de la evidencia sobre los recursos requeridos (costes)?
No se han incluido estudios.El coste-efectividad de la intervención, ¿favorece a la intervención o a la comparación?
No se sabe.No se han identificado estudios de coste-efectividad.
¿Cuál sería el impacto en la equidad en salud?
No se sabe.No se han identificado estudios al respecto.
¿Es aceptable la opción para las partes interesadas?
Probablemente sí.No se han incluido estudios al respecto.
¿Es factible la implementación de la opción?
Probablemente sí.Tablas GRADE
Bibliografía
39. Stroke Foundation. Clinical guidelines for stroke management. Chapter 3 of 8: acute medical and surgical management. Available at https://app.magicapp.org/#/guideline/QnoKGn.
99. Hao Q, Tampi M, O’Donnell M, Foroutan F, Siemieniuk RA, Guyatt G. Clopidogrel plus aspirin versus aspirin alone for acute minor ischaemic stroke or high risk tran-sient ischaemic attack: systematic review and meta-analysis. Bmj. 2018;363:k5108. DOI: 10.1136/bmj.k5108
100. Johnston SC, Amarenco P, Denison H, Evans SR, Himmelmann A, James S, et al. Ti-cagrelor and Aspirin or Aspirin Alone in Acute Ischemic Stroke or TIA. N Engl J Med. 2020;383(3):207-17. DOI: 10.1056/NEJMoa1916870
Estrategias diagnósticas y terapéuticas (algoritmos)
En este apartado se ha mantenido la estrategia a seguir ante sospecha de ictus que ya se describió en la versión anterior de la guía, subrayándose además los criterios de derivación de los ictus (agudo/comunicado).
Los cambios que se han realizado con respecto la versión anterior han sido la adición de la escala ROSIER como posible escala a utilizar ante una persona con sospecha de ictus (ver Figura 1).
Por otro lado, también se ha elaborado un algoritmo sobre la estrategia de AP desde el momento del alta hospitalaria y seguimiento del paciente (ver Figura 2).
Información para pacientes
Metodología
La metodología empleada para elaborar la GPC, se recoge en el documento “Elaboración de Guías de Práctica Clínica en el Sistema Nacional de Salud. Actualización del Manual Metodológico” (15). El proceso más detallado se puede encontrar en el Material metodológico publicado en la página de GuíaSalud y en la página de Osteba.
A continuación, se resumen los pasos que se han seguido en el proceso:
- Constitución del grupo elaborador de la GPC, integrado por profesionales de AP, una especialista en neurología, una representante de personas con ictus y especialistas en metodología.
- Selección y priorización de las preguntas de la GPC de 2009 (1) sobre el manejo de ictus en AP que deberían ser actualizadas.
- Formulación de las preguntas clínicas siguiendo el formato Paciente/Intervención/Comparación/Outcome o resultado.
- Análisis del uso de recursos y costes (URC) para determinar las preguntas en las que sería necesario analizar en profundidad el impacto que el URC podría tener en la formulación de las recomendaciones.
- Búsqueda bibliográfica en las bases de datos de Pubmed, EMBASE y Cochrane Library, incluyendo estudios publicados en inglés, francés y español, desde el año de publicación de la versión anterior de la guía (año 2009) o sin límite inicial (en función de la pregunta) con seguimiento de las actualizaciones hasta la publicación final de esta guía.
- La evaluación de la calidad de los estudios y resumen de la evidencia se ha desarrollado según el método Grading of Recommendations Assessment, Development and Evaluation (GRADE) (16). Se han generado los perfiles de evidencia GRADE, que son tablas en las que se resume tanto la evaluación de la calidad de la evidencia que se ha identificado y que responde a la pregunta planteada, así como los resultados numéricos obtenidos para cada desenlace de interés.
- La formulación de las recomendaciones se ha realizado siguiendo el marco de trabajo Evidence to Decision (EtD) propuesto por el grupo GRADE (17). Se han generado las tablas o marcos de EtD para cada pregunta propuesta, y las recomendaciones controvertidas o con ausencia de evidencia se han resuelto por consenso en reuniones sucesivas del grupo elaborador.
- Los colaboradores expertos han participado en la formulación de preguntas y en la revisión del primer borrador de la guía. Los revisores externos han participado en la revisión del segundo borrador. Se ha contactado con distintas sociedades científicas implicadas (Asociación Española de Trabajo Social y Salud (AETSYS), Federación de asociaciones de enfermería comunitaria y atención primaria (FAECAP), Sociedad Española de Geriatría y Gerontología (SEGG), Sociedad Española de Medicina Geriátrica (SEMEG), Sociedad Española de Medicina de Familia y Comunitaria (SEMFYC), Sociedad Española de Médicos Generales y de Familia (SEMG), Sociedad Española de Neurología (SEN), Sociedad Española de Rehabilitación y Medicina Física (SERMEF)), que están representadas a través de los miembros del grupo elaborador, de los colaboradores expertos y revisores externos de la GPC.
- La GPC fue sometida a un proceso de Exposición Pública, en el cual el borrador de la GPC fue revisado por organizaciones del ámbito de la salud que no participaron en la re-visión externa, registradas previamente e interesadas en hacer aportaciones al mismo. En el caso de esta GPC han participado diez organizaciones, cuyas aportaciones y comentarios están disponibles para su consulta en la web de GuíaSalud: http://www.guiasalud.es.
- Tanto en www.guiasalud.es como en https://www.euskadi.eus/tecnologias-sanitarias-osteba/ está disponible el material donde se presenta de forma detallada la información con el proceso metodológico de la GPC (estrategias de búsquedas para cada pregunta clínica, fichas de lectura crítica de los estudios seleccionados, perfiles de evidencia GRADE y tablas/marcos EtD).
- Está previsto actualizar la guía siguiendo un procedimiento de actualización continuada que consiste en la realización de búsquedas bibliográficas y evaluación de la nueva evidencia cada 12 meses. Las revisiones se realizarán sobre la versión electrónica de la guía, disponible en las URL: http://www.guiasalud.es y en https://www.euskadi.eus/tecnologias-sanitarias-osteba/.
Material complementario
Preguntas y recomendaciones
Investigación futura
Líneas de investigación futura
Difusión e implementación
Difusión e implementación de la GPC
Anexos
Anexo 1. Escalas prehospitalarias
Anexo 2. Ejercicios para la disfagia
Anexo 3. Información para pacientes y cuidadores
Anexo 4. Abreviaturas
Exposición pública
Informe de la Exposición pública de la GPC
Actualización
Está previsto actualizar la guía siguiendo un procedimiento de actualización continuada que consiste en la realización de búsquedas bibliográficas y evaluación de la nueva evidencia cada 12 meses. Las actualizaciones se realizarán sobre la versión electrónica de la guía, disponible en la URL: http://www.guiasalud.es.
La actualización de la GPC será realizada por integrantes del grupo elaborador que participarán en la monitorización continuada de la nueva evidencia disponible a partir de la publicación de la GPC.
Para esta actualización se van a incluir los siguientes aspectos:
Miembros del Grupo de Actualización de la GPC
La actualización contará con la participación de los coordinadores de la guía, necesitándose al menos que un/una coordinador/a clínico/a (mínimo), un/una coordinador/a metodológica/o y un/una documentalista conformen el grupo encargado de detectar información relevante y evidencia disponible, a ser posible, las mismas personas que han elaborado el documento, con el objetivo de aprovechar la experiencia y los hitos aprendidos. La persona coordinadora clínica podrá participar como informante clave y como persona asesora ante la aparición de nueva evidencia ante la solicitud de la coordinación metodológica. En caso de aparición de información con gran incertidumbre se comunicará a GuíaSalud y se conformará un grupo para la valoración de las cuestiones planteadas.
Listado de preguntas clínicas que se consideraron candidatas a monitorizarse
De las preguntas que se han tenido en cuenta en la elaboración de esta guía, el Grupo Elaborador de la Guía plantea la monitorización de las siguientes preguntas clínicas:
Pregunta clínica nº 1:
| ¿Es eficaz la terapia ocupacional en la mejoría de la independencia para las AVD en personas que han sufrido un ictus? |
Pregunta clínica nº 16:
| ¿Son eficaces las intervenciones multidisciplinares (fisioterapia + terapia ocupacional + logopedia…) en la mejoría de la independencia para las AVD en pacientes que han sufrido un ictus? |
Ambas preguntas fueron seleccionadas por su importancia y por la cantidad de estudios que se identificaron al realizar la actualización, lo que se asocia a una mayor probabilidad de que aparezcan nuevos estudios que aborden dichas preguntas.
Cronograma de ejecución de las búsquedas y evaluación del impacto de la nueva evidencia
Se crearán alertas de las búsquedas bibliográficas realizadas en las principales bases de datos biomédicas (MEDLINE, EMBASE y COCHRANE). A partir de la fecha de publicación de esta guía, cada seis meses se revisarán los artículos identificados en estas alertas.
Asimismo, contar con la coordinación clínica como informante clave permitirá identificar las publicaciones más relevantes lo antes posible, evitando así la obsolescencia de las recomendaciones elaboradas.
Para la evaluación de la nueva evidencia detectada, se contará con dos investigadores que analicen (por pares) los criterios de inclusión y exclusión. En caso de cumplir dichos criterios, se pondrá en conocimiento de GuíaSalud y se incorporará la nueva evidencia a la síntesis elaborada previamente.
En caso de considerar que la nueva evidencia podría modificar la recomendación en fuerza o dirección, se volverá a constituir el grupo de expertos para su discusión y acuerdo.
Autores
Grupo de trabajo de la GPC sobre el Manejo de Ictus en
Atención Primaria
Blanca Fuentes Gimeno, Jefa de Sección del Servicio de Neurología, Hospital Universitario La Paz,
Madrid.
Carmen Aleix Ferrer, Presidenta de la Federación Española de Ictus (FEI), Madrid.
Javier Gracia San Román, Director Médico- Innovación, Modelos de Cooperación, Suscripción y
Reclamos en Munich.Re (Grupo), Europa del Sur & LATAM, Münich.
Juan Carlos Bayón Yusta, Economista de la Salud, Servicio de Evaluación de Tecnologías Sanitarias
del Gobierno Vasco (Osteba) en la Fundación Vasca de Innovación Sanitaria (BIOEF), Barakaldo.
Juan Carlos Obaya-Rebollar, Médico de Familia, Centro de Salud de La Chopera, Servicio Madrileño de
Salud, Madrid.
Lorea Galnares Cordero, Documentalista, Servicio de Evaluación de Tecnologías Sanitarias del
Gobierno Vasco (Osteba) en la Fundación Vasca de Innovación Sanitaria (BIOEF), Barakaldo.
María Isabel Egocheaga Cabello, Médica de Familia, Centro de Salud de Isla de Oza, Servicio
Madrileño de Salud, Miembro del Comité Técnico de la Estrategia en Ictus del Sistema Nacional de
Salud, Madrid.
Nora Ibargoyen Roteta, Metodóloga, Servicio de Evaluación de Tecnologías Sanitarias del Gobierno
Vasco (Osteba) en la Fundación Vasca de Innovación Sanitaria (BIOEF), Barakaldo.
Raquel Ramírez Parrondo, Médica de Familia y de medicina psicosomática en Clínica Universidad de
Navarra, Madrid.
Coordinación metodológica
Nora Ibargoyen Roteta, Metodóloga, Servicio de Evaluación de Tecnologías Sanitarias del Gobierno
Vasco (Osteba) en la Fundación Vasca de Innovación Sanitaria (BIOEF), Barakaldo.
Colaboración
Nerea Arias Jayo, Directora Científica de Abyntek Biopharma, Zamudio.
Gaizka Benguria Arrate, Metodólogo, Servicio de Evaluación de Tecnologías Sanitarias del Gobierno
Vasco (Osteba) en la Fundación Vasca de Innovación Sanitaria (BIOEF), Barakaldo.
Colaboración experta
Ana Vena Martínez, Médica especialista en Geriatría, Hospital Universitario Santa María, Lleida
Raquel Cutillas Ruiz, Médica especialista en Medicina Física y rehabilitación, Fundación Jiménez Díaz,
Madrid.
Sara Laxe García, Médica especialista en Medicina Física y rehabilitación, Servicio de rehabilitación,
Hospital Clínic de Barcelona, Barcelona.
Blanca Garmendia Prieto, Facultativa especialista en Geriatría, Hospital Central de la Cruz Roja, San
José y Santa Adela, Madrid.
Esther San Cristobal Velasco, Médica Especialista en Geriatría, Hospital Monte Naranco, Oviedo.
Angel Lizcaíno Álvarez, Diplomado en Enfermería, Vicedecano y profesor del área de enfermería,
Universidad Rey Juan Calos, Madrid.
María José Planas García de Dios, Trabajadora Social Sanitaria, Centro de Salud de Corea, Dirección
Asistencial Este, SERMAS, Madrid.
María Carmen Soler González, Trabajadora Social Sanitaria, Hospital Universitario y Politécnico La Fe de
Valencia.
Revisión externa
Ángel Carlos Matía Cubillo, Médico de Familia, Centro de Salud Ignacio López Saiz, Burgos.
Yasmín Drak Hernández, Médica de Familia, Centro de Salud Sánchez Morate, Getafe.
Ana Vena Martínez, Médica especialista en Geriatría, Hospital Universitario Santa María, Lleida.
Carolina de Miguel Benadiba, Médica especialista en Medicina Física y rehabilitación, Hospital
Universitario Ramón y Cajal, Madrid.
Helena Bascuñana Ambròs, Médica especialista en Medicina Física y rehabilitación, Hospital de Sant
Pau, Barcelona.
Maria Pilar Sánchez Tarifa, Médica especialista en Medicina Física y rehabilitación, UGC. Hospital
Universitario Puerta del Mar y Puerto Real, Cádiz.
María José Peña Gascón, Enfermera Especialista en Enfermería familiar y comunitaria, Directora de
enfermería en AP, Sector III Zaragoza, Centro de Salud Seminario Condes de Aragón, Zaragoza.
Pedro García Martínez, Enfermero Especialista en Enfermería familiar y comunitaria, Escuela
Universitaria de Enfermería de la Fe, Valencia.
Agradecimientos
Queremos agradecer a Paloma Roset Monrós y a Beatriz Nieto Pereda por haber participado en la medida
de lo posible en la realización de esta guía.
Sociedades colaboradoras
Asociación Española de Trabajo Social y Salud (AETSYS).
Federación de asociaciones de enfermería comunitaria y atención primaria (FAECAP).
Sociedad Española de Geriatría y Gerontología (SEGG).
Sociedad Española de Medicina de Familia y Comunitaria (SEMFYC).
Sociedad Española de Médicos Generales y de Familia (SEMG).
Sociedad Española de Neurología (SEN).
Sociedad Española de Rehabilitación y Medicina Física (SERMEF).
Miembros de estas sociedades han participado en la autoría, colaboración experta o revisión externa
de la GPC.
Exposición pública
Esta GPC ha sido sometida a un proceso de Exposición Pública. El listado completo de los grupos de
interés que han participado en el proceso de exposición pública está disponible en la web de GuíaSalud:
www.guiasalud.es
Declaración de interés: Todos los miembros del Grupo de Trabajo, así como las personas que han
participado en la colaboración experta y en la revisión externa de esta guía, han realizado la declaración
de posibles conflictos de interés. Este documento podrá ser consultado, bajo petición, a través del Servicio
de Evaluación de Tecnologías del País Vasco (Osteba-BIOEF).
Bibliografía
1. Grupo de Trabajo de la Guía de Práctica Clínica para el manejo de pacientes con Ictus en Atención Primaria. Guía de Práctica Clínica para el manejo de pacientes con Ictus en Atención Primaria. Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad y Política Social. Unidad de Evaluación de Tecnologías Sanitarias de la Agencia Laín Entralgo de la Comunidad de Madrid; 2009. Guías de Práctica Clínica en el SNS: UETS Nº 2007/5-2.
2. Sociedad Española de Neurología. El Atlas del Ictus. España 2019. Disponible en: https://www.sen.es/images/2020/atlas/Atlas_del_Ictus_de_Espana_version_web.pdf.
3. Feigin VL, Brainin M, Norrving B, Martins S, Sacco RL, Hacke W, et al. World Stroke Organization (WSO): Global Stroke Fact Sheet 2022. Int J Stroke. 2022;17(1):18-29. DOI: 10.1177/17474930211065917
4. Díaz-Guzmán J, Egido JA, Gabriel-Sánchez R, Barberá-Comes G, Fuentes-Gimeno B, Fernández-Pérez C. Stroke and transient ischemic attack incidence rate in Spain: the IBERICTUS study. Cerebrovasc Dis. 2012;34(4):272-81. DOI: 10.1159/000342652
5. Soto A, Guillén-Grima F, Morales G, Muñoz S, Aguinaga-Ontoso I, Fuentes-Aspe R.[Prevalence and incidence of ictus in Europe: systematic review and metaanalysis]. An Sist Sanit Navar. 2022;45(1):e0979. DOI: 10.23938/ASSN.0979
6. Stevens E, Emmett E, Wang Y, McKevitt C, Wolfe CD. The burden of stroke in Europe. Appendix [Internet]. London: Stroke Alliance for Europe; 2017. Available from: http://www.strokeeurope.eu/downloads/The_Burden_of_Stroke_in_Europe_Report_-_Appendix.pdf.
7. Crichton SL, Bray BD, McKevitt C, Rudd AG, Wolfe CD. Patient outcomes up to 15 years after stroke: survival, disability, quality of life, cognition and mental health. J Neurol Neurosurg Psychiatry. 2016;87(10):1091-8. DOI: 10.1136/jnnp-2016-313361
8. Mar J, Arrospide A, Begiristain JM, Larrañaga I, Sanz-Guinea A, Quemada I. [Quality of life and burden of carers of patients with acquired brain injury]. Rev Esp Geriatr Geron-tol. 2011;46(4):200-5. DOI: 10.1016/j.regg.2011.01.010
9. Rico-Blázquez M, García-Sanz P, Martín-Martín M, López-Rodríguez JA, Morey-Montalvo M, Sanz-Cuesta T, et al. Effectiveness of a home-based nursing support and cognitive restructuring intervention on the quality of life of family caregivers in primary care: A pragmatic cluster-randomized controlled trial. Int J Nurs Stud. 2021;120:103955. DOI : 10.1016/j.ijnurstu.2021.103955
10. Wilkins E, Wilson L, Wickramasinghe K, Bhatnagar P, Leal J, Luengo-Fernandez R et al. European Cardiovascular Disease Statistics 2017. Brussels: European Heart Net-work, 2017. Available from: http://www.ehnheart.org/images/CVD-statistics-report-August-2017.pdf.
11. Grupo de trabajo de la Guía de prevención del ictus. Centro Cochrane Iberoamericano, coordinador. Guía de práctica clínica sobre la prevención primaria y secundaria del ictus. Madrid: Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad y Consumo. Agència d’Avaluació de Tecnologia i Recerca Mèdiques; 2008. Guía de práctica clínica: AATRM N.º 2006/15.
12. Sistema Nacional de Salud. Estrategia en Ictus del Sistema Nacional de Salud. Plan de Calidad Sistema Nacional de Salud. Ministerio de Sanidad y Consumo, 2008. [Internet]. Disponible en: https://www.sanidad.gob.es/bibliotecaPub/repositorio/libros/29231_estrategia_en_ictus_del_Sistema_Nacional_de_Salud_-_informe_de_evaluacion_y_lineas_ prioritarias_de_actuacion.pdf.
13. Egocheaga Cabello MI SAM, Peña Mateo MJ, Miranda Fernández-Santos C, Rodríguez Ledo MP. Conocimiento y actitudes sobre el ictus de los médicos de atención primaria. Med. Gen. Fam. 2021;10(6):263-71. DOI: 10.24038/mgyf.2021.056.
14. Lehnerer S, Hotter B, Padberg I, Knispel P, Remstedt D, Liebenau A, et al. Social work support and unmet social needs in life after stroke: a cross-sectional exploratory study. BMC Neurol. 2019;19(1):220. DOI: 10.1186/s12883-019-1451-y
15. Grupo de trabajo para la actualización del Manual de Elaboración de GPC. Elaboración de Guías de Práctica Clínica en el Sistema Nacional de Salud. Actualización del Manual Metodológico [Internet]. Madrid: Ministerio de Sanidad, Servicios Sociales e Igualdad; Zaragoza: Instituto Aragonés de Ciencias de la Salud (IACS); 2016. Disponible en: http://portal.guiasalud.es/emanuales/elaboracion_2/?capitulo.
16. Guyatt GH, Oxman AD, Kunz R, Vist GE, Falck-Ytter Y, Schünemann HJ. What is “quality of evidence” and why is it important to clinicians? Bmj. 2008;336(7651):995-8. DOI: 10.1136/bmj.39490.551019.BE
17. Alonso-Coello P, Schünemann HJ, Moberg J, Brignardello-Petersen R, Akl EA, Da-voli M, et al. GRADE Evidence to Decision (EtD) frameworks: a systematic and trans-parent approach to making well informed healthcare choices. 1: Introduction. Bmj. 2016;353:i2016. DOI: https://doi.org/10.1136/bmj.i2016
18. Zhelev Z, Walker G, Henschke N, Fridhandler J, Yip S. Prehospital stroke scales as screening tools for early identification of stroke and transient ischemic attack. Cochrane Database Syst Rev. 2019;4(4):Cd011427. DOI: 10.1002/14651858.CD011427.pub2
19. Oostema JA, Carle T, Talia N, Reeves M. Dispatcher Stroke Recognition Using a Stroke Screening Tool: A Systematic Review. Cerebrovasc Dis. 2016;42(5-6):370-7. DOI: 10.1159/000447459
20. Meyran D, Cassan P, Avau B, Singletary E, Zideman DA. Stroke Recognition for First Aid Providers: A Systematic Review and Meta-Analysis. Cureus. 2020;12(11):e11386. DOI: 10.7759/cureus.11386
21. Jones SP, Bray JE, Gibson JM, McClelland G, Miller C, Price CI, et al. Characteris-tics of patients who had a stroke not initially identified during emergency prehospital assessment: a systematic review. Emerg Med J. 2021;38(5):387-93. DOI: 10.1136/emermed-2020-209607
22. Ankolekar S, Fuller M, Cross I, Renton C, Cox P, Sprigg N, et al. Feasibility of an ambulance-based stroke trial, and safety of glyceryl trinitrate in ultra-acute stroke: the rapid intervention with glyceryl trinitrate in Hypertensive Stroke Trial (RIGHT, ISRCTN66434824). Stroke. 2013;44(11):3120-8. DOI: 10.1161/STROKEAHA.113.001301
23. Bath PMS, P.; Anderson, C.S.; Appleton, J.P.; Berge, E.; Cala, l.; and the RIGHT-2 In-vestigators. Prehospital transdermal glyceryl trinitrate in patients with ultra-acute pre-sumed stroke (RIGHT-2): an ambulance-based, randomised, sham-controlled, blinded, phase 3 trial. Lancet. 2019;393(10175):1009-20. DOI: 10.1016/S0140-6736(19)30194-1
24. Sandset EC, Anderson CS, Bath PM, Christensen H, Fischer U, Gąsecki D, Lal A, Manning LS, Sacco S, Steiner T, Tsivgoulis G. European Stroke Organisa-tion (ESO) guidelines on blood pressure management in acute ischaemic stroke and intracerebral haemorrhage. Eur Stroke J. 2021 Jun;6(2):XLVIII-LXXXIX. DOI: 10.1177/23969873211012133
25. Lim BL, Lee WF, Ng WM, Situ W, Loo KV, Man Goh CJ, et al. Benefits and safety of transdermal glyceryl trinitrate in acute stroke: A systematic review and meta-analysis of randomized trials. Acad Emerg Med. 2022;29(6):772-88. DOI: 10.1111/acem.14408
26. Guo QH, Liu CH, Wang JG. Blood Pressure Goals in Acute Stroke. Am J Hypertens. 2022;35(6):483-99. DOI: 10.1093/ajh/hpac039
27. Tsivgoulis G, Frey JL, Flaster M, Sharma VK, Lao AY, Hoover SL, et al. Pre-tissue plasminogen activator blood pressure levels and risk of symptomatic intracerebral hem-orrhage. Stroke. 2009;40(11):3631-4. DOI: 10.1161/STROKEAHA.109.564096
28. Mundiyanapurath S, Hees K, Ahmed N, Wahlgren N, Uhlmann L, Kieser M, et al. Pre-dictors of symptomatic intracranial haemorrhage in off-label thrombolysis: an analysis of the Safe Implementation of Treatments in Stroke registry. Eur J Neurol. 2018;25(2):340-e11. DOI: 10.1111/ene.13507
29. Bath PM, Krishnan K. Interventions for deliberately altering blood pressure in acute stroke. Cochrane Database Syst Rev. 2014;2014(10):Cd000039. DOI: 10.1002/14651858. CD000039.pub3
30. Kobayashi A, Czlonkowska A, Ford GA, Fonseca AC, Luijckx GJ, Korv J, et al. Euro-pean Academy of Neurology and European Stroke Organization consensus statement and practical guidance for pre-hospital management of stroke. Eur J Neurol. 2018;25(3):425-33. DOI: 10.1111/ene.13539
31. Nurmi J, Lindsberg PJ, Häppölä O, Klemetti E, Westerbacka J, Castrén M. Strict glucose control after acute stroke can be provided in the prehospital setting. Acad Emerg Med. 2011;18(4):436-9. DOI: 10.1111/j.1553-2712.2011.01020.x
32. Stroke Foundation. Clinical Guidelines for Stroke Management. Available at https://informme.org.au/guidelines/living-clinical-guidelines-for-stroke-management.
33. Middleton S, McElduff P, Ward J, Grimshaw JM, Dale S, D’Este C, et al. Implementation of evidence-based treatment protocols to manage fever, hyperglycaemia, and swallowing dysfunction in acute stroke (QASC): a cluster randomised controlled trial. Lancet. 2011;378(9804):1699-706. DOI: 10.1016/S0140-6736(11)61485-2
34. Fuentes B, Castillo J, San José B, Leira R, Serena J, Vivancos J, et al. The prognostic value of capillary glucose levels in acute stroke: the GLycemia in Acute Stroke (GLIAS) study. Stroke. 2009;40(2):562-8. DOI: 10.1161/STROKEAHA.108.519926
35. Fuentes B, Ntaios G, Putaala J, Thomas B, Turc G, Díez-Tejedor E. European Stroke Organisation (ESO) guidelines on glycaemia management in acute stroke. Eur Stroke J. 2018;3(1):5-21. DOI: 10.1177/2396987317742065
36. Green DM, O’Phelan KH, Bassin SL, Chang CW, Stern TS, Asai SM. Intensive versus conventional insulin therapy in critically ill neurologic patients. Neurocrit Care. 2010;13(3):299-306. DOI: 10.1007/s12028-010-9417-3
37. Chen ZM, Sandercock P, Pan HC, Counsell C, Collins R, Liu LS, et al. Indications for early aspirin use in acute ischemic stroke : A combined analysis of 40 000 randomized patients from the chinese acute stroke trial and the international stroke trial. On behalf of the CAST and IST collaborative groups. Stroke. 2000;31(6):1240-9. DOI: 10.1161/01. str.31.6.1240
38. Minhas JS, Chithiramohan T, Wang X, Barnes SC, Clough RH, Kadicheeni M, et al. Oral antiplatelet therapy for acute ischaemic stroke. Cochrane Database Syst Rev. 2022;1(1):Cd000029. DOI: 10.1002/14651858.CD000029.pub4
39. Stroke Foundation. Clinical guidelines for stroke management. Chapter 3 of 8: acute medical and surgical management. Available at https://app.magicapp.org/#/guideline/QnoKGn.
40. Shahjouei S, Sadighi A, Chaudhary D, Li J, Abedi V, Holland N, et al. A 5-Decade Analysis of Incidence Trends of Ischemic Stroke After Transient Ischemic Attack: A Systematic Review and Meta-analysis. JAMA Neurol. 2021;78(1):77-87. DOI: 10.1001/jamaneurol.2020.3627
41. Rothwell PM, Giles MF, Chandratheva A, Marquardt L, Geraghty O, Redgrave JN, et al. Effect of urgent treatment of transient ischaemic attack and minor stroke on early recurrent stroke (EXPRESS study): a prospective population-based sequential comparison. Lancet. 2007;370(9596):1432-42. DOI: 10.1016/S0140-6736(07)61448-2
42. Luengo-Fernandez R, Gray AM, Rothwell PM. Effect of urgent treatment for transient ischaemic attack and minor stroke on disability and hospital costs (EXPRESS study): a prospective population-based sequential comparison. Lancet Neurol. 2009;8(3):235-43. DOI: 10.1016/S1474-4422(09)70019-5
43. Luengo-Fernandez R, Li L, Silver L, Gutnikov S, Beddows NC, Rothwell PM. Long-Term Impact of Urgent Secondary Prevention After Transient Ischemic Attack and Minor Stroke: Ten-Year Follow-Up of the EXPRESS Study. Stroke. 2022;53(2):488-96. DOI: 10.1161/STROKEAHA.121.034279
44. Johnston SC, Rothwell PM, Nguyen-Huynh MN, Giles MF, Elkins JS, Bernstein AL, et al. Validation and refinement of scores to predict very early stroke risk after transient ischaemic attack. Lancet. 2007;369(9558):283-92. DOI: 10.1016/S0140-6736(07)60150-0
45. Giles MF, Rothwell PM. Risk of stroke early after transient ischaemic attack: a systematic review and meta-analysis. Lancet Neurol. 2007;6(12):1063-72. DOI: 10.1016/S1474-4422(07)70274-0
46. Mohan KM, Wolfe CD, Rudd AG, Heuschmann PU, Kolominsky-Rabas PL, Grieve AP. Risk and cumulative risk of stroke recurrence: a systematic review and meta-analysis. Stroke. 2011;42(5):1489-94. DOI: 10.1161/STROKEAHA.110.602615
47. Canadian Stroke Best Practices. Secondary Prevention Of Stroke. Triage and Initial Diagnostic Evaluation of Transient Ischemic Attack and Non-Disabling Stroke. 2020. Available at https://www.strokebestpractices.ca/recommendations/secondary-prevention-of-stroke/triage-and-initial-diagnostic-evaluation-of-transient-ischemic-attack-and-non-disabling-stroke.
48. Simpson DM, Gracies JM, Yablon SA, Barbano R, Brashear A. Botulinum neurotoxin versus tizanidine in upper limb spasticity: a placebo-controlled study. J Neurol Neurosurg Psychiatry. 2009;80(4):380-5. DOI: 10.1136/jnnp.2008.159657
49. Bes A, Eyssette M, Pierrot-Deseilligny E, Rohmer F, Warter JM. A multi-centre, double-blind trial of tizanidine, a new antispastic agent, in spasticity associated with hemiplegia. Curr Med Res Opin. 1988;10(10):709-18. DOI: 10.1185/03007998809111122
50. Medici M, Pebet M, Ciblis D. A double-blind, long-term study of tizanidine (‘Sirdalud’) in spasticity due to cerebrovascular lesions. Curr Med Res Opin. 1989;11(6):398-407. DOI: 10.1185/03007998909110141
51. Leijon G, Boivie J. Central post-stroke pain–a controlled trial of amitriptyline and carbamazepine. Pain. 1989;36(1):27-36. DOI: 10.1016/0304-3959(89)90108-5
52. Vranken JH, Dijkgraaf MG, Kruis MR, van der Vegt MH, Hollmann MW, Heesen M. Pregabalin in patients with central neuropathic pain: a randomized, double-blind, placebo-controlled trial of a flexible-dose regimen. Pain. 2008;136(1-2):150-7. DOI: 10.1016/j.pain.2007.06.033
53. Kim JS, Bashford G, Murphy KT, Martin A, Dror V, Cheung R. Safety and efficacy of pregabalin in patients with central post-stroke pain. Pain. 2011;152(5):1018-23. DOI: 10.1016/j.pain.2010.12.023
54. Vestergaard K, Andersen G, Gottrup H, Kristensen BT, Jensen TS. Lamotrigine for central poststroke pain: a randomized controlled trial. Neurology. 2001;56(2):184-90. DOI: 10.1212/wnl.56.2.184
55. Jungehulsing GJ, Israel H, Safar N, Taskin B, Nolte CH, Brunecker P, et al. Levetiracetam in patients with central neuropathic post-stroke pain–a randomized, double-blind, placebo-controlled trial. Eur J Neurol. 2013;20(2):331-7.DOI: 10.1111/j.1468-1331.2012.03857.x
56. Osawa A, Maeshima S, Tanahashi N. Water-swallowing test: screening for aspiration in stroke patients. Cerebrovasc Dis. 2013;35(3):276-81. DOI: 10.1159/000348683
57. Wu MC, Chang YC, Wang TG, Lin LC. Evaluating swallowing dysfunction using a 100- ml water swallowing test. Dysphagia. 2004;19(1):43-7. DOI: 10.1007/s00455-003-0030-x
58. Momosaki R, Abo M, Kakuda W, Kobayashi K. Applicability of the two-step thickened water test in patients with poststroke dysphagia: a novel assessment tool for paste food aspiration. J Stroke Cerebrovasc Dis. 2013;22(6):817-21. DOI: 10.1016/j.jstrokecerebrovasdis.2012.05.011
59. Zhou Z, Salle J, Daviet J, Stuit A, Nguyen C. Combined approach in bedside assessment of aspiration risk post stroke: PASS. Eur J Phys Rehabil Med. 2011;47(3):441-6.
60. Martino R, Silver F, Teasell R, Bayley M, Nicholson G, Streiner DL, et al. The Toronto Bedside Swallowing Screening Test (TOR-BSST): development and validation of a dysphagia screening tool for patients with stroke. Stroke. 2009;40(2):555-61. DOI: 10.1161/STROKEAHA.107.510370
61. Brodsky MB, Suiter DM, González-Fernández M, Michtalik HJ, Frymark TB, Venediktov R, et al. Screening Accuracy for Aspiration Using Bedside Water Swallow Tests: A Systematic Review and Meta-Analysis. Chest. 2016;150(1):148-63. DOI: 10.1016/j. chest.2016.03.059
62. Osawa A, Maeshima S, Matsuda H, Tanahashi N. Functional lesions in dysphagia due to acute stroke: discordance between abnormal findings of bedside swallowing assessment and aspiration on videofluorography. Neuroradiology. 2013;55(4):413-21. DOI: 10.1007/s00234-012-1117-6
63. Bartlett RS, Kenz MK, Wayment HA, Thibeault SL. Correlation Between EAT-10 and Aspiration Risk Differs by Dysphagia Etiology. Dysphagia. 2022;37(1):11-20. DOI: 10.1007/s00455-021-10244-0
64. Giraldo-Cadavid LF, Gutiérrez-Achury AM, Ruales-Suárez K, Rengifo-Varona ML, Barros C, Posada A, et al. Validation of the Spanish Version of the Eating Assessment Tool-10 (EAT-10spa) in Colombia. A Blinded Prospective Cohort Study. Dysphagia. 2016;31(3):398-406. DOI: 10.1007/s00455-016-9690-1
65. Zhang PP, Yuan Y, Lu DZ, Li TT, Zhang H, Wang HY, et al. Diagnostic Accuracy of the Eating Assessment Tool-10 (EAT-10) in Screening Dysphagia: A Systematic Review and Meta-Analysis. Dysphagia. 2023;38(1):145-58. DOI: 10.1007/s00455-022-10486-6
66. Cordier R, Joosten A, Clavé P, Schindler A, Bülow M, Demir N, et al. Evaluating the Psychometric Properties of the Eating Assessment Tool (EAT-10) Using Rasch Analysis. Dysphagia. 2017;32(2):250-60. DOI: 10.1007/s00455-016-9754-2
67. Wang R, Xiong X, Zhang C, Fan Y. [Reliability and validity of the Chinese Eating Assessment Tool (EAT-10) in evaluation of acute stroke patients with dysphagia]. Zhong Nan Da Xue Xue Bao Yi Xue Ban. 2015;40(12):1391-9. DOI: 10.11817/j.issn.1672-7347.2015.12.017
68. Speyer R, Cordier R, Kertscher B, Heijnen BJ. Psychometric properties of questionnaires on functional health status in oropharyngeal dysphagia: a systematic literature review. Biomed Res Int. 2014;2014:458678. DOI: 10.1155/2014/458678
69. Belafsky PC, Mouadeb DA, Rees CJ, Pryor JC, Postma GN, Allen J, et al. Validity and reliability of the Eating Assessment Tool (EAT-10). Ann Otol Rhinol Laryngol. 2008;117(12):919-24. DOI: 10.1177/000348940811701210
70. Dziewas R, Michou E, Trapl-Grundschober M, Lal A, Arsava EM, Bath PM, et al. Euro-pean Stroke Organisation and European Society for Swallowing Disorders guideline for the diagnosis and treatment of post-stroke dysphagia. Eur Stroke J. 2021;6(3):Lxxxixcxv. DOI: 10.1177/23969873211039721
71. Marin S, Ortega O, Serra-Prat M, Valls E, Pérez-Cordón L, Clavé P. Economic Evaluation of Clinical, Nutritional and Rehabilitation Interventions on Oropharyngeal Dysphagia after Stroke: A Systematic Review. Nutrients. 2023;15(7). DOI: 10.3390/nu15071714
72. Kotecki S, Schmidt R. Cost and effectiveness analysis using nursing staff-prepared thickened liquids vs. commercially thickened liquids in stroke patients with dysphagia. Nurs Econ. 2010;28(2):106-9, 13.
73. Pelczarska A, Jakubczyk M, Niewada M. The cost-effectiveness of food consistency modification with xanthan gum-based Nutilis Clear® in patients with post-stroke dysphagia in Poland. BMC Health Serv Res. 2020;20(1):552. DOI: 10.1186/s12913-020-05411-2
74. Swan K, Speyer R, Heijnen BJ, Wagg B, Cordier R. Living with oropharyngeal dysphagia: effects of bolus modification on health-related quality of life–a systematic review. Qual Life Res. 2015;24(10):2447-56.DOI: 10.1007/s11136-015-0990-y
75. Eom MJ, Chang MY, Oh DH, Kim HD, Han NM, Park JS. Effects of resistance expiratory muscle strength training in elderly patients with dysphagic stroke. NeuroRehabilitation. 2017;41(4):747-52. DOI: 10.3233/NRE-172192
76. Speyer R, Cordier R, Sutt AL, Remijn L, Heijnen BJ, Balaguer M, et al. Behavioural Interventions in People with Oropharyngeal Dysphagia: A Systematic Review and Meta-Analysis of Randomised Clinical Trials. J Clin Med. 2022;11(3). DOI: 10.3390/jcm11030685
77. Kim HD, Choi JB, Yoo SJ, Chang MY, Lee SW, Park JS. Tongue-to-palate resistance training improves tongue strength and oropharyngeal swallowing function in subacute stroke survivors with dysphagia. J Oral Rehabil. 2017;44(1):59-64. DOI: 10.1111/joor.12461
78. Choi JB, Shim SH, Yang JE, Kim HD, Lee DH, Park JS. Effects of Shaker exercise in stroke survivors with oropharyngeal dysphagia. NeuroRehabilitation. 2017;41(4):753-7. DOI: 10.3233/NRE-172145
79. Allida S, Cox KL, Hsieh CF, Lang H, House A, Hackett ML. Pharmacological, psychological, and non-invasive brain stimulation interventions for treating depression after stroke. Cochrane Database Syst Rev. 2020;1(1):Cd003437. DOI: 10.1002/14651858. CD003437.pub5
80. Legg LA, Rudberg AS, Hua X, Wu S, Hackett ML, Tilney R, et al. Selective serotonin reuptake inhibitors (SSRIs) for stroke recovery. Cochrane Database Syst Rev. 2021;11(11):Cd009286. DOI: 10.1002/14651858.CD009286.pub4
81. Jones JS, Kimata R, Almeida OP, Hankey GJ. Risk of Fractures in Stroke Patients Treated With a Selective Serotonin Reuptake Inhibitor: A Systematic Review and Meta-Analysis. Stroke. 2021;52(9):2802-8.DOI: 10.1161/STROKEAHA.120.032973
82. Deng L, Qiu S, Yang Y, Wang L, Li Y, Lin J, et al. Efficacy and tolerability of pharmacotherapy for post-stroke depression: a network meta-analysis. Oncotarget. 2018;9(34):23718-28. DOI: 10.18632/oncotarget.23891
83. Li X, Zhang C. Comparative efficacy of nine antidepressants in treating Chinese patients with post-stroke depression: A network meta-analysis. J Affect Disord. 2020;266:540-8. DOI: 10.1016/j.jad.2020.09.078
84. Qin B, Chen H, Gao W, Zhao LB, Zhao MJ, Qin HX, Chen W, Chen L, Yang MX. Efficacy, acceptability, and tolerability of antidepressant treatments for patients with post-stroke depression: a network meta-analysis. Braz J Med Biol Res. 2018;51(7):e7218. DOI: 10.1590/1414-431×20187218
85. Sun Y, Liang Y, Jiao Y, Lin J, Qu H, Xu J, et al. Comparative efficacy and acceptability of antidepressant treatment in poststroke depression: a multiple-treatments meta-analysis. BMJ Open. 2017;7(8):e016499.DOI: 10.1136/bmjopen-2017-016499
86. Chun HY, Newman R, Whiteley WN, Dennis M, Mead GE, Carson AJ. A systematic review of anxiety interventions in stroke and acquired brain injury: Efficacy and trial design. J Psychosom Res. 2018;104:65-75. DOI: 10.1016/j.jpsychores.2017.11.010
87. Knapp P, Campbell Burton CA, Holmes J, Murray J, Gillespie D, Lightbody CE, et al. Interventions for treating anxiety after stroke. Cochrane Database Syst Rev. 2017;5(5):Cd008860. DOI: 10.1002/14651858.CD008860.pub3
88. Allida S, Patel K, House A, Hackett ML. Pharmaceutical interventions for emotionalism after stroke. Cochrane Database Syst Rev. 2019;3(3):Cd003690. DOI: 10.1002/14651858.CD003690.pub5
89. Cao WW YJ, Sun SY, Sun YB, Luan L, Cai XJ, et al. Group psychotherapy in treatment of post stroke depression [团体心理治疗在脑卒中后抑郁治疗中的应用]. Chinese Mental Health Journal 2009;23(2):100-4. Available from: https://www.cochranelibrary. com/central/doi/10.1002/central/CN-00744478/full.
90. Wang X, He Y, Xiao C-L. A clinical trial of paroxetine and psychotherapy in pa-tients with poststroke depression and anxiety. Chinese mental health journal [Internet]. 2005; 19(8):[564-6 pp.]. Available from: https://www.cochranelibrary.com/central/doi/10.1002/central/CN-00712949/full.
91. Fens M, Vluggen T, van Haastregt JC, Verbunt JA, Beusmans GH, van Heugten CM. Multidisciplinary care for stroke patients living in the community: a systematic review. J Rehabil Med. 2013;45(4):321-30. DOI: 10.2340/16501977-1128
92. Vluggen T, van Haastregt JCM, Tan FE, Verbunt JA, van Heugten CM, Schols J. Ef-fectiveness of an integrated multidisciplinary geriatric rehabilitation programme for older persons with stroke: a multicentre randomised controlled trial. BMC Geriatr. 2021;21(1):134. DOI: 10.1186/s12877-021-02082-4
93. Feng W, Yu H, Wang J, Xia J. Application effect of the hospital-community integrated service model in home rehabilitation of stroke in disabled elderly: a randomised trial. Ann Palliat Med. 2021;10(4):4670-7. DOI: 10.21037/apm-21-602
94. Willeit P, Toell T, Boehme C, Krebs S, Mayer L, Lang C, et al. STROKE-CARD care to prevent cardiovascular events and improve quality of life after acute ischaemic stroke or TIA: A randomised clinical trial. EClinicalMedicine. 2020;25:100476. DOI: 10.1016/j.eclinm.2020.100476
95. Abdul Aziz AF, Mohd Nordin NA, Muhd Nur A, Sulong S, Aljunid SM. The integrated care pathway for managing post stroke patients (iCaPPS(©)) in public primary care Healthcentres in Malaysia: impact on quality adjusted life years (QALYs) and cost effec-tiveness analysis. BMC Geriatr. 2020;20(1):70. DOI: 10.1186/s12877-020-1453-z
96. Legg LA, Lewis SR, Schofield-Robinson OJ, Drummond A, Langhorne P. Occupational therapy for adults with problems in activities of daily living after stroke. Cochrane Data-base Syst Rev. 2017;7(7):Cd003585.DOI: 10.1002/14651858.CD003585.pub3
97. Forgea MC, Lyons AG, Lorenz RA. Barriers and Facilitators to Engagement in Rehabili-tation Among Stroke Survivors: An Integrative Review. Rehabil Nurs. 2021;46(6):340-7. DOI: 10.1097/RNJ.0000000000000340
98. Williams S, Murray C. The Experience of Engaging in Occupation following Stroke: A Qualitative Meta-Synthesis. British Journal of Occupational Therapy. 2013;76(8):370-378. DOI:10.4276/030802213X13757040168351
99. Hao Q, Tampi M, O’Donnell M, Foroutan F, Siemieniuk RA, Guyatt G. Clopidogrel plus aspirin versus aspirin alone for acute minor ischaemic stroke or high risk tran-sient ischaemic attack: systematic review and meta-analysis. Bmj. 2018;363:k5108. DOI: 10.1136/bmj.k5108
100. Johnston SC, Amarenco P, Denison H, Evans SR, Himmelmann A, James S, et al. Ti-cagrelor and Aspirin or Aspirin Alone in Acute Ischemic Stroke or TIA. N Engl J Med. 2020;383(3):207-17. DOI: 10.1056/NEJMoa1916870