La enfermedad renal crónica (ERC) se reconoce cada vez más como un problema de salud pública de gran importancia. La ERC se define como un conjunto de enfermedades heterogéneas que afectan la estructura y función renal. La variabilidad de su expresión clínica es debida, al menos en parte, a su etiopatogenia, la estructura del riñón afectada (glomérulo, vasos, túbulos o intersticio renal), su severidad y el grado de progresión.
En el año 2002, la publicación de las guías K/DOQI (Kidney Disease Outcome Quality Initiative) por parte de la National Kidney Foundation (NKF) sobre definición, evaluación y clasificación de la ERC supuso un paso importante en el reconocimiento de su importancia. Se promovió por primera vez una clasificación basada en estadios de severidad y se definió como una tasa de filtrado glomerular inferior a 60 mL/min/1,73 m2 o daño renal durante al menos tres meses. Siendo el daño renal la presencia de anormalidades estructurales o funcionales del riñón, que puedan provocar potencialmente un descenso de la tasa de filtrado glomerular1. Posteriormente, en 2012, el grupo de trabajo en ERC de las guías KDIGO (Kidney Disease: Improving Global Outcomes), añadió en la definición y la clasificación, la evaluación de las causas y de la albuminuria respectivamente, debido a que estos dos factores pueden afectar directamente al pronóstico y a la elección del tratamiento2. Las causas principales de ERC en países desarrollados son la diabetes y la hipertensión, mientras que en países en vías de desarrollo son principalmente las causas de tipo infeccioso, tóxico o desconocido3,4.
La incidencia y la prevalencia global de la ERC están probablemente subestimadas debido al uso de diferentes clasificaciones a lo largo del tiempo. Los resultados de un reciente estudio sobre el impacto de diferentes patologías a nivel mundial, mostró que la ERC fue, en 1990, la causa número 27 en número de muertes totales (15,7 por 100.000). En cambio en el año 2010 se situó en el número 18, causando 16,3 muertes por 100.000 habitantes (tasas estandarizadas por edad)5. Probablemente se deba a un mejor reconocimiento de la ERC como causa de muerte junto a la diabetes o la enfermedad vascular. Diferentes estudios han estimado que más del 10% de la población mundial sufre algún grado de enfermedad renal crónica, de hecho bastante similar a los datos disponibles de diabetes6. Hay una amplia variabilidad en estos datos debido a las medidas utilizadas y la propia variabilidad en las características socio-demográficas de las personas afectadas entre los diferentes países y regiones7-11. Por el contrario, el 80% de las personas con ERC avanzada en fase de tratamiento sustitutivo, se encuentran en países desarrollados por lo que en los próximos años se prevé un incremento muy importante de pacientes en este estadío a medida que países como China o India incrementen su esperanza de vida12. Según la Kidney Disease Outcomes Quality Initiative, se estima que en España la prevalencia global de ERC en estadios 3-5 es aproximadamente, del 6,8%; siendo del 3,3% para edades 40-64 años y del 21,4% para edades >64 años13.
La ERC presenta importantes relaciones con otras enfermedades y particularmente con la enfermedad cardiovascular. Numerosos estudios han encontrado una relación lineal entre el grado de insuficiencia renal (medido por tasa de filtrado glomerular) y la mortalidad vascular. En personas con ERC en estadio 3 el riesgo de muerte de causa vascular se duplica en relación a una persona sin enfermedad renal y es hasta cuatro veces superior en personas con ERC en estadio 4. La presencia de albuminuria parece también relacionarse de forma independiente con un aumento de riesgo vascular y un aumento –incluso en el límite superior de la normalidad– debe considerarse de riesgo14,15. Además, la enfermedad cardiovascular es un factor reconocido de progresión a fases avanzadas de enfermedad renal. En España no hay muchos estudios sobre el riesgo de enfermedad vascular en personas con ERC. El estudio MERENA, mostró que la prevalencia de enfermedad vascular en los pacientes con ERC estadios 3 y 4 es del 39,1%, siendo más elevada en pacientes con estadio 4 que en pacientes en estadio 316.
Debido a la compleja etiopatogenia y las interrelaciones con otras patologías y condiciones, es probable que la prevención mediante las intervenciones habituales en factores de riesgo sea menos eficaz y que sea necesario investigar en nuevas estrategias como, por ejemplo, la prevención precoz, el diseño de objetivos terapéuticos sobre factores no tradicionales o intervenciones multifactoriales. En este sentido, existen dudas si ciertas intervenciones sobre los factores de riesgo son igualmente eficaces en los pacientes con ERC. Tal es el caso del tratamiento de la dislipemia con estatinas. También existe controversia sobre el objetivo de cifra de presión arterial para prevenir la progresión de la ERC y reducir los eventos vasculares. Las estrategias basadas en el auto-cuidado de estos pacientes están siendo investigadas actualmente. Finalmente, tampoco está del todo claro cuál ha de ser la población objetivo para realizar un cribado de ERC, ni qué pruebas son las ideales ni si estas estrategias de cribado se pueden traducir en una menor morbi-mortalidad a medio-largo plazo.
Todo ello justifica que la presente GPC disponga de un amplio capítulo dedicado a las intervenciones preventivas, tanto de la progresión de la propia enfermedad renal como de la enfermedad vascular. El grupo elaborador también es consciente que la complejidad de los pacientes con enfermedad renal, principalmente por la comorbilidad asociada, requiere a menudo de una atención dirigida a nivel individual, más allá de las recomendaciones de esta GPC.
1.1. Criterios diagnósticos de la enfermedad renal crónica
La definicón actual de ERC se basa en la propuesta por parte de la National Kidney Foundation (NKF) en las guías K/DOQI (Kidney Disease Outcome Quality Initiative) en el año 2002 y porsteriormente adoptadas por las guías KDIGO (Kidney Disease: Improving Global Outcomes) en 20041. En el año 2012 se publicó la actualización de las guías KDIGO que realizaron una serie de recomendaciones sobre el diagnóstico y clasificación de la ERC que han sido aceptadas e implemetadas ampliamente2. En nuestro entorno, diferentes sociedades científicas han adoptado estos mismos criterios en un reciente documento de consenso para la detección y manejo de la ERC19,20.
Aunque la definición general de ERC no ha variado desde la popuesta de las guías K/DOQI, el grupo de trabajo de las guías KDIGO detalló una serie de criterios diagnósticos y propusieron una clasificación para la estratificación del riesgo. Más que recomendaciones, el grupo de trabajo realizó propuestas que se basaron en la descripción de los resultados de un número importante de estudios de diseños diversos. Por este motivo no se graduaron ni la calidad de la evidencia ni la fuerza de las recomendaciones, que el grupo de trabajo presenta como propuestas basadas en el sentido común.
El grupo de trabajo de esta guía reconoce que la clasificación y los criterios propuestos por las guías KDIGO son válidos y son utilizados de forma general en nuestro entorno. Por ello la clasificación y los criterios que se proponen a continuación son una adaptación de estas guías.
Tabla 1. Criterios para la definición de enfermedad renal crónica

Adaptada de: Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney inter., Suppl. 2013; 3:1-150.
La propuesta del grupo de trabajo de las guías KDIGO se basa en la clasificación de la ERC, según la función renal calculada con la medición del filtrado glomerular estimada (ecuaciones de estimación del filtrado glomerular en el anexo 2), además de la presencia de albúmina en la orina y la causa. Por lo que se refiere a la causa, diferencia la presencia de enfermedad sistémica o causa renal primaria, así como la localización principal en el sistema renal (afectación glomerular, túbulo-intersticial, vascular o alteración quística o congénita).
La clasificación de la ERC por categorías según el filtrado glomelular se resume en la siguiente tabla:
Tabla 2. Clasificación de la ERC por categorías según el filtrado glomerular
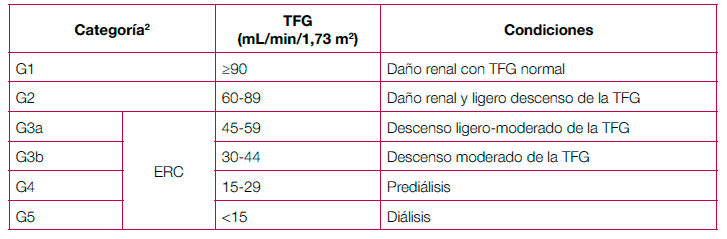
Adaptada de: Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney inter., Suppl. 2013; 3: 1-150.
La clasificación de la ERC por categorías, según el filtrado glomerular, se resume en la siguiente tabla:
Tabla 3.Clasificación de la ERC por categorías según la albuminuria

Adaptada de: Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation
and Management of Chronic Kidney Disease. Kidney inter., Suppl. 2013; 3: 1-150.
A partir de los resultados de un meta-análisis, de un total de 45 estudios observacionales que incluyeron más de un millón y medio de pacientes, se estableció la relación entre la estimación del filtrado glomerular y la excreción de albúmina con la mortalidad, la mortalidad vascular, el fallo renal y la progresión de la enfermedad renal crónica. Los resultados permitieron realizar unos nomogramas para la estimación del pronóstico que son ampliamente utilizados18.
Tabla 4. Pronóstico de la enfermedad renal crónica por filtrado glomerular estimado y albuminuria
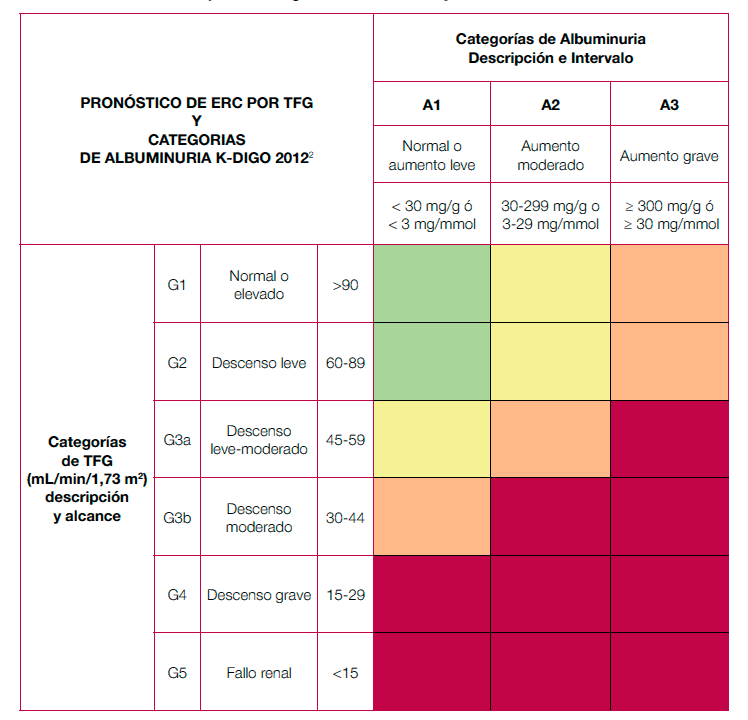
El riesgo menor corresponde al color verde (categoría de «bajo riesgo» y si no hay datos de lesión renal no se puede catalogar ni siquiera como ERC), seguido del color amarillo (riesgo «moderadamente aumentado»), naranja («alto riesgo») y rojo («muy alto riesgo»), que expresan riesgos crecientes para los eventos mencionados.
Adaptada de: Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney inter., Suppl. 2013; 3:1-150.
Bibliografía 1. Introducción
1. K/DOQI clinical practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Am J Kidney Dis. 2002;39 (2 Suppl 1):S1-266.
2. Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney inter., Suppl. 2013;3:1–150.
3. Engelgau MM, El-Saharty S, Kudesia P, et al. Regional aging and disease burden. In: Capitalizing on the demographic transition: tackling noncommunicable diseases in South Asia. Washington, DC: World Bank. 2011:15–40.
4. Ayodele OE, Alebiosu CO. Burden of chronic kidney disease: an international perspective. Adv Chronic Kidney Dis. 2010;17:215–24.
5. Lozano R, Naghavi M, Foreman K, et al. Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet. 2013;380:2095–128.
6. James MT, Hemmelgarn BR, Tonelli M. Early recognition and prevention of chronic kidney disease. Lancet. 2010;375:1296–309.
7. Feehally J. Ethnicity and renal disease. Kidney Int. 2005;68:414–24.
8. McDonald SP, Maguire GP, Hoy WE. Renal function and cardiovascular risk markers in a remote Australian Aboriginal community. Nephrol Dial Transplant. 2003;18:1555–61.
9. Ashton CW, Duffie D. Chronic kidney disease in Canada’s First Nations: results of an effective cross-cultural collaboration. Healthcare Q. 2011;14:42–7.
10. Rajapurkar MM, John GT, Kirpalani AL, et al. What do we know about chronic kidney disease in India: first report of the Indian CKD registry. BMC Nephrol. 2012;13:10.
11. Zhang L, Wang F, Wang L, et al. Prevalence of chronic kidney disease in China: a cross-sectional survey. Lancet. 2012;379:815–22.
12. White SL, Chadban SJ, Jan S, et al. How can we achieve global equity in provision of renal replacement therapy? Bull World Health Organ. 2008;86:229–37.
13. Otero A, de Francisco A, Gayoso P, et al. EPIRCE Study Group. Prevalence of chronic renal disease in Spain: results of the EPIRCE study. Nefrologia. 2010;30(1):78-86
14. Van der Velde M, Matsushita K, Coresh J, et al, for the Chronic Kidney Disease Prognosis Consortium. Lower estimated glomerular filtration rate and higher albuminuria are associated with all cause and cardiovascular mortality. A collaborative meta-analysis of high-risk population cohorts. Kidney Int. 2011;79:1341–52.
15. Matsushita K, van der Velde M, Astor BC, et al, for the CKD Prognosis Consortium. Association of estimated glomerular filtration rate and albuminuria with all-cause and cardiovascular mortality in general population cohorts: a collaborative meta-analysis. Lancet. 2010;375: 2073–81.
16. Martinez-Castelao A, Gorriz JL, Portoles JM, et al. Baseline characteristics of patients with chronic kidney disease stage 3 and stage 4 in Spain: the MERENA observational cohort study. BMC Nephrol. 2011;12:53.
17. National Collaborating Centre for Chronic Conditions. Chronic kidney disease: national clinical guideline for early identification and management in adults in primary and secondary care. London: Royal College of Physicians, September 2008.
18. Levey AS, de Jong PE, Coresh J et al. The definition, classification, and prognosis of chronic kidney disease: a KDIGO Controversies Conference report. Kidney Int. 2011;80:17–28.
19. Martínez-Castelao A, Górriz JL, Bover J, et al. Documento de consenso para la detección y manejo de la enfermedad renal crónica. Nefrologia. 2014;34(2):243-62.
20. Montañés Bermúdez R, Gracia García S, Pérez Surribas D, et al. Sociedad Española de Bioquímica Clínica y Patología Molecular; Sociedad Española de Nefrología. Documento de Consenso. Recomendaciones sobre la valoración de la proteinuria en el diagnóstico y seguimiento de la enfermedad renal crónica. Nefrologia. 2011;31(3):331-45.






